溴化芐 Benzyl Bromide
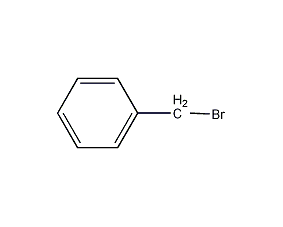
結構式
| 物競編號 | 02HS |
|---|---|
| 分子式 | C7H7Br |
| 分子量 | 171.03 |
| 標簽 | α-溴甲苯, 溴芐, 溴甲苯, 溴甲基苯, 溴化芐, 芐基溴, 苯甲溴, 1-Bromotoluene, α-Bromo-toluene, Bromophenylmethane, 發泡劑, 鹵代烴類溶劑 |
編號系統
CAS號:100-39-0
MDL號:MFCD00000172
EINECS號:202-847-3
RTECS號:XS7965000
BRN號:385801
PubChem號:24848056
物性數據
1.性狀:無色液體,有芳香氣味,具有催淚性。[10]
2.熔點(℃):-4.0[11]
3.沸點(℃):198[12]
4.相對密度(水=1):1.44[13]
5.相對蒸氣密度(空氣=1):5.8[14]
6.飽和蒸氣壓(kPa):0.133(32℃)[15]
7.燃燒熱(kJ/mol):-4278.2[16]
8.辛醇/水分配系數:2.92[17]
9.閃點(℃):79(CC)[18]
10.溶解性:不溶于水,溶于乙醇、乙醚、苯。[19]
毒理學數據
1、 致突變性:突變微生物試驗:細菌-鼠傷寒沙門氏菌,300μmol/L; 非定性DNA綜合試驗:細菌-大腸桿菌,1300μmol/L; 姐妹染色單體交換試驗:倉鼠卵巢,30μmol/L;
2、對眼睛和黏膜有強刺激作用。對機體有不可逆損傷的可能性。
3.其他[20] LCLo:2000mg/m3(兔吸入,30min)
生態學數據
1.生態毒性 暫無資料
2.生物降解性 暫無資料
3.非生物降解性[21] 空氣中,當羥基自由基濃度為5.00×105個/cm3時,降解半衰期為7.1d(理論)。在25℃時,水解半衰期為79min(理論)。
4.生物富集性[22] BCF:35(理論)
分子結構數據
1、摩爾折射率:38.90
2、摩爾體積(cm3/mol):118.9
3、等張比容(90.2K):296.2
4、表面張力(dyne/cm):38.4
5、介電常數:
6、偶極距(10-24cm3):
7、極化率:15.42
計算化學數據
1.疏水參數計算參考值(XlogP):無
2.氫鍵供體數量:0
3.氫鍵受體數量:0
4.可旋轉化學鍵數量:1
5.互變異構體數量:無
6.拓撲分子極性表面積0
7.重原子數量:8
8.表面電荷:0
9.復雜度:55.4
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:1
性質與穩定性
1.化學性質活潑,溴原子易被羥基、氨基等取代生成芐醇、芐胺等。
2.穩定性[23] 穩定
3.禁配物[24] 堿類、胺類、強氧化劑、醇類
4.避免接觸的條件[25] 受熱
5.聚合危害[26] 不聚合
6.分解產物[27] 溴化氫
貯存方法
儲存注意事項[28] 儲存于陰涼、通風的庫房。遠離火種、熱源。保持容器密封。應與氧化劑、堿類、胺類、醇類、食用化學品分開存放,切忌混儲。配備相應品種和數量的消防器材。儲區應備有泄漏應急處理設備和合適的收容材料。
合成方法
由甲苯溴化而得。將甲苯加熱到50℃,加溴反應,反應溫度為75-80℃,反應6h,在常壓下分餾除去140℃以前的餾分,然后減壓蒸餾,收集112-114℃(2.0kPa)餾分,得芐基溴。
用途
1.芐溴的最大用途是作為雜原子官能團的芐基化試劑,在各種條件下能有效地對各種雜原子官能團發生芐基化,從而在有機合成中具有廣泛的用途 (主要是作為保護基團使用)[1]。
醇和酚能與芐溴在堿性條件下發生反應。如在醚類或DMF溶劑中,將醇用NaH或KH處理得到烷氧化合物,進而與芐溴發生Williamson反應[2]。在低溫下,一級醇相比二級醇能更優先發生芐基化反應。除了NaH和KH堿性體系外,使用KF/Al或Ag2O同樣可以作為堿體系誘導醇的芐基化反應。
芐基化反應在糖類化合物中的應用非常成功。首先將糖類衍生物用錫試劑預處理,然后發生芐基化反應,這樣可以在軸向羥基存在下選擇性地實現平伏羥基的保護 (式1)[3]。
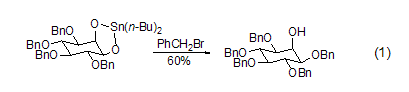
對于空間位阻較大的醇化合物的芐基化反應,可以采取加入催化劑量的碘試劑如(n-Bu)4NI作為碘源,將芐溴轉變為活性更高的芐碘,從而更容易實現芐基化反應。由于酚類化合物相比脂肪醇化合物具有更強的酸性,因此,酚的芐基化反應只需要弱堿如碳酸鉀即可實現[4]。
芐溴也可以保護胺類化合物的含氮基團。反應也需要在堿性條件下完成,并且對于一級胺的反應主要產物是雙芐基化產物[5]。此外,酰胺、內酰胺、磺酰胺以及含氮雜環均能與芐溴反應。
含硫化合物如硫醇、硅基硫醚等也能在堿性條件下與芐溴發生反應,如L-半胱氨酸與芐溴在氫氧化鈉堿液中的反應 (式2)。在DMF溶劑或羰基鋅的作用下,芐溴也能與羧酸陰離子反應制備芐基羧酸酯化合物[6]。
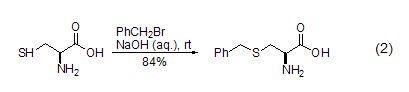
芐溴還能與帶活潑亞甲基的化合物如烯醇式酮、酯、1,3-二羰基化合物、酰胺、內酰胺以及硝基穩定的碳陰離子發生烷基化反應。如芐溴與金屬烯胺在手性亞胺作用下發生的芐基化反應能夠獲得較好的對映選擇性 (式3)[7]。

芐溴與活潑金屬反應制備芐基金屬化合物(如芐基鋰)很難實現,主要原因是生成的化合物能容易發生Wurz偶聯反應[8]。但也有例外,如芐基溴化鎂、芐基溴化鋅以及BnCu(CN)ZnBr均是成功的例子。
芐溴傾向于與有機金屬化合物如烷基鋰、格氏試劑、烷基酮等發生偶聯反應。如芐溴與N-甲基鄰苯二甲酰亞胺在Li的作用下發生的偶聯反應 (式4)[9]。
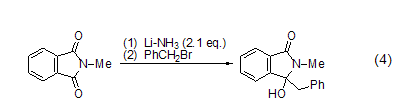
2.用于有機合成及制造發泡劑。[29]
安全信息
危險運輸編碼:UN 1737 6.1/PG 2
危險品標志: 刺激
刺激
安全標識:S39
危險標識:R36/37/38
文獻
1. (a) Greene, T. W.; Wuts, P. G. M. Protective Groups in Organic Synthesis, 2nd ed.; Wiley: New York, 1991. (b) Protective Groups in Organic Chemistry, McOMie, J. F. W., Ed.; Plenum: New York, 1973. 2. Nicolaou, K. C.; Pavia, M. R.; Seitz, S. P. J. Am. Chem. Soc., 1981, 103, 1224. 3. (a) Nashed, M. A.; Anderson, L. Tetrahedron Lett., 1976, 3503. (b) Cruzado, C.; Bernabe, M.; Martin-Lomas, M. J. Org. Chem., 1989, 54, 465. 4. Schmidhammer, H.; Brossi, A. J. Org. Chem., 1971, 36, 746. 5. Yamazaki, N.; Kibayashi, C. J. Am. Chem. Soc., 1989, 111, 1396. 6. Shono, T.; Ishige, O.; Uyama, H.; Kashimura, S. J. Org. Chem., 1986, 51, 546. 7. Saigo, K.; Kashahara, A.; Ogawa, S.; Nohira, H. Tetrahedron Lett., 1983, 24, 511. 8. Wakefield, B. J. Organolithium Methods, Academic: New York, 1988. 9. Flynn, G. A. Chem. Commun. 1980, 862. [1~9]參考書:現代有機合成試劑<性質、制備和反應>;胡躍飛 付華 編著;化學工業出版社;ISBN 7-5025-8542-7 [10~29]參考書:危險化學品安全技術全書.第一卷/張海峰主編.—2版.北京;化學工業出版社,2007.6 ISBN 978-7-122-00165-8
備注
暫無
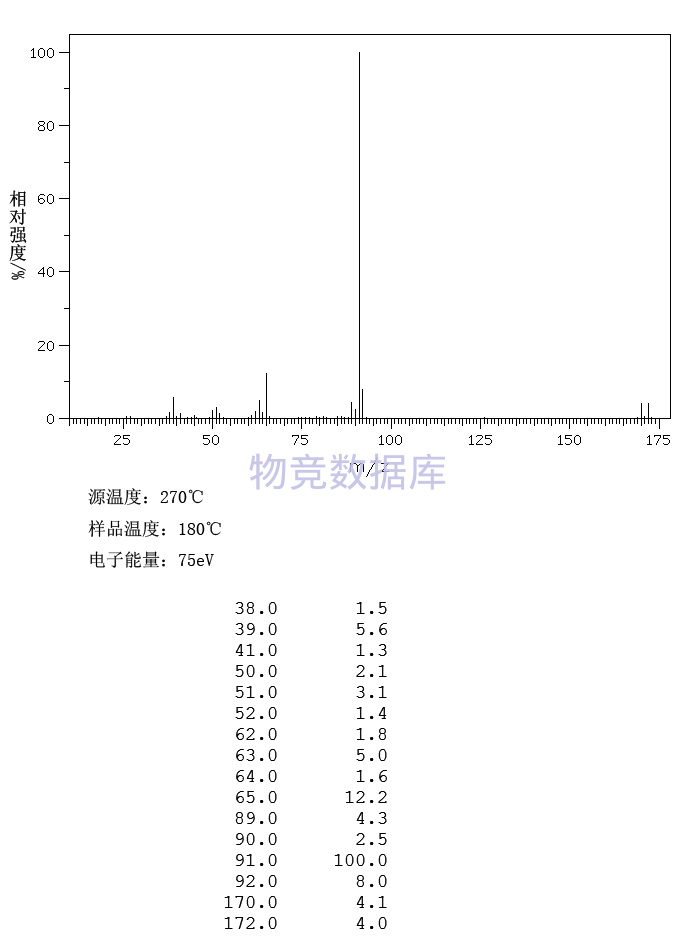
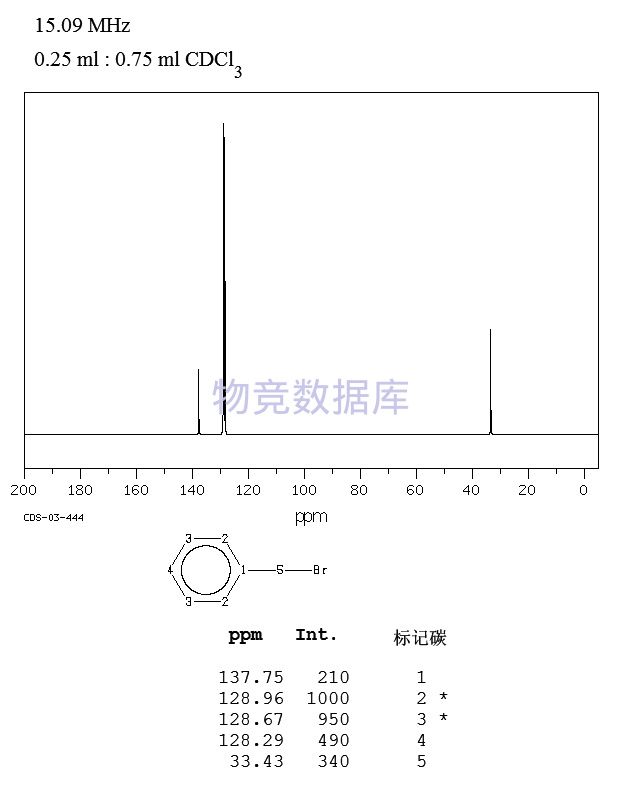
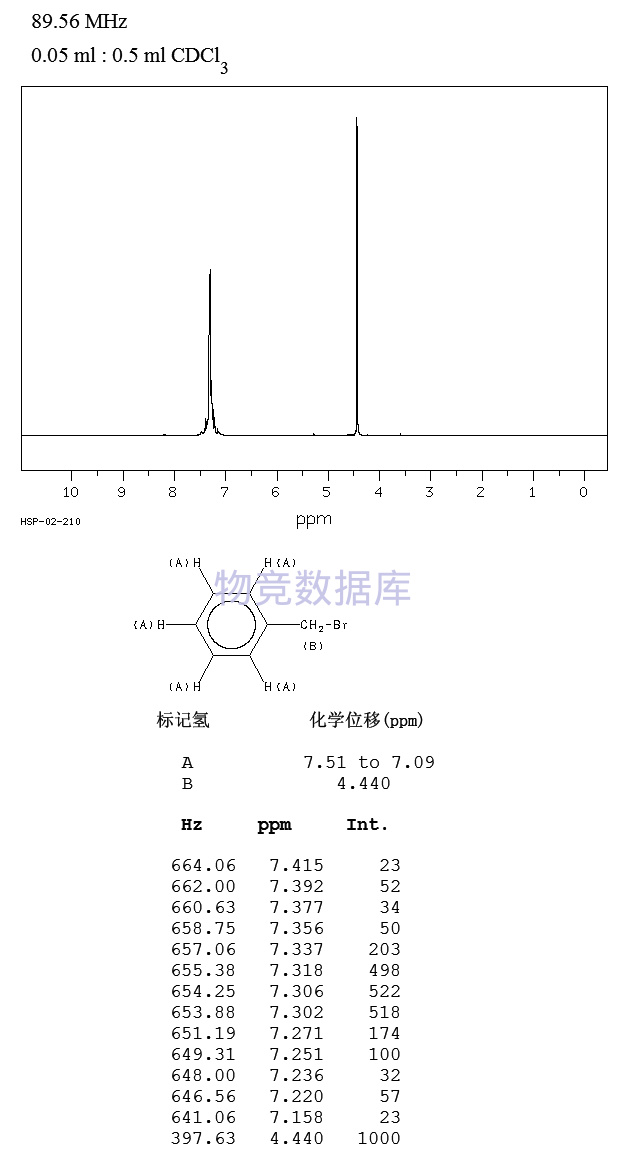
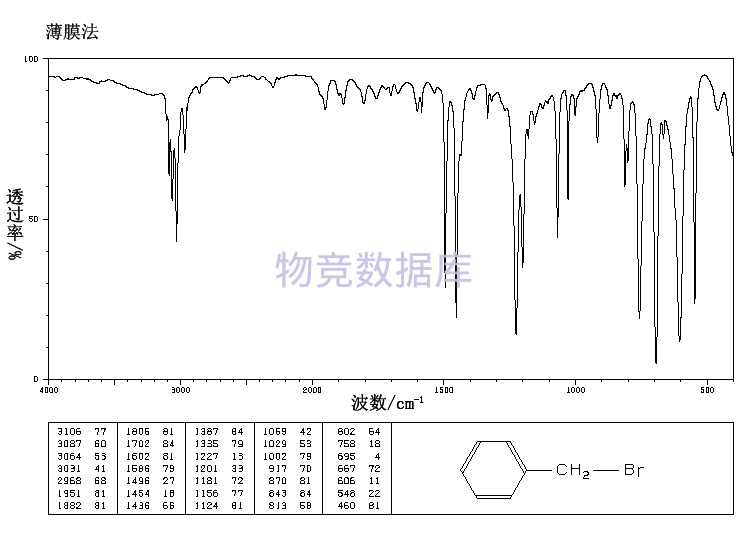
表征圖譜
統計數據
共收錄化學品數據
147579 條



 滬公網安備 31010602001115號
滬公網安備 31010602001115號