硫酸 Sulfuric acid
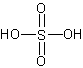
結構式
| 物競編號 | 0JY3 |
|---|---|
| 分子式 | H2SO4 |
| 分子量 | 98.08 |
| 標簽 | 磺鏹水, 硫鏹水, Battery acid, Hydrogen sulfate, Oil of vitriol, 脫水劑, 氧化劑, 助硝化劑, 酸洗劑, 磺化劑, 催化劑, 蓄電池化學品 |
編號系統
CAS號:7664-93-9
MDL號:MFCD00064589
EINECS號:231-639-5
RTECS號:WS5600000
BRN號:2037554
PubChem號:24873388
物性數據
1.性狀:純品為無色透明油狀液體,無臭。[1]
2.熔點(℃):10~10.49[2]
3.沸點(℃):330[3]
4.相對密度(水=1):1.84[4]
5.相對蒸氣密度(空氣=1):3.4[5]
6.飽和蒸氣壓(kPa):0.13(145.8℃)[6]
7.臨界壓力(MPa):6.4[7]
8.辛醇/水分配系數:-2.2[8]
9.溶解性:與水、乙醇混溶。[9]
10.熔點(oC,98%):10.46
11.熔點(oC,95.05%):-16.5
12.熔點(oC,90.65%):-25
13.沸點(oC,101.3kPa,98%):210~338
14.沸點(oC,101.3kPa,95%):297
15.沸點(oC,101.3kPa,90.6%):259
16.折射率(94.11%):1.42879
17.折射率(60.98%):1.40998
18.黏度(mPa·s,25oC,98.3%):20.2
19.比熱容(KJ/(kg·K),16~20oC,100%):1.39
20.蒸發熱(KJ/(kg/mol),326oC):50.16
21.生成熱(KJ/mol,SO2·O·H2O):224.00
22.生成熱(KJ/mol,SO3·H2O):89.26
23.生成熱(KJ/mol,H2SO4·H2O):40.83
24.壓縮系數(18.2~22oC,63%,8.1MPa):0.0000242
25.壓縮系數(18.2~22oC,91.7%,8.1MPa):0.0000250
26.電導率(S/m,18oC,30%):0.7388
27.電導率(S/m,18oC,85%):0.098
28.電導率(S/m,18oC,90%):0.1102
29.電導率(S/m,18oC,99.4%):0.0085
毒理學數據
1、急性毒性:LD50:2140 mg/kg(大鼠經口) LC50:510mg/m3,2小時(大鼠吸入);320mg/m3,2小時(小鼠吸入)
2、硫酸有極強的腐蝕性和吸水性,能嚴重燒傷人體,故接觸或使用硫酸時,工作人員必須做好防護。含量低于76%的硫酸與金屬反應時會放出氫氣。
3、稀釋硫酸時,只能將濃硫酸逐漸加入到水中,切不可將水加入濃硫酸中以免發生危險。吸入高濃度硫酸酸霧能引起上呼吸道刺激癥狀,嚴重者發生喉頭水腫,支氣管炎,細支氣管肺炎和肺水腫等。皮膚接觸濃硫酸引起嚴重灼傷。濺入眼內引起結膜炎、水腫,角膜渾濁以至穿孔。口服濃硫酸1mL即可致死。TJ 36-79規定車間空氣中最高容許濃度為2mg/m3。
4.急性毒性[10]
LD50:2140mg/kg(大鼠經口)
LC50:510mg/m3(大鼠吸入,2h);320mg/m3(小鼠吸入,2h)
5.刺激性[11] 家兔經眼:1380μg,重度刺激。
6.亞急性與慢性毒性[12] 牛長期每天攝入含硫酸的飲水(劑量110~190mg/kg),出現疲乏,外觀極度衰弱,以致轉入死亡。狗長期攝入含硫酸(115mg/kg)飲水,出現腹瀉。
7.致癌性[13] IARC致癌性評論:G1,確認人類致癌物。
生態學數據
1.生態毒性[14] TLm:42mg/L(48h)(食蚊魚);49mg/L(48h)(藍鰓太陽魚)
2.生物降解性 暫無資料
3.非生物降解性 暫無資料
4.其他有害作用[15] 該物質對環境有危害,應特別注意對水體和土壤的污染。
分子結構數據
1、摩爾折射率:13.92
2、摩爾體積(cm3/mol):44.5
3、等張比容(90.2K):148.8
4、表面張力(dyne/cm):124.1
5、極化率(10-24cm3):5.52
計算化學數據
1、疏水參數計算參考值(XlogP):-1.4
2、氫鍵供體數量:2
3、氫鍵受體數量:4
4、可旋轉化學鍵數量:0
5、互變異構體數量:無
6、拓撲分子極性表面積(TPSA):83
7、重原子數量:5
8、表面電荷:0
9、復雜度:81.3
10、同位素原子數量:0
11、確定原子立構中心數量:0
12、不確定原子立構中心數量:0
13、確定化學鍵立構中心數量:0
14、不確定化學鍵立構中心數量:0
15、共價鍵單元數量:1
性質與穩定性
1.暴露在空氣中迅速吸收水分,也能奪取有機物如糖、木等中的水分子而碳化。冷卻時能凝成結晶,此結晶在10.37℃熔化。但液態硫酸易形成過冷液體。純硫酸在290℃沸騰,98.3%的硫酸為恒沸物,沸點為330℃。濃硫酸有強烈的吸水性,是良好的干燥劑。
2.與水混溶。濃硫酸對一些無機和有機化合物都有一定的溶解能力,雖然可作某些反應的溶劑使用,但是長時間在高溫處于穩定狀態的化合物很少。例如己烷、庚烷、辛烷等在室溫下與硫酸不反應,但加熱到硫酸的沸點附近則可發生磺化反應。乙烯被硫酸吸收后生成乙烯硫酸酯。丙烯更易被硫酸吸收生成丙烯硫酸酯及其他各種化合物。硫酸吸收乙炔后生成磺酸酯。濃硫酸可以溶解聚酰胺,例如具有下列結構的聚酰胺可以溶解在濃度為80%~100%的硫酸中,特別是在95%以上的硫酸中,室溫下穩定,性能良好。甚至含6%~7%SO3的發煙硫酸也常用作這類聚合物的溶劑。
3.化學性質:硫酸加熱到290℃時開始分解,放出三氧化硫。317℃形成共沸混合物,轉變成組成為98.54%的水溶液。濃硫酸與水混合時產生大量的熱。濃硫酸對多種化合物都有脫水作用。例如蔗糖、紙等都因脫水而游離出碳。乙醇與濃硫酸一起加熱時脫水變成乙烯。一般有機化合物除發生脫水作用外,還可發生加成反應、氧化反應和磺化反應等。與金屬反應時,因硫酸的濃度、反應溫度、金屬種類的不同,可以生成H2、H2S、SO2、S以及金屬硫化物等。硫酸與金屬氧化物生成硫酸鹽。冷的濃硫酸與鐵、鋁不作用。苯與濃硫酸煮沸20~30分鐘生成苯磺酸。醇類一般發生酯化反應,烯丙醇與60%硫酸作用生成烯丙醇硫酸酯。硫酸可以與水以任何比例混合并放出大量的熱量,混合時,只能將酸緩慢倒入水中,切不可把水往酸里加,以防止酸液表面局部過熱引起酸液噴濺。硫酸是無機強酸,腐蝕性強,幾乎能溶解所有的金屬。硫酸具有較強的吸水性和氧化性,能使棉布、紙張、木材等脫水炭化,或使有機物磺化、硫酸化,接觸皮膚會引起嚴重的灼燒。
4.穩定性[16] 穩定
5.禁配物[17] 堿類、強還原劑、易燃或可燃物、電石、高氯酸鹽、雷酸鹽、硝酸鹽、苦味酸鹽、金屬粉末等
6.避免接觸的條件[18] 水
7.聚合危害[19] 不聚合
8.分解產物[20] 氧化硫
貯存方法
儲存注意事項[21] 儲存于陰涼、通風的庫房。保持容器密封。應與易(可)燃物、還原劑、堿類、堿金屬、食用化學品分開存放,切忌混儲。儲區應備有泄漏應急處理設備和合適的收容材料。
合成方法
1.目前國內生產蓄電池硫酸有吹出法、蒸餾法。國外有從硫酸廠發煙硫酸獲取純凈三氧化硫,通人特制的蒸餾水配制的濃度為98%吸收硫酸循環吸收塔,可制得高質量蓄電池硫酸。吹出法將具有一定壓力的干凈空氣直接通人工業硫酸中,將溶解在硫酸中的二氧化硫吹出來,直至合格為止。蒸餾法將工業硫酸加熱蒸發,使液體硫酸變成硫酸蒸氣,通過冷凝器把硫酸蒸氣冷凝,制得蓄電池硫酸成品。硫酸的提純法:在工業濃硫酸中加入約1%(質量分數)的鉻酸酐,澄清后轉入耐高溫玻璃制的蒸餾瓶中,蒸餾瓶包上石棉,以粗玻璃管為冷凝器。在負壓下進行蒸餾,可蒸出80%~85%。向蒸出的酸中緩慢地通入H2S氣體16h,并靜置二天后再重新蒸餾,去掉開頭和最后10%的餾分即可獲取純度較高的硫酸。濃硫酸具有很強的腐蝕性,操作時應采取適當的防護措施。另外從發煙硫酸中蒸出三氧化硫,并使之與蒸餾水反應也可以制得試劑級的硫酸。
2.(1)精餾法 以工業硫酸為原料,經精餾,冷凝、分離、超凈過濾除去雜質,得無色透明的BV1級硫酸。(2)蒸餾法 以工業硫酸為原料,通過蒸餾法純化原料,冷凝分離除去雜質,并經微孔濾膜過濾除去塵埃顆粒,制得無色透明的MOS級和低塵高純級硫酸。
3.由硫、硫化鐵礦、石油精制處理物,以接觸法制取。用作食品添加劑時,限用此法。
4.工業上生產硫酸都以接觸法為主,其主要分為三個階段:焙燒黃鐵礦或硫燃燒制得SO2;在 V 2O5 催化下將 SO2 氧化為SO3;用 9 8 . 3% 的濃H2SO4吸收SO3 得發煙硫酸,加稀酸調整含量為9 8%,即得產品。
5.(1)硫磺法 由硫磺制取二氧化硫氣體,再將二氧化硫催化氧化,生成三氧化硫,最后將三氧化硫與水接觸制取硫酸。(2)硫鐵礦法 硫化鐵礦為原料,經焙燒得到二氧化硫,經凈化,氧化成三氧化硫,用稀硫酸吸收得到成品。
用途
1.為分析和實驗室廣泛使用的試劑。鋇、鍶和鉛的沉淀物,有機物分析及合成中吸收水分,磺化作用,縮合作用與硝酸混合用于硝化作用。MOS級適用于電子工業半導體集成電路生產之用。
2.可用作硬水的軟化劑、離子交換再生劑、pH值調節劑、氧化劑和洗滌劑等。還可用于化肥、農藥、染料、顏料、塑料、化纖、炸藥以及各種硫酸鹽的制造。在石油的煉制、有色金屬的冶煉、鋼鐵的酸洗處理、制革過程以及煉焦業、輕紡業、國防軍工都有廣泛的應用。強酸性清洗腐蝕劑。在集成電路制造工藝中主要用于硅片清洗。
3.硫酸在合成藥物、合成染料、炸藥、石油煉制、金屬冶煉、合成洗滌劑、機械、農藥、化肥等方面都有著廣泛的應用。除作為強的無機酸使用外,還用作脫水劑、氧化劑、助硝化劑、酸洗劑、磺化劑和催化劑等。此外硫酸還可用作高熔點聚酰胺的溶劑,用于紡絲原液的制造。
4.用作強酸性清洗腐蝕劑,可與雙氧水配合使用。
5.用作酸、加工助劑。用于含醇飲料、干酪等。用于由淀粉水解制葡萄糖。或調節水解條件,以制造含25%以上糊精的淀粉糖漿。用2%~4%的硫酸溶液去除柑橘內的果皮以制造柑橘罐頭。精煉食用油時使用濃硫酸(添加約1%)于15~20℃攪拌,使油脂中的有機物脫水炭化后,經水洗除去。啤酒生產中防止CO2的損失。
6.用于生產化學肥料,在化工、醫藥、塑料、染料、石油提煉等工業也有廣泛的應用。[22]
安全信息
危險運輸編碼:UN 1830 8/PG 2
危險品標志: 腐蝕
腐蝕
危險標識:R35
文獻
[1~22]參考書:危險化學品安全技術全書.第一卷/張海峰主編.—2版.北京;化學工業出版社,2007.6 ISBN 978-7-122-00165-8
備注
曾用CAS:7664-93-6
表征圖譜
統計數據
共收錄化學品數據
147579 條




 滬公網安備 31010602001115號
滬公網安備 31010602001115號