硝酸 Nitric acid
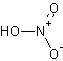
結構式
| 物競編號 | 0JZE |
|---|---|
| 分子式 | HNO3 |
| 分子量 | 63.01 |
| 標簽 | 硝鏹水, 氫氮水, 濃硝酸, 稀硝酸, 硝鏹水, 白霧硝酸, Aquafortis, 聚合物溶劑, 硝化劑, 氧化劑 |
編號系統
CAS號:7697-37-2
MDL號:MFCD00011349
EINECS號:231-714-2
RTECS號:QU5775000
BRN號:暫無
PubChem號:24855630
物性數據
1.性狀:純品為無色透明發煙液體,有酸味。[1]
2.熔點(℃):-42(無水)[2]
3.沸點(℃):83(無水)[3]
4.相對密度(水=1):1.50(無水)[4]
5.相對蒸氣密度(空氣=1):2~3[5]
6.飽和蒸氣壓(kPa):6.4(20℃)[6]
7.臨界壓力(MPa):6.89[7]
8.辛醇/水分配系數:0.21[8]
9.溶解性:與水混溶,溶于乙醚。[9]
10.黏度(mPa·s,20oC):0.89
11.比熱容(KJ/(kg·K),98.15%):1.99
12.比熱容(KJ/(kg·K),90.33%):2.22
13.比熱容(KJ/(kg·K),70.00%):2.56
14.比熱容(KJ/(kg·K),40.00%):2.80
15.電導率(S/m,30.42%):7008
16.電導率(S/m,51.78%):5554.2
17.電導率(S/m,78.96%):1945.1
18.電導率(S/m,98.50%):167.8
19.生成熱(KJ/mol,H.N.30):173.79
20.生成熱(KJ/mol,H.NO.20):264.12
21.生成熱(KJ/mol,NO2.O.H):182.21
毒理學數據
1.急性毒性[10] LC50:130mg/m3(大鼠吸入,4h);67ppm(小鼠吸入,4h)
2.刺激性 暫無資料
生態學數據
1.生態毒性 暫無資料
2.生物降解性 暫無資料
3.非生物降解性 暫無資料
4.其他有害作用[11] 該物質對環境有危害,應特別注意對水體和土壤的污染。
分子結構數據
1、摩爾折射率:9.60
2、摩爾體積(cm3/mol):38.8
3、等張比容(90.2K):107.4
4、表面張力(dyne/cm):58.6
5、極化率(10-24cm3):3.80
計算化學數據
暫無
性質與穩定性
1.化學性質:硝酸為強酸,遇光及空氣部分發生分解。加熱時分解生成一氧化氮和氧氣。稀硝酸比較穩定,70%~90%硝酸在0℃,陰暗處不發生分解。濃硝酸氧化性強,標準氧化電位。
2.硫、磷經硝酸氧化可生成硫酸和磷酸。能溶解多種金屬形成硝酸鹽溶液。鐵、鉻、鋁等金屬在濃硝酸中處于鈍態而不作用,但可溶于稀硝酸中。錫、銻、鉬等生成不溶性氧化物,金、鉑等不發生反應。硝酸能與多種有機化合物發生硝化或氧化反應,生成硝基化合物或氧化產物。
3.穩定性[12] 穩定
4.禁配物[13] 還原劑、堿類、醇類、堿金屬、銅、胺類、金屬粉末、電石、硫化氫、松節油、可燃物如糖、纖維素、木屑、棉花、稻草或廢紗頭等
5.聚合危害[14] 不聚合
6.分解產物[15] 氮氧化物
貯存方法
儲存注意事項[16] 儲存于陰涼、通風的庫房。遠離火種、熱源。庫溫不超過30℃,相對濕度不超過80%。保持容器密封。應與還原劑、堿類、醇類、堿金屬等分開存放,切忌混儲。儲區應備有泄漏應急處理設備和合適的收容材料。
合成方法
按稀硝酸和濃硝酸分述如下。
(一)稀硝酸
工業上制取稀硝酸的方法有常壓法、綜合法、中壓法和GP雙加壓法。
常壓法是氨一空氣混合氣在常壓下氧化成氮氧化物,氮氧化物在常壓下經多級填料吸收塔進行水吸收,以制得稀硝酸。其尾氣經堿吸收后排放。
綜合法足凈化后的氨-空氣混合氣經鼓風機升壓,預熱后通過紙板過濾器進入氧化爐,氧化成一氧化氮。氣體進人冷卻洗滌器,進入氧化塔進行一氧化氮氧化,隨即進入酸吸收塔,由塔頂加入水進行吸收生成稀硝酸。由塔底部流出的硝酸進入漂白塔,制得稀硝酸成品。
中壓法是采用蒸汽透平與尾氣膨脹壓縮機直接驅動空氣透平壓縮機。經漂白塔、氧化塔、吸收塔制得稀硝酸成品。
GP雙加壓法是采用兩臺氧化爐并聯操作。生成的氣體再經冷凝吸收,制得稀硝酸產品。
稀硝酸生產其
4NH3+5O2→4NO+6H2O
2NO+O2→2NO2
3NO2+H2O→2HNO3+NO
(二)濃硝酸
工業上制取濃硝酸的方法有間接法、直接法(見發煙硝酸)和超共沸酸的蒸餾法。間接法是先制得稀硝酸,然后稀硝酸在脫水劑存在的情況下,經提純、精餾、冷凝、漂白等工序制得濃硝酸,作為脫水劑的有硝酸鎂和濃硫酸等。超共沸酸蒸餾法包括氨的氧化、超共沸酸的制取和直接蒸餾等步驟。
精制方法:硝酸中所含雜質大多為氮的氧化物。精制時添加少量硝酸鉀進行蒸餾即可除去。
以工業硝酸為原料,經精餾、冷凝分離除去雜質后,再經微孔膜過濾去除雜質,得到無色透明的電子級硝酸。
(三)制法 將發煙硝酸用電導水稀釋到90%左右。加熱蒸餾,首先蒸出的是濃硝酸,棄去前段餾分(約總量10%),沸點逐升至120.5℃,達到恒沸點,此時蒸出的硝酸含量68.5%,為保證試劑質量,要留有一定量殘液。根據所需硝酸的濃度要求,可加適量水稀釋。初餾物和殘液可作為原料反復使用。用壓縮空氣將溶在硝酸溶液中的少量NO2吹出,可得無色透明溶液。要除去氯離子,可在蒸餾前加入硝酸銀,直到不再有氯化銀沉淀生成為止,并在30~40℃下靜置澄清,采用虹吸將清液移至蒸餾器中,可根據氯離子含量,來確定硝酸銀用量(一般過量20%左右)。
(四)硝酸制備一般采用氨氧化法:以鉑為催化劑,將氨氧化為一氧化氮,再用空氣與濃硝酸全部氧化為二氧化氮,然后用濃硝酸吸收,生成發煙硝酸,再經過解吸而得。或由氨氧化生成一氧化氮,再與空氣中的氧作用生成二氧化氮,用水吸收得到稀硝酸。
用途
1.用途極廣的重要化工原料,主要用于制造硝酸銨、硝酸銨鈣、硝酸磷肥、氮磷鉀等復合肥料。有機工業用于制造四硝基甲烷、硝基己烷、l-硝基丙烷、2,4-二硝基苯氧乙醇等硝基化合物。染料工業用于對硝基苯甲醚、4,4’-二硝基二苯醚、對硝基苯酚、2,5-二氯硝基苯等染料中間體的合成。涂料工業用于制造硝基清漆和硝基瓷漆。醫藥工業用于制造硝基苯乙酮。硝酸作為氧化劑可氧化醇、苯胺及其他化學品。并已經用于火箭的推進劑。硝酸也是制造鈣、銅、銀、鈷和鍶等的硝酸鹽的原料。
2.硝酸屬于強氧化性酸,對大多數金屬有腐蝕作用。高濃度硝酸對金屬有鈍化作用。硝酸用于清洗碳素鋼、不銹鋼、銅、黃銅、碳素鋼不銹鋼組成的設備,可除去水垢、鐵銹,對 α-Fe2O3和磁性Fe3O4有良好的溶解力。 在生物法污水處理過程中,可用作微生物養分中的氮源等。此外,硝酸廣泛用于化肥、化纖、醫藥、染料、橡膠等的制造,在國防工業、冶金工業、印染工業以及其他工業部門中,也是不可缺少的重要的分析化學試劑。
3.硝酸是最重要的基本化工原料之一,是一種用途極廣的化工產品。在水處理領域,硝酸可用作碳素鋼、不銹鋼設備的清洗除銹劑,用在污水、廢水的氧化還原處理過程中;在污水的生物法處理過程中,可用作微生物養分中的氮源等。
4.用作蝕刻劑及強酸性清洗腐蝕劑,可與冰醋酸、雙氧水等配合使用。
5.用作分析試劑,如作溶劑,氧化劑。還用于有機合成,制取各類硝基化合物。
6.用途極廣,主要用于化肥、染料、國防、炸藥、冶金、醫藥等工業。[17]
安全信息
危險運輸編碼:UN 2031 8/PG 1
危險品標志: 氧化劑
氧化劑  腐蝕
腐蝕
文獻
[1~17]參考書:危險化學品安全技術全書.第一卷/張海峰主編.—2版.北京;化學工業出版社,2007.6 ISBN 978-7-122-00165-8
備注
暫無
表征圖譜
統計數據
共收錄化學品數據
147579 條




 滬公網安備 31010602001115號
滬公網安備 31010602001115號