氯化亞砜 Thionyl chloride
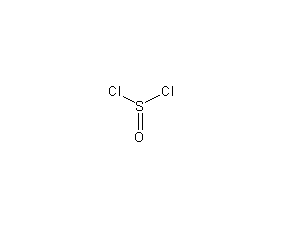
結構式
| 物競編號 | 0JZX |
|---|---|
| 分子式 | SOCl2 |
| 分子量 | 118.98 |
| 標簽 | 亞硫酰(二)氯, 亞硫酰氯, 氯化亞砜, 二氯氧硫, 氯化亞硫酰, 亞硫酰二氯, SOCl2, Sulfinyl chloride, Sulfinyl dichloride, 氯化劑, 脫水劑, 氧化劑, 催化劑 |
編號系統
CAS號:7719-09-7
MDL號:MFCD00011449
EINECS號:231-748-8
RTECS號:XM5150000
BRN號:1209273
PubChem號:暫無
物性數據
1.性狀:淡黃色至紅色、發煙液體,有強烈刺激氣味。[11]
2.熔點(℃):-105[12]
3.沸點(℃):76~79[13]
4.相對密度(水=1):1.64[14]
5.相對蒸氣密度(空氣=1):4.1[15]
6.飽和蒸氣壓(kPa):13.3(21.4℃)[16]
7.臨界壓力(MPa):4.43[17]
8.辛醇/水分配系數:0.92[18]
9.溶解性:可混溶于苯、氯仿、四氯化碳等。[19]
10.黏度(mPa·s,0oC):0.80
11.黏度(mPa·s,38oC):0.545
12.蒸發熱(KJ/mol):31.32
13.生成熱(KJ/mol):206.0
14.電導率(S/m):2×10-6
15.蒸氣壓(kPa,20oC):13.3
16.蒸氣壓(kPa,50oC):42.9
17.蒸氣壓(kPa,70oC):85.0
18.蒸氣壓(kPa,75oC):99.5
19.體膨脹系數(K-1):0.0010
毒理學數據
1、本品有毒,其蒸氣刺激眼睛和黏膜,液體觸及皮膚能引起燒傷。
2、毒性比二氧化硫大,蒸氣對呼吸道和眼結膜有明顯的刺激作用。皮膚接觸引起灼傷。工作場所最高容許濃度24.15mg/m3(空氣中)。貓吸入85mg/m3濃度的亞硫酰(二)氯蒸氣,20分鐘可引起死亡。
3.急性毒性[20] LC50:2435mg/m3(大鼠吸入)
生態學數據
對水是稍微危害的,若無政府許可,勿將材料排入周圍環境。
分子結構數據
1、摩爾折射率:20.60
2、摩爾體積(cm3/mol):60.8
3、等張比容(90.2K):179.9
4、表面張力(dyne/cm):76.7
5、極化率(10-24cm3):8.17
計算化學數據
1、疏水參數計算參考值(XlogP):1.5
2、氫鍵供體數量:0
3、氫鍵受體數量:1
4、可旋轉化學鍵數量:0
5、互變異構體數量:
6、拓撲分子極性表面積(TPSA):17.1
7、重原子數量:4
8、表面電荷:0
9、復雜度:29
10、同位素原子數量:0
11、確定原子立構中心數量:0
12、不確定原子立構中心數量:0
13、確定化學鍵立構中心數量:0
14、不確定化學鍵立構中心數量:0
15、共價鍵單元數量:1
性質與穩定性
1.遇水易分解為二氧化硫和氯化氫。溶于苯、氯仿和四氯化碳中。加熱至140℃開始分解生成氯氣、二氧化硫和一氯化硫。其氯原子取代羥基或巰基能力顯著,有時可以取代二氧化硫、氫或氧。氯化亞砜能與有羥基的酚或醇有機化合物反應生成相應的氯化物,與磺酸反應生成磺酰氯,與格利雅試劑反應生成相應的亞砜化合物。折光能力很強,有如SO2一樣令人不愉快的氣味。二氯亞砜在稍高于沸點的溫度下會發生明顯的分解,分解產物為S2Cl2,SO2和Cl2。可溶于苯和三氯甲烷,與水反應生成SO2和HCl。
2.非常活潑,具有強腐蝕性,其蒸氣和液體對眼睛、黏膜和皮膚有強烈的刺激作用。操作時應戴防護手套,避免皮膚接觸。氯化亞砜須在玻璃瓶內于室溫下干燥環境中儲存。它與水反應放出有毒氣體HCl和SO2,由于SOCl2參與的大部分反應都會放出以上兩種氣體,所以必須在通風櫥中進行操作。SOCl2在高于140 oC時會分解生成Cl2、SO2和S2Cl2,鐵和/或鋅的雜質會催化加劇該分解反應。
3.穩定性[21] 穩定
4.禁配物[22] 水、堿類
5.避免接觸的條件[23] 受熱、潮濕空氣
6.聚合危害[24] 不聚合
貯存方法
儲存注意事項[25] 儲存于陰涼、通風的庫房。庫溫不超過30℃,相對濕度不超過75%。保持容器密封。應與堿類等分開存放,切忌混儲。儲區應備有泄漏應急處理設備和合適的收容材料。
合成方法
1.氯磺酸法 先將硫黃粉加入反應器中,通入氯氣進行反應生成一氯化硫。再將一定量的氯磺酸和一氯化硫加入反應器內,在50℃以下通入氯氣進行反應,反應好的物料經粗餾、冷凝,收集130℃以下的料液送至精餾鍋,為了使低沸點的二氯化硫轉變成一氯化硫留在鍋內,則要加入粗品數量的15%~20%硫黃,然后送去精餾,經回流4h,色澤正常后,收集氣相75~80℃的餾分,制得亞硫酰氯成品。其反應方程式如下:
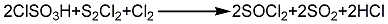
2.二氧化硫法 以硫黃、液氯和液體二氧化硫為原料,采用全循環和液相循環法,生產高純度氯化亞砜礬,純度99%以上,該方法工藝先進,產品質量穩定,“三廢”排放少。

圖XVI-4 制備SOCL2的制備
二氯亞砜也叫亞硫酰二氯或氯化亞硫酰。
圖制備SOCl2的裝置
1—燒瓶1;2—燒瓶2;3—密封磨口
(1).在如圖所示的燒瓶1中加入純凈的發煙硫酸,在燒瓶2中加入SCl2。慢慢加熱燒瓶1,并用冰水冷卻燒瓶2,SO3進入SCl2中即開始發生反應,放出的SO2通過通風柜排出。當反應完成后將1拆除并密封磨口3,在隔絕濕氣的條件下慢慢進行蒸餾。然后在中間餾分中加入硫,仔細地分餾數次。獲取76~77℃完全無色的餾分為最后產品。
(2).用一裝有回流冷凝管的250mL雙口燒瓶作反應器,反應器經徹底干燥后放入100g PCl5。冷凝管的上端聯接一支CaCl2干燥管,在反應器的另一口中插入一根導氣管至瓶底。從導氣管中通入經仔細干燥過的SO2氣體,搖蕩反應瓶以加速反應進行。數小時后,PCl5全部溶解,反應即完成。用高效能的分餾柱仔細分餾產物數次,可得SOCl2產品。
精制方法:工業品的亞硫酸(二)氯中常含有硫酰氯、一氯化硫和二氯化硫等雜質,一般重蒸一次即可使用,但仍帶有黃色。若需高純度的產品,可將450mL亞硫酰(二)氯與12.5g硫加熱回流4.5小時,然后用高效分餾柱分餾兩次可得無色純品。也可在亞磷酸三苯酯存在下進行蒸餾精制。
3.在干燥的五氯化磷中通入干燥的二氧化硫氣體,在攪拌下邊回流邊反應,反應放出的熱量將五氯化磷熔融:
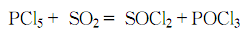
待五氯化磷完全熔融后,加熱混合物并攪拌均勻。然后精餾混合物數次,收集77~80℃餾分,即得試劑氯化亞砜。
用途
1.用作有機合成的氯化劑,如醇類羥基的氯化、羧酸的氯化、酸酐的氯化、有機磺酸或硝基化合物的氯置換。制造酰基氯化物。制造醫藥中間體,例如驅蟲凈、無味合霉素。還用作脫水劑和溶劑。
2.用作有機合成中的氯化劑和氧化劑,如制備酰基氯,有機酸酐等。也用作催化劑。
3.氯化劑。制氯烷、酰氯,磺酰氯,環狀酸酐。由酰胺制腈,甲酰胺制異腈。制氨基酸腈、吡啶4一磺酸。合成雜環,芳亞砜脫氧,等等。
4.氯化亞砜是一種常用的氯代試劑[1,2],其反應性能主要受反應物投料比、溶劑、堿等條件影響。此外它還是常用的脫水試劑,用于催化分子內脫水等消除反應。由于氯化亞砜易分解的性質,它還可以用作電解質溶液,例如:AlCl3/SOCl2的介質溶液[3]。
氯磺酸酯或鹵代烴的合成 氯化亞砜能與一級、二級和三級醇反應生成特定的氯磺酸酯(等當量反應)。產物的種類決定于反應條件,尤其是反應物的化學計量數、溶劑和使用的堿。如果2當量的醇在吡啶作用下與氯化亞砜反應,將生成亞硫酸二酯。若亞硫酰氯過量,或氯磺酸酯與氯化亞砜反應,將生成相應的鹵代烴,并伴隨生成HCl和SO2。因此直接將醇與氯化亞砜在堿作用下反應,是將醇轉化為鹵代烴的有效的方法之一 (式1)[4]。但是對于不飽和烴α-位取代的醇,由于烯醇式中間體的存在,常發生雙鍵上的氯代反應 (式2)[5]。

酰氯的制備 氯化亞砜還廣泛應用于制備酰氯。將羧酸或羧酸酐與SOCl2反應(惰性溶劑或直接以SOCl2為溶劑),可得到相應的酰氯,同時生成HCl和SO2 (式3)[6]。得到的酰氯可繼續與氨基反應得到酰胺,該方法通常可以合并為一步反應 (式4)[7]。

芳香醛或α,β-不飽和醛以及它們的亞硫酸鹽衍生物可與氯化亞砜反應。例如:丙烯醛、苯甲醛等的羰基可與氯化亞砜發生加成反應,生成相應的二氯代物和SO2。
脫水反應 目前,氯化亞砜最主要的應用還是作為脫水劑使用。特別是在大分子合成領域中,氯化亞砜被廣泛應用于分子內關環 (式5)[8] 等一系列反應。
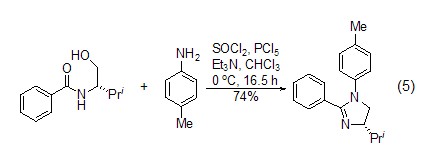
S-N鍵的生成 可與氨基反應構建S-N鍵,這一性質常被用于雜原子的成環反應 (式6)[9]。
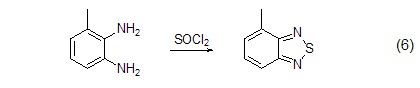
C-H鍵的氧化 氯化亞砜還可以氧化比較活潑的C-H鍵,生成氯代物或亞氯硫代物 (式7)[10],且反應條件通常比較溫和。值得注意的是,此類反應往往很容易發生逆反應,還原成原來的C-H鍵化合物。
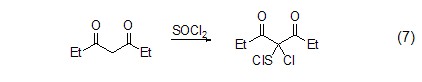
5.用于有機合成,農藥及醫藥工業。[26]
安全信息
危險運輸編碼:UN 1836 8/PG 1
危險品標志: 腐蝕
腐蝕
安全標識:S26 S45 S36/S37/S39
文獻
1. Feng, S.; Panetta, C. A.; Graves, D. E. J. Org. Chem., 2001, 66, 612. 2. Amaresh, R. R.; Lakshmikantham, M. V.; Baldwin, J. W.; Cava, M. P.; Metzger, R. M.; Rogers, R. D. J. Org. Chem., 2002, 67, 2453. 3. Boyle, T. J.; Andrews, N. L.; Alam, T. M.; Tallant, D. R.; Rodriguez, M. A.; Ingersoll, D. Inorg. Chem., 2005, 44, 5934. 4. Amato, J. S.; Chung, J. Y. L.; Cvetovich, R. J.; Gong, X.; McLaughlin, M.; Reamer, R. A. J. Org. Chem., 2005, 70, 1930. 5. Krafft, M. E.; Haxell, T. F. N. J. Am. Chem. Soc., 2005, 127, 10168. 6. Alagic, A.; Koprianiuk, A.; Kluger, R. J. Am. Chem. Soc., 2005, 127, 8036. 7. Mishani, E.; Abourbeh, G.; Jacobson, O.; Dissoki, S.; Daniel, R. B.; Rozen, Y.; Shaul, M.; Levitzki, A. J. Med. Chem., 2005, 48, 5337. 8. Boland, N. A.; Casey, M.; Hynes, S. J.; Matthews, J. W.; Smyth, M. P. J. Org. Chem., 2002, 67, 3919. 9. Jorgensen, M.; Krebs, F. C. J. Org. Chem., 2005, 70, 6004. 10. Hawata, M. A. M.; El-Torgoman, A. M.; El-Kousy, S. M.; Ismail, A. E.-H.; Madsen, J. O.; I. S?tofte, Senning, A. Eur. J. Org. Chem., 2002, 2039. [1~10]參考書:現代有機合成試劑<性質、制備和反應>;胡躍飛 付華 編著;化學工業出版社;ISBN 7-5025-8542-7 [11~26]參考書:危險化學品安全技術全書.第一卷/張海峰主編.—2版.北京;化學工業出版社,2007.6 ISBN 978-7-122-00165-8
備注
暫無
表征圖譜
統計數據
共收錄化學品數據
147579 條




 滬公網安備 31010602001115號
滬公網安備 31010602001115號