草酰氯 Oxalyl dichloride
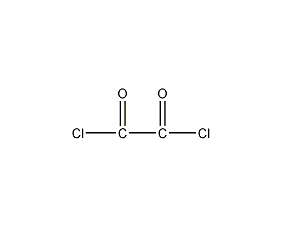
結構式
| 物競編號 | 01PT |
|---|---|
| 分子式 | C2Cl2O2 |
| 分子量 | 126.92 |
| 標簽 | 乙二酰氯, Ethanedioyl dichlorid |
編號系統
CAS號:79-37-8
MDL號:MFCD00000704
EINECS號:201-200-2
RTECS號:KI2950000
BRN號:1361988
PubChem號:24853204
物性數據
1. 性狀:無色發煙液體
2. 相對密度:1.488
3. 相對蒸汽密度(g/mL,空氣=1):不確定
4. 熔點(oC):-12
5. 沸點(oC,常壓):63-64
6. 沸點(oC,5.2kPa):不確定
7. 折射率:1.4340(13℃)
8. 閃點(oC):不確定
9. 比旋光度(o):不確定
10. 自燃點或引燃溫度(oC):不確定
11. 蒸氣壓(kPa,25oC):不確定
12. 飽和蒸氣壓(kPa,60oC):不確定
13. 燃燒熱(KJ/mol):不確定
14. 臨界溫度(oC):不確定
15. 臨界壓力(KPa):不確定
16. 油水(辛醇/水)分配系數的對數值:不確定
17. 爆炸上限(%,V/V):不確定
18. 爆炸下限(%,V/V):不確定
19. 溶解性:溶于乙醚,遇水及醇能劇烈分解。加熱至約600℃即分解并逸出一氧化碳。溶于正己烷、苯、乙醚、乙腈和鹵代溶劑如二氯甲烷、氯仿。
毒理學數據
1、急性毒性 大鼠吸入LC50:1840ppm/4H
生態學數據
暫無
分子結構數據
1、 摩爾折射率:21.07
2、 摩爾體積(cm3/mol):78.5
3、 等張比容(90.2K):198.7
4、 表面張力(dyne/cm):40.9
5、 極化率(10-24cm3):8.35
計算化學數據
1.疏水參數計算參考值(XlogP):1.7
2.氫鍵供體數量:0
3.氫鍵受體數量:2
4.可旋轉化學鍵數量:1
5.互變異構體數量:無
6.拓撲分子極性表面積34.1
7.重原子數量:6
8.表面電荷:0
9.復雜度:75.5
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:1
性質與穩定性
1.草酰氯不僅對空氣敏感,遇到潮氣會發生分解放出氯化氫,而且有一種不愉快的味道。
2.草酰氯具有高毒性和腐蝕性,能嚴重刺激眼睛、皮膚和呼吸道。盛放草酰氯的試劑瓶必須在陰涼、干燥的環境下保存,并嚴格密封,嚴禁與濕氣接觸。草酰氯與水能劇烈反應,放出毒性氣體CO、CO2和HCl。
貯存方法
本品應密封于陰涼避光處保存。
合成方法
將無水草酸與五氯化磷混勻后,慢慢加熱至64℃左右,反應至無氯化氫止。將粗品精餾后即得草酰氯。
用途
1.用于合成苯甲酰脲類殺蟲劑氟鈴脲、殺鈴脲等的中間體,也是磺酰脲類除草劑甲磺隆、芐嘧磺隆、吡嘧磺隆等的中間體。
2.草酰氯是一個應用廣泛的制備碳酰氯、磷酰二氯、氯代烷烴以及酰基異氰的酰化試劑。
草酰氯是一個非常有效的酰化試劑,能廣泛用于制備酰基疊氮化物、溴代烯烴、碳酰胺、鄰二氮萘、偶氮酮、內酯,以及實現乙烯酮的環加成反應,分子內Fridel-Crafts酰化反應。
與亞硫酰氯相似,草酰氯與酸作用會給出氣體副產物,生成的氯化物能很容易分離出來 (式1)[1]。
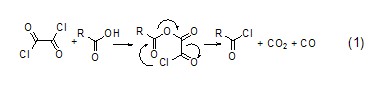
草酰氯與羧酸根離子的作用機理包括親核取代、分子內電荷轉移,從而形成相應的酰氯產物。通過調整草酰氯與羧酸根離子的比例還可以得到酸酐化合物 (式2)[2]。
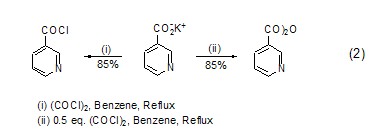
草酰氯與金屬有機化合物如格氏試劑,烷基鋰作用生成鄰二羰基化合物 (式3)[3]。草酰氯與鋯雜環戊二烯在CuCl的作用下生成環戊二烯酮衍生物 (式4)[4]。
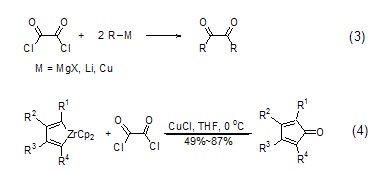
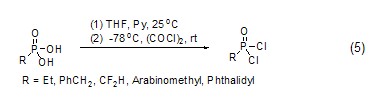
草酰氯能用于制備磷酰氯衍生物,如磷酸在草酰氯和吡啶作用下在低溫能高產率地轉換為相應的磷酰氯 (式5)[5]。
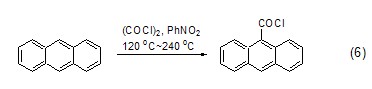
草酰氯還能直接為烷烴或環烷烴化合物引入氯羰基團,不過通常反應得到的是混合物。芳香烴化合物在草酰氯和路易斯酸作用下也能發生氯羰基化反應,其中,蒽在沒有催化劑存在下也能直接發生反應 (式6)[6]。
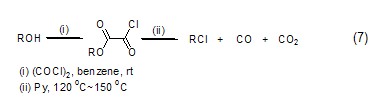
醇類化合物與草酰氯反應能得到乙二酰單烷基酯,進而在加熱條件下轉變為氯代烷烴化合物 (式7)[7]。
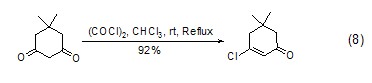
草酰氯與于1,3-二酮反應,能高產率地生成β-氯烯烴環化物 (式8)[8]。
安全信息
危險運輸編碼:UN 2922 8/PG 1
危險品標志: 腐蝕
腐蝕
安全標識:S26 S43 S45 S36/S37/S39
文獻
1. (a) Adams, R; Ulich, L. H. J. Am. Chem. Soc., 1920, 42, 599. (b) Paquette, L. A.; Dahnke, K.; Doyon, J.; He, W.; Wyant, K.; Friendrich, D. J. Org. Chem., 1991, 56, 6199. 2. (a) Wingfield, H. N.; Harlan, W. R.; Hanmer, H. R. J. Am. Chem. Soc., 1953, 75, 4364. (b) Schrecker, A. W.; Haury, P. B. J. Am. Chem. Soc., 1954, 76, 5803. 3. (a) Larock, R. C. In Comprehensive Organic Transformations; VCH: New York, 1989. (b) O’Niel, B. T. In Comprehensive Organic Synthesis, 1991, Vol. 1; 397. (c) Shirley, D. A. Org. React., 1954, 8, 28. (d) Jorgenson, M. J. Org. React., 1970, 18, 1. (e) Faust, R.; Weber, C.; Fiandanese, V.; Marchese, G.; Punzi, A. Tetrahedron, 1997, 53, 14655. (f) Faust, R.; Weber, C. J. Org. Chem., 1999, 64, 2571. 4. Chen, C.; Xi, C.; Jiang, Y.; Hong, X. J. Am. Chem. Soc., 2005, 127, 8024. 5. Stowell, M. H. B.; Ueland, J. M.; McClard, R. W. Tetrahedron Lett., 1990, 31, 3261. 6. Latham, H. G.; May, E. L.; Mosettig, E. J. Am. Chem. Soc., 1984, 70, 1079. 7. Rhoads, S. J.; Michel, R. E. J. Am. Chem. Soc., 1963, 85, 585. 8. (a) Clark, R. D.; Heathcock, C. H.; J. Org. Chem., 1976, 41, 636. (b) Buchi, G.; Carlson, J. A. J. Am. Chem. Soc., 1969, 91, 6470. 9.參考書:現代有機合成試劑<性質、制備和反應>;胡躍飛 付華 編著;化學工業出版社;ISBN 7-5025-8542-7
備注
暫無
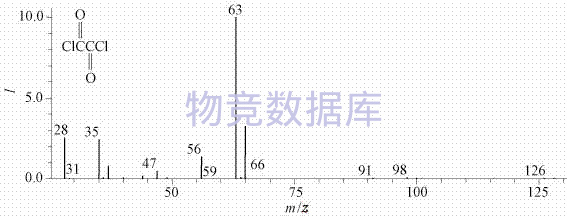
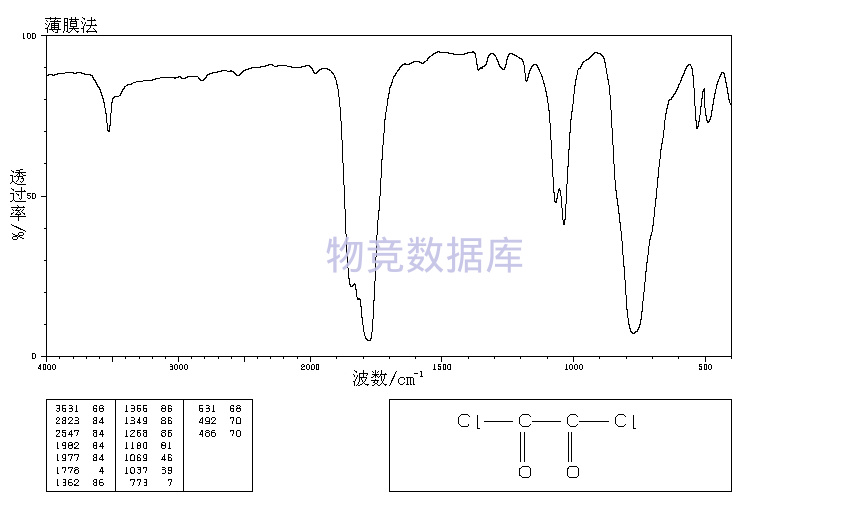
表征圖譜
統計數據
共收錄化學品數據
147579 條



 滬公網安備 31010602001115號
滬公網安備 31010602001115號