α-氫氧化鐵 Iron(III) hydroxide, alpha
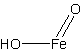
結構式
| 物競編號 | 0PH2 |
|---|---|
| 分子式 | FeH3O3 |
| 分子量 | 88.85 |
| 標簽 | Ferric oxide hydroxide, Iron hydroxide oxide, Iron(III) oxide Hydrate |
編號系統
CAS號:20344-49-4
MDL號:MFCD00064782
EINECS號:243-746-4
RTECS號:暫無
BRN號:暫無
PubChem號:24863095
物性數據
1. 性狀:無氣味棕色粉末
2. 密度(g/mL,25/4℃):4.03
3. 相對蒸汽密度(g/mL,空氣=1):未確定
4. 熔點(oC):未確定
5. 沸點(oC,常壓):未確定
6. 沸點(oC,5.2kPa): 未確定
7. 折射率: 2.3
8. 閃點(oC): 未確定
9. 比旋光度(o): 未確定
10. 自燃點或引燃溫度(oC): 未確定
11. 蒸氣壓(kPa,25oC): 未確定
12. 飽和蒸氣壓(kPa,60oC): 未確定
13. 燃燒熱(KJ/mol):未確定
14. 臨界溫度(oC): 未確定
15. 臨界壓力(KPa): 未確定
16. 油水(辛醇/水)分配系數的對數值: 未確定
17. 爆炸上限(%,V/V):未確定
18. 爆炸下限(%,V/V): 未確定
19. 溶解性:未確定
毒理學數據
暫無
生態學數據
暫無
分子結構數據
暫無
計算化學數據
1.疏水參數計算參考值(XlogP):無
2.氫鍵供體數量:1
3.氫鍵受體數量:2
4.可旋轉化學鍵數量:0
5.互變異構體數量:無
6.拓撲分子極性表面積37.3
7.重原子數量:3
8.表面電荷:0
9.復雜度:10.3
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:1
性質與穩定性
避免接觸酸
貯存方法
放入緊密的貯藏器內,儲存在陰涼,干燥的地方
合成方法
1.氧化鐵黃主要是采用硫酸亞鐵氧化法生產,可直接用硫酸亞鐵溶液,也可用鐵屑與硫酸制備硫酸亞鐵,再加入苛性鈉溶液和空氣制得晶種、晶種成長、加熱氧化、過濾、洗滌、干燥并粉碎而成,也可采用苯胺法生產。也可用空氣使金屬鐵氧化而得。
2.在大約30℃溫度下,將3L 0.5mol/L的氫氧化鈉水溶液加入到5L 0.2mol/L的硫酸亞鐵水溶液中,得到氫氧化亞鐵。以較快的速度向其中輸送空氣,鼓泡2~3h,氧化之后生成極細小α-FeO(OH)晶種。將此晶種和鐵屑、硫酸亞鐵水溶液一起裝到主反應槽,在40~60℃加熱的條件下,慢慢通入空氣。硫酸亞鐵氧化的同時水解,形成α-FeO(OH)的晶種。另一方面,同時生成的硫酸和鐵屑反應,補充硫酸亞鐵。數小時到十幾小時之后,當α-FeO(OH)達到所需的大小時停止反應。
3.制造時如不考慮粒徑分布和粒子大小等問題,可向01mol/L硝酸鐵加氫氧化鉀作沉淀劑,稍過量一些,可以加熱到室溫至50℃之間,放置一晝夜。茶褐色無定形沉淀逐漸變為黃色α-FeO(OH)。α-FeO(OH)作為黃色顏料或者作為磁帶錄音用針狀四氧化三鐵和γ-Fe2O3的起始原料時,主要是按照制法(Ⅰ)進行工業生產。在280℃左右脫水則變為α-Fe2O3。這時,仍保留針狀外形。β-FeO(OH)
4.β-FeO(OH)可由三氯化鐵水解制得。將0.1mol/L三氯化鐵水溶液的pH值調整到2左右,盡可能慢慢地加熱(每小時升溫10℃左右),在80℃保溫2h之后,在室溫下放置一晝夜。先用含有少量氨的水,再用蒸餾水洗滌之后,進行離心分離,在50℃下干燥。100g FeCl3·6H2O可得大約35g β-FeO(OH)。在組成中多多少少含有一些Cl-。γ-FeO(OH)
5.在Fe2+水溶液里,加入化學計算以下的堿金屬氫氧化物,在溶解少量PO3-4的條件下進行空氣氧化,經過被稱為綠銹的綠色沉淀生成過程,得到γ-FeO(OH)。在堿過量的狀態下,即使將CdI2型Fe(OH)2沉淀氧化,也得不到γ-FeO(OH)。另外,在溶解少量PO3-4時,可以抑制雜質α-FeO(OH)的生成,有可能生成只含γ-FeO(OH)的純品。不加PO3-4時,幾乎毫無例外,氧化生成物都是γ-相和α-相混合物。
將20.5g FeSO4·7H2O溶于1L水中,加5g氫氧化鈉,再用少量氫氧化鈉溶液將pH調節為5.0。相當于Na+和Fe2+的混合比(2Na+/Fe2+)約為085。再加1.3g Na2HPO4,待完全溶解后,加熱到40℃,通入空氣進行氧化。沉淀一旦經過深銅綠色就變為黃色的細小針狀γ-FeO(OH)。為使粒子進一步成長,追加約30g FeSO4·7H2O,再加入70g網狀金屬鐵,加熱到60℃,鼓入空氣,約20h后停止反應。粒子在這個過程中成長約1μm長。將沉淀分離,在50℃左右干燥。
6.取500mL吡啶,通二氧化碳并使其沸騰趕除氧氣,冷卻后再通入二氧化碳,在攪拌下慢慢加入125mL氯化亞鐵水溶液,反應結束后靜置一夜,將析出的氯化四吡啶合鐵(Ⅱ)結晶過濾,用吡啶洗滌干燥。用蒸餾水按20g/L比例使其溶解。在最初15min稍強一些,以后就慢慢地送入凈化的空氣直至氧化完了為止。充分洗滌沉淀,在50℃下干燥。利用此法大體上可以得到05~1μm長的針狀結晶。γFeO(OH)在250~300℃脫水,生成γ-Fe2O3。δ-FeO(OH)。δ-FeO(OH)是將氫氧化亞鐵沉淀在30℃溫度以下用過氧化氫溶液迅速氧化制得的。
7.將50mL 1.6mol/L硫酸亞鐵水溶液在攪拌下慢慢加到約400mL 10mol/L氫氧化鈉水溶液里。反應放出的熱量用流動水冷卻保持20℃左右。氫氧化亞鐵在濃度為10~8mol/L濃度范圍內的氫氧化鈉水溶液里析出。將10mL 10%過氧化氫溶液在攪拌下快速加入(溫度上升到30~35℃)。繼續攪拌,在確證溶液底部白色沉淀完全被氧化之后放置一段時間,使沉淀沉降,首先用傾瀉法再經抽吸過濾之后充分水洗,在50℃以下干燥。這樣制得的δ-FeO(OH)粒子,保持著母體結晶氫氧化亞鐵的粒子形態為六角板狀,它的平均粒徑可達0.1μm。用氫氧化鈉作沉淀劑是適宜的。另外,初始氫氧化鈉濃度越小,析出的氫氧化亞鐵進而使δ-FeO(OH)粒子的尺寸也越小。
δ-FeO(OH)在室溫下雖顯強磁性,加熱到75℃以上時,磁性逐漸減弱。大約200℃轉變為α-FeO(OH),大約300℃時則分解為α-Fe2O3。
用途
主要用于涂料、水泥制件、建筑表面、塑料、橡膠的著色
安全信息
危險運輸編碼:暫無
危險品標志:暫無
安全標識:暫無
危險標識:暫無
文獻
暫無
備注
暫無
表征圖譜
統計數據
共收錄化學品數據
147579 條




 滬公網安備 31010602001115號
滬公網安備 31010602001115號