碘化鋅 Zinc iodide
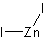
結構式
| 物競編號 | 0KSN |
|---|---|
| 分子式 | ZnI2 |
| 分子量 | 319.22 |
| 標簽 | Hydriodic acid zinc salt (2:1), 高純度化合物, 消毒劑, 收斂劑 |
編號系統
CAS號:10139-47-6
MDL號:MFCD00011299
EINECS號:233-396-0
RTECS號:暫無
BRN號:暫無
PubChem號:24865631
物性數據
1. 性狀:白色、無味的顆粒狀固體。
2. 密度(g/mL,25/4℃): 4.736
3. 相對蒸汽密度(g/mL,空氣=1):無可用
4. 熔點(oC):446
5. 沸點(oC,常壓):625
6. 沸點(oC,5.2kPa): 無可用
7. 折射率: 無可用
8. 閃點(oC): 625
9. 比旋光度(o): 無可用
10. 自燃點或引燃溫度(oC): 無可用
11. 蒸氣壓(kPa,25oC): 無可用
12. 飽和蒸氣壓(kPa,60oC): 無可用
13. 燃燒熱(KJ/mol):無可用
14. 臨界溫度(oC): 無可用
15. 臨界壓力(KPa): 無可用
16. 油水(辛醇/水)分配系數的對數值:無可用
17. 爆炸上限(%,V/V):無可用
18. 爆炸下限(%,V/V): 無可用
19. 溶解性:溶于水、甘油,在醇和乙醚中能無限溶解。
毒理學數據
在皮膚和粘膜上造成腐蝕性影響,刺激皮膚和粘膜。
生態學數據
該物質對環境可能有危害,對水體應給予特別注意。
分子結構數據
1、摩爾折射率:無可用的
2、摩爾體積(cm3/mol):無可用的
3、等張比容(90.2K):無可用的
4、表面張力(dyne/cm):無可用的
5、介電常數:無可用的
6、極化率(10-24cm3):無可用的
7、單一同位素質量:317.738066 Da
8、標稱質量:318 Da
9、平均質量:319.2179 Da
計算化學數據
1.疏水參數計算參考值(XlogP):無
2.氫鍵供體數量:0
3.氫鍵受體數量:0
4.可旋轉化學鍵數量:0
5.互變異構體數量:無
6.拓撲分子極性表面積0
7.重原子數量:3
8.表面電荷:0
9.復雜度:2.8
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:1
性質與穩定性
1.遵照規格使用和儲存不會分解。碘化鋅溶于水、乙醇、丙酮和液氨等,微溶于乙醚。置于空氣中見光變為棕色。在1150℃左右時,碘化鋅蒸氣開始分解成鋅(或ZnI)和碘。加熱時可被氫還原,與氧作用生成ZnO和碘。在室溫下與氧和水反應生成ZnO和碘。此外,它還能將硫酸還原成SO2,并放出碘。
2.碘化鋅具有很強的吸濕性和光敏感性,應在避光環境中置于干燥處保存。
貯存方法
密封干燥避光保存
合成方法
1.可用金屬鋅與碘直接加熱反應,或碘化鋇與硫酸鋅復分解反應,或碘的乙醚溶液在鋅存在的情況下回流,減壓除乙醚后在400度升華制備。
2.在圓底燒瓶中,加入由電解所得到的高純鋅粉6.5g,碘晶體20g及水70mL,經充分振蕩混合后靜置一段時間。當碘的顏色褪去后,濾出剩余的鋅粉,并將濾液蒸發濃縮至10mL左右。然后把容器移入盛有H2SO4和氮氣保護的真空干燥器內進行干燥。當有結晶析出時,再將其移入盛有NaOH和氮氣保護的真空干燥器內繼續干燥。最后將所得晶體置于耐熱玻璃容器中加熱至300~350℃,經真空升華即可制得純度較高的ZnI2產品。
3.將1份鋅粉,2~4份碘(視鋅粉的純度而定)和10份無水乙醚置于圓底燒瓶中,加熱回流。在液體初始的顏色消失后,停止回流,用砂芯漏斗濾出殘留的Zn-ZnO,然后在減壓下,溫熱產物以除去乙醚,最后在400℃左右升華而得碘化鋅純品。
4.在冷卻條件下將鋅粉、碘和水混合,攪拌下進行反應,控制溫度不超過60℃:
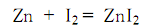
反應結束后,再加入少量鋅,并加熱至溶液變為無色,過濾,濾液加熱濃縮,在溫度低于95℃下減壓蒸發干燥至結晶松散,即為成品。
用途
1.醫療上用作局部防腐消毒劑、收斂劑;用于碘淀粉試劑以測定亞硝酸鹽;用作游離氯和其他氧化劑的試劑。
2.碘化鋅通過轉移金屬化反應能有效制備有機鋅試劑,同時作為一個溫和路易斯酸也能促進加成反應和取代反應的發生。
碘化鋅能與有機金屬試劑如有機鋰、有機鎂和有機銅等發生轉移金屬化反應,得到有機鋅試劑,進而作為親核試劑參與鈀催化的對烷基碘化合物等碳陽離子試劑的碳-碳鍵形成偶聯反應 (式1)[1]。
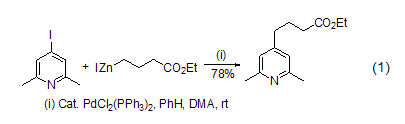
碘化鋅與重氮甲烷作用也為合成Simmons- Smith試劑(碘代碘甲基鋅)提供了一種新的方法 (式2)[2]。

作為一個溫和的路易斯酸,碘化鋅也能催化活潑二烯底物和親二烯底物如呋喃與烯丙基甲酯間的Diels-Alder環加成反應 (式3)[3]。

碘化鋅也能用于活化碳雜原子雙鍵C=X,如通過螯合效應活化官能化的羰基,進而高度立體選擇性地實現與硅基乙烯酮縮醛的羥醛縮合反應 (式4)[4]。
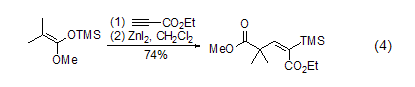
碘化鋅與炔烴在二氯二茂鈦的催化作用下反應生成烯基鋅試劑,該物質進一步和其它親電試劑反應生成多取代烯烴化合物 (式5)[5]。

碘化鋅的路易斯酸性也使得它可以活化多種碳-雜原子C-X鍵,進而實現親核取代反應。如環醚在碘化鋅作用下能夠與RSSiMe3或RSeSiMe3試劑發生親核取代,得到開環后的C-S鍵或C-Se鍵形成產物 (式6)[6]。
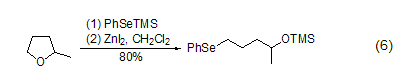
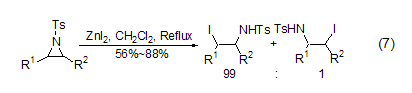
碘化鋅與氮雜環丙烷作用可以高選擇性地得到碘代的開環產物 (式7)[7]。
碘化鋅與還原劑如氰基硼氫化鈉組合能夠將烯丙基或芳基的酮、醛和醇還原為相應的飽和烴化合物 (式8)[8]。

安全信息
危險運輸編碼:暫無
危險品標志: 腐蝕
腐蝕
安全標識:S26 S45 S36/S37/S39
危險標識:R34
文獻
1. Sakamoto, T.; Nishimura, S.; Kondo, Y.; Yamanaka, H. Synthesis, 1988, 485. 2. (a) Wittig, G.; Schwarzenback, K. LA, 1961, 650, 1. (b) Wittig, G.; Wingher, F. LA, 1962, 656, 18. 3. Brion, F. Tetrahedron Lett., 1982, 23, 5239. 4. Quendo, A.; Rousseau, G. Tetrahedron Lett., 1988, 29, 6443. 5. Gao, Y.; harada, K.; Hata, T.; Urabe, H.; Sato, F. J. Org. Chem., 1995, 60, 290. 6. Miyoshi, N.; Hatayama, Y.; Ryu, I.; Kambe, N.; Murai, T.; Murai, S.; Sonoda, Synthesis, 1988, 175. 7. Ghorai, M. K.; Das, K.; Kumar, A.; Ghosh, K. Tetrahedron Lett., 2005, 46, 4103. 8. Lau, C. K.; Dufresne, C.; Belanger, P. C.; Pietre, S.; Scheigetz, J. J. Org. Chem., 1986, 51, 3038. 9.參考書:現代有機合成試劑<性質、制備和反應>;胡躍飛 付華 編著;化學工業出版社;ISBN 7-5025-8542-7
備注
暫無
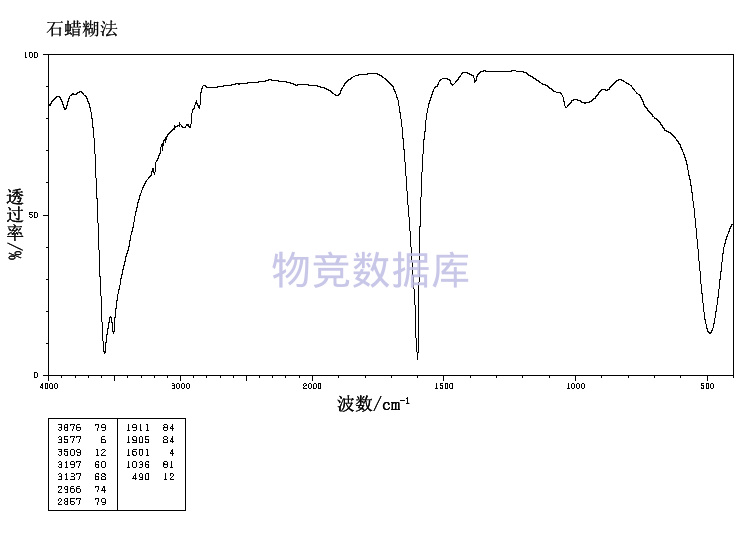
表征圖譜
統計數據
共收錄化學品數據
147579 條



 滬公網安備 31010602001115號
滬公網安備 31010602001115號