氯化鉺(III) Erbium(III)chloride
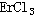
結構式
| 物競編號 | 0KSF |
|---|---|
| 分子式 | ErCl3 |
| 分子量 | 273.62 |
| 標簽 | 三氯化鉺,無水, Erbium(III)chloride,anhydrous |
編號系統
CAS號:10138-41-7
MDL號:MFCD00010989
EINECS號:233-385-0
RTECS號:KD8575000
BRN號:暫無
PubChem號:24868510
物性數據
1. 性狀:粉紅色晶體。
2. 密度(g/mL,25℃):4.100
3. 相對蒸汽密度(g/mL,空氣=1):未確定
4. 熔點(oC):774
5. 沸點(oC,常壓):1500
6. 沸點(oC,5.2kPa):未確定
7. 折射率:未確定
8. 閃點(oC):未確定
9. 比旋光度(o):未確定
10. 自燃點或引燃溫度(oC):未確定
11. 蒸氣壓(kPa,20oC):未確定
12. 飽和蒸氣壓(kPa,60oC):未確定
13. 燃燒熱(KJ/mol):未確定
14. 臨界溫度(oC):未確定
15. 臨界壓力(KPa):未確定
16. 油水(辛醇/水)分配系數的對數值:未確定
17. 爆炸上限(%,V/V):未確定
18. 爆炸下限(%,V/V):未確定
19. 溶解性:溶于水。稍溶于MeOH和THF,并常常在這些溶劑中使用。
毒理學數據
1、急性毒性:大鼠腹腔LD50:4417 mg/kg;豚鼠腹腔LD50:128 mg/kg;小鼠腹腔LD50:226 mg/kg。
生態學數據
通常對水體是稍微有害的,不要將未稀釋或大量產品接觸地下水,水道或污水系統,未經政府許可勿將材料排入周圍環境。
分子結構數據
1、摩爾折射率:無可用的
2、摩爾體積(cm3/mol):無可用的
3、等張比容(90.2K):無可用的
4、表面張力(dyne/cm):無可用的
5、介電常數:無可用的
6、極化率(10-24cm3):無可用的
7、單一同位素質量:270.836858 Da
8、標稱質量:271 Da
9、平均質量:273.618 Da
計算化學數據
1.疏水參數計算參考值(XlogP):無
2.氫鍵供體數量:0
3.氫鍵受體數量:0
4.可旋轉化學鍵數量:0
5.互變異構體數量:無
6.拓撲分子極性表面積0
7.重原子數量:4
8.表面電荷:0
9.復雜度:8
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:1
性質與穩定性
在室溫下可長期保存
貯存方法
暫無
合成方法
暫無
用途
三氯化鉺是鑭系元素鹵化物的重要成員,在有機合成中最成熟的應用是作為一個溫和的Lewis 酸催化劑[1,2]。
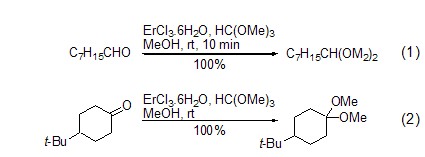
三氯化鉺在甲醇溶液中可以高效地催化醛的縮醛化反應[3]。如果使用原甲酸三甲酯作為除水試劑的話,反應可以直接使用ErCl3·6H2O。該反應在室溫下進行時,脂肪族醛只需數分鐘就可定量地完成反應。芳香肪族醛在反應時間和產率上表現出稍稍偏低的活性 (式1)。在與醛完全相同的反應條件下,脂肪族酮可以定量地完成反應,而芳香肪族酮則幾乎不反應。在明顯的位阻情況下可以實現兩種不同酮的選擇性縮酮化反應 (式2)。
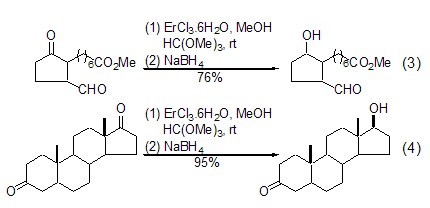
正是由于醛-酮結構差異和酮-酮結構差異對該反應表現出顯著的選擇性,所以可以實現含有醛-酮結構和酮-酮結構底物分子的選擇性還原[4]。與其它鑭系元素鹵化物比較,三氯化鉺在該轉化中具有最好選擇性。在三氯化鉺存在下,NaBH4可以選擇性地還原醛-酮結構分子中的酮羰基成為醇,而醛羰基保持不變 (式3)。酮-酮結構分子有時具有更好的選擇性 (式4)。
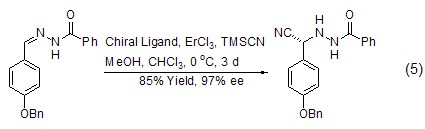
最近一篇論文報道顯示[5],三氯化鉺在催化醛腙與TMSCN的手性氰基化反應中表現出比同族其它氯化物更高的化學產率和光學產率。5% 摩爾用量的三氯化鉺便可滿足該反應需求 (式5)。
安全信息
危險運輸編碼:暫無
危險品標志: 刺激
刺激
安全標識:暫無
危險標識:暫無
文獻
1. Molander, G. A. Chem. Rev., 1992, 92, 29. 2. Kagan, H. B.; Namy, J. L. Tetrahedron, 1986, 42, 6573. 3. Luche, J.; Gemal, A. L. Chem. Commun., 1978, 976. 4. Gemal, A. L. Luche, J. L. J. Org. Chem., 1979, 44, 4187. 5. Keith, J. M.; Jacobsen, E. N. Org. Lett., 2004, 6, 153. 6.參考書:現代有機合成試劑<性質、制備和反應>;胡躍飛 付華 編著;化學工業出版社;ISBN 7-5025-8542-7
備注
暫無
表征圖譜
統計數據
共收錄化學品數據
147579 條




 滬公網安備 31010602001115號
滬公網安備 31010602001115號