氫化鋁鋰 Lithium aluminium hydride
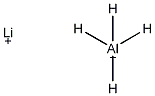
結(jié)構(gòu)式
| 物競編號 | 0NDH |
|---|---|
| 分子式 | LiAlH4 |
| 分子量 | 37.95 |
| 標簽 | 四氫化鋁鋰, LAH, Lithium alanate, Lithium tetrahydroaluminate, 還原劑 |
編號系統(tǒng)
CAS號:16853-85-3
MDL號:MFCD00011075
EINECS號:240-877-9
RTECS號:BD0100000
BRN號:暫無
PubChem號:24882214
物性數(shù)據(jù)
1.性狀:白色疏松的結(jié)晶塊或粉末,有吸濕性,放置時變成灰色。[8]
2.熔點(℃):>125(分解)[9]
3.相對密度(水=1):0.92[10]
4.溶解性:不溶于烴類,溶于乙醚、四氫呋喃。[11]
毒理學(xué)數(shù)據(jù)
1.急性毒性[12] LC50:85mg/m3(小鼠吸入)
2.刺激性 暫無資料
生態(tài)學(xué)數(shù)據(jù)
通常對水體是稍微有害的,不要將未稀釋或大量產(chǎn)品接觸地下水,水道或污水系統(tǒng),未經(jīng)政府許可勿將材料排入周圍環(huán)境。
分子結(jié)構(gòu)數(shù)據(jù)
暫無
計算化學(xué)數(shù)據(jù)
1.疏水參數(shù)計算參考值(XlogP):無
2.氫鍵供體數(shù)量:0
3.氫鍵受體數(shù)量:0
4.可旋轉(zhuǎn)化學(xué)鍵數(shù)量:0
5.互變異構(gòu)體數(shù)量:無
6.拓撲分子極性表面積0
7.重原子數(shù)量:2
8.表面電荷:0
9.復(fù)雜度:0
10.同位素原子數(shù)量:0
11.確定原子立構(gòu)中心數(shù)量:0
12.不確定原子立構(gòu)中心數(shù)量:0
13.確定化學(xué)鍵立構(gòu)中心數(shù)量:0
14.不確定化學(xué)鍵立構(gòu)中心數(shù)量:0
15.共價鍵單元數(shù)量:6
性質(zhì)與穩(wěn)定性
1.容易吸潮分解,室溫時在干燥空氣中穩(wěn)定。其乙醚溶液可作還原劑或氫化劑。
2.氫化鋁鋰的固體和溶液都具有高度可燃性,必須隔絕空氣、濕氣,并最好在氮氣氛下保存。
3.穩(wěn)定性[13] 穩(wěn)定
4.禁配物[14] 強氧化劑、酸類、醇類、水
5.避免接觸的條件[15] 潮濕空氣、受熱
6.聚合危害[16] 不聚合
7.分解產(chǎn)物[17] 金屬鋁、氫氣
貯存方法
儲存注意事項[18] 儲存于陰涼、干燥、通風(fēng)良好的專用庫房內(nèi),遠離火種、熱源。庫溫不超過32℃,相對濕度不超過75%。包裝密封。應(yīng)與氧化劑、酸類、醇類等分開存放,切忌混儲。儲區(qū)應(yīng)備有合適的材料收容泄漏物。
合成方法
1.用氫化鋰為原料與三氯化鋁或三溴化鋁在乙醚溶液中作用,可制得氫化鋁鋰。
預(yù)先粉碎氫化鋰;在N2氣氛圍中將塊狀的氫化鋰粉碎成細小顆粒,并過篩。顆粒大小決定反應(yīng)的難易。
乙醚的干燥:所用的乙醚須絕對干燥并且不含過氧乙醚。用CaCl2和金屬鈉來干燥還顯不夠,應(yīng)用NaOH或CaH2脫水,然后進行蒸餾以除去水分和過氧乙醚。
氫化鋁鋰的制備:取三口燒瓶、滴液漏斗、回流冷凝器、攪拌棒等進行干燥后備用。并注意切莫使AlCl3吸潮。
在三口燒瓶中加入23.5g(2.96mol)的LiH和200mL乙醚制成懸濁液,在強烈的攪拌下滴加入71.2g(0.534mol)的三氯化鋁乙醚溶液300mL。乙醚呈現(xiàn)沸騰狀說明反應(yīng)開始。調(diào)節(jié)滴加速度控制反應(yīng)平穩(wěn)的進行。AlCl3滴加完畢后,繼續(xù)攪拌直至反應(yīng)終止,靜置片刻。用N2氣將燒瓶中的反應(yīng)物壓出,使經(jīng)過一個玻璃砂芯漏斗過濾,將澄清的濾液蒸發(fā)至黏稠狀,殘余的乙醚在減壓下70℃除去,剩余物即為氫化鋁鋰。收率約85%。
如果滴加AlCl3時未發(fā)生反應(yīng),或者反應(yīng)以后又停下來,表明LiH粉碎得細度不夠。遇以上情況可在燒瓶中加30mL LiAlH4(3g)的乙醚溶液作為引發(fā)劑,以避免反應(yīng)因延緩可能導(dǎo)致的突發(fā)式的爆炸反應(yīng)。
若以AlBr3代替AlCl3,LiH的顆粒可不必太細,可以似黃豆大小,不致影響反應(yīng)的進行。操作步驟類似于使用AlCl3。加完AlBr3可加熱至乙醚沸騰的溫度,冷卻后過濾即得LiAlH4的乙醚溶液。
用途
1.羰基試劑。還原劑。制造其他氫化物及硅烷、硼烷等。在醫(yī)藥、香料、農(nóng)藥、染料及其他精細有機合成中用作還原劑。可將醛酮、酸、酸酐、酯、醌、酰氯等還原為醇,將腈還原為伯胺,將鹵化烴還原為烴,芳香硝基化合物還原成偶氮化合物。但通常不能使碳—碳雙鍵氫化。100份乙醚能溶本品30份,100份四氫呋喃能溶13份,100份二甲基溶纖劑能溶10份,100份二丁醚能溶2份,100份二氧六環(huán)能溶0.1份。
2.氫化鋁鋰是有機化學(xué)中一個常用的還原試劑,能夠還原多種官能團化合物;同時也能作用于雙鍵和三鍵化合物實現(xiàn)氫鋁化反應(yīng);氫化鋁鋰也能作為堿參與反應(yīng)。
氫化鋁鋰具有很強的氫轉(zhuǎn)移能力,能夠?qū)⑷⑼Ⅴァ?nèi)酯、羧酸、酸酐和環(huán)氧化物還原為醇,或者將酰胺、亞胺離子、腈和脂肪族硝基化合物轉(zhuǎn)換為對應(yīng)的胺。此外,氫化鋁鋰超強的還原能力使得可以作用于其它官能團,如將鹵代烷烴還原為烷烴 (式1)[1]。該類反應(yīng)中,鹵代物的活性從大到小依次是碘代物、溴代物和氯代物。
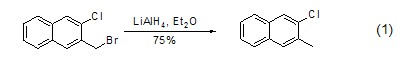
通常氫化鋁鋰對醚類化合物無反應(yīng)活性,但也有例外,如將鄰酯衍生物高產(chǎn)率地轉(zhuǎn)換為羧醛 (式2)[2]。
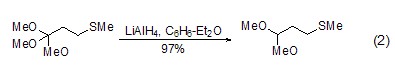
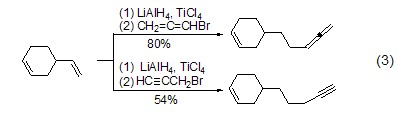
氫化鋁鋰能夠?qū)οN發(fā)生氫鋁化反應(yīng),得到Al-C鍵中間體,進而能夠與其它親核試劑如鹵代物反應(yīng),實現(xiàn)烯烴的加成反應(yīng) (式3)[3]。該類反應(yīng)通常需要加入路易斯酸如四氯化碳或氯化鎳,才能獲得較好的反應(yīng)活性。
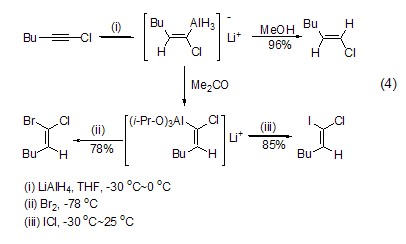
同樣,氫化鋁鋰也能對炔烴發(fā)生氫鋁化反應(yīng),得到sp2-C-Al鍵中間體,進而與質(zhì)子、溴和碘正離子反應(yīng)得到相應(yīng)的官能化烯烴產(chǎn)物 (式4)[4]。
當烯烴或炔烴底物含有鄰位羥基時,氫化鋁鋰能夠單獨誘導(dǎo)實現(xiàn)氫鋁化反應(yīng) (式5)[5]。這是因為鋁有很強的親氧性,在反應(yīng)中能夠形成穩(wěn)定的鋁-氧鍵成環(huán)狀中間體,從而利于氫轉(zhuǎn)移反應(yīng)的發(fā)生。

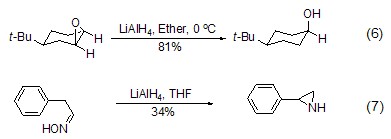
環(huán)氧化合物在氫化鋁鋰作用下能夠發(fā)生還原斷裂反應(yīng),得到相應(yīng)的開環(huán)產(chǎn)物 (式6)[6]。該類反應(yīng)中,負氫離子通常進攻空間位阻較小的碳端。肟在氫化鋁鋰的作用下,則能通過氫還原發(fā)生閉環(huán)反應(yīng),得到氮雜環(huán)丙烷產(chǎn)物 (式7)[7]。
3.用作聚合催化劑、還原劑、噴氣發(fā)動機燃料,也用于合成藥物。[19]
安全信息
危險運輸編碼:暫無
危險品標志: 很易燃
很易燃  極易燃
極易燃  有害
有害  刺激
刺激  腐蝕
腐蝕
安全標識:S43
危險標識:R10 R11 R12 R15 R19 R22 R34 R40 R66 R67 R36/37 R14/15
文獻
1. Karabatsos, G. J.; Shone, R. L. J. Org. Chem., 1968, 33, 619. 2. Claus, C. J.; Morgenthau, J. L. J. Am. Chem. Soc., 1951, 73, 5005. 3. (a) Sato, F.; Kodama, H.; Sato, M.; Chem. Lett., 1978, 789. (b) Sato, F.; Ogura, K.; Sato, M. Chem. Lett., 1978, 805. 4. Zweifel, G.; Lewis, W.; On, H. P. J. Am. Chem. Soc., 1979, 101, 5101. 5. Keck, G. E.; Webb, R. R. Tetrahdron Lett., 1982, 23, 3051. 6. Rickborn, B.; Quartucci, J. J. Org. Chem., 1984, 29, 3185. 7. Kotera, K.; Kitahonoki, K. Tetrahedron Lett., 1965, 1059. [1~7]參考書:現(xiàn)代有機合成試劑<性質(zhì)、制備和反應(yīng)>;胡躍飛 付華 編著;化學(xué)工業(yè)出版社;ISBN 7-5025-8542-7 [8~19]參考書:危險化學(xué)品安全技術(shù)全書.第一卷/張海峰主編.—2版.北京;化學(xué)工業(yè)出版社,2007.6 ISBN 978-7-122-00165-8
備注
暫無
表征圖譜
統(tǒng)計數(shù)據(jù)
共收錄化學(xué)品數(shù)據(jù)
147579 條




 滬公網(wǎng)安備 31010602001115號
滬公網(wǎng)安備 31010602001115號