N,N-二甲基亞甲基碘化胺 N,N-Dimethylmethyleneammonium iodide
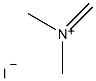
結構式
| 物競編號 | 0RTC |
|---|---|
| 分子式 | C3H8IN |
| 分子量 | 185.01 |
| 標簽 | 二甲基亞甲基碘化銨, n,n-二甲基亞甲基碘化胺, (N,N-二甲基), N,N-二甲基亞甲基碘化銨, Eschenmoser's Salt, Dimethyl methylene ammonium Iodide, Dimethyl methyleneimmonium iodide, N,N-Dimethylmethyleneammonium Iodide, N,N-Dimethylmethyleneiminium Iodide, Dimethyl Methyleneammonium Iodide~Eschenmosers Iodide Salt, (N,N-Dimethyl)Methyleneammoniumiodi |
編號系統
CAS號:33797-51-2
MDL號:MFCD00011810
EINECS號:251-680-2
RTECS號:暫無
BRN號:1731022
PubChem號:24865478
物性數據
1. 性狀:淺黃色固體
2. 密度(g/mL,20℃):未確定
3. 相對蒸汽密度(g/mL,空氣=1):未確定
4. 熔點(oC):240
5. 沸點(oC,常壓):未確定
6. 沸點(oC,KPa):未確定
7. 折射率:未確定
8. 閃點(oC):未確定
9. 比旋光度(o):未確定
10. 自燃點或引燃溫度(oC):未確定
11. 蒸氣壓(Pa,20oC):未確定
12. 飽和蒸氣壓(KPa,20oC):未確定
13. 燃燒熱(KJ/mol):未確定
14. 臨界溫度(oC):未確定
15. 臨界壓力(KPa):未確定
16. 油水(辛醇/水)分配系數的對數值:未確定
17. 爆炸上限(%,V/V):未確定
18. 爆炸下限(%,V/V):未確定
19. 溶解性:溶于DMF,稍溶于MeOH、THF、MeCN和CH2Cl2,但是溶解度不影響該試劑在這些溶劑中的使用。
毒理學數據
暫無
生態學數據
通常對水是稍微有危害的,若無政府許可,勿將材料排入周圍環境。
分子結構數據
暫無
計算化學數據
1、 疏水參數計算參考值(XlogP):
2、 氫鍵供體數量:0
3、 氫鍵受體數量:1
4、 可旋轉化學鍵數量:0
5、 互變異構體數量:
6、 拓撲分子極性表面積(TPSA):3
7、 重原子數量:5
8、 表面電荷:0
9、 復雜度:26.3
10、同位素原子數量:0
11、確定原子立構中心數量:0
12、不確定原子立構中心數量:0
13、確定化學鍵立構中心數量:0
14、不確定化學鍵立構中心數量:0
15、共價鍵單元數量:2
性質與穩定性
1.如果遵照規格使用和儲存則不會分解,未有已知危險反應。
2.避免氧化物、水分等。
3.具有較強的吸濕性,對濕氣非常敏感,試劑瓶需要用石蠟封口。
貯存方法
密封、在2 oC -8 oC下保存
合成方法
1. 將三甲胺、二碘甲烷、二氧六環和無水乙醇的混合物置暗處在室溫反應100h,濾集生成的晶體,依次用乙醇和乙醚洗滌,在70℃真空干燥,得到碘甲基三甲基碘化銨。將其和環丁砜一起加熱,至160℃保持12min,濾集析出的晶體,用四氯化碳洗滌,在50℃真空干燥,得成品。
2. 制二甲基亞甲基碘化銨在裝有攪拌器、溫度計、氮氣導入管、與冷阱相連的導出管的干燥四頸燒瓶中,加入40.0克(0 .122摩爾)碘甲基三甲基碘化鐵和120毫升環丁諷(用前先后經過氫氧化鈣、氫化鈣蒸餾)。通氮氣沖洗,在攪拌和緩慢注入氮氣流下,置油浴中加熱至160℃,約12分鐘。升溫130℃時晶體迅速溶解,碘甲烷被氮氣流帶入冷阱。冷卻,從黃色溶液中析出晶體,氮氣氛中吸濾晶體,用四氯化碘洗滌五次至近無色,在高真空下50℃干燥,得到二甲基亞甲基碘化按18 .4克(81%)。
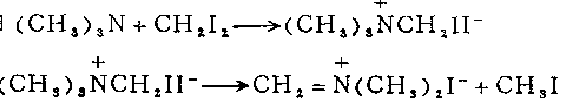
3. 在裝有電磁攪拌棒、橡皮帽、氮氣導入管的干燥25。毫升三頸燒瓶中,加入現制備的32.8克(0.164摩爾)碘化三甲硅溶于20毫升無水乙醚的溶液。在0℃下加入1毫升2一甲基一2一丁烯以除去碘化三甲硅水解產生的碘化氫,并滴加16.8i克(0.164摩爾)N,N,N’,N‘,一四甲基亞甲二胺溶寸:20毫升無水乙醚的溶·液。立即生成白色沉淀,繼續攪拌20分鐘。吸濾,用無水乙醚洗滌(3份每份75毫升),空氣干燥,立即入真空于燥器貯存。得產品29.1克96%)。如果需要,可以減壓升華或從環丁颯中重結晶。
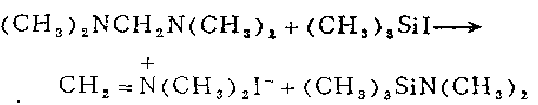
用途
1. 用作高反應性的Mannich試劑。與格氏試劑、乙烯基鋰、苯硫酚鈉及穩定的負碳離子加成。將甲基引入可碄核(Corrin nucleus)內醋亞甲化。
2. Eschenmoser鹽在有機合成中被定義為Mannich反應中甲醛和二甲胺的替代物。由于Mannich反應是一個可逆反應,所以許多時候直接使用甲醛和二甲胺發生的反應具有產率低的缺點。Eschenmoser鹽實際上是甲醛和二甲胺生成的亞胺鹽,不僅使用操作比較方便,而且具有更高的反應活性。
Eschenmoser鹽在Mannich反應中與能夠形成碳負離子的底物分子發生親電胺甲基化反應,在底物分子中引入N,N-二甲氨基甲基片段。被醛、酮羰基或者酯基致活的亞甲基或者次甲基均可以發生該反應,生成β-二甲氨基醛、酮或者酯 (式1)[2]。該試劑與帶有推電子基取代的芳香碳環或者富電子的芳香雜環化合物的胺甲基化反應非常容易[3,4]。吲哚或者吡唑衍生物可以在非常溫和的條件下給出幾乎定量的產率 (式2,式3)[5,6]。

該試劑最重要的應用價值是在有機合成中作為一碳合成子,與醛和酮羰基、酯基致活的亞甲基或者次甲基發生反應生成α-取代的丙烯醛、酮或者酯。實質上,該反應產物是Mannich反應前期產物β-二甲氨基醛、酮或者酯進一步發生二甲胺消去反應形成的最終產物。所以,只需提高Mannich反應的溫度和延長Mannich反應的時間即可得到理想的產物。環酮和內酯在該反應中生成相應的環外雙鍵具有特別重要的意義 (式4,式5)[7,8]。

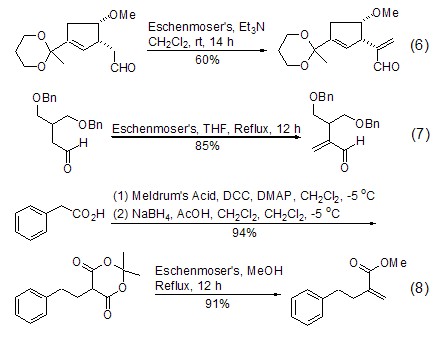
由于Eschenmoser鹽可以在非常溫和的條件下制備具有重要合成價值的α-取代的丙烯醛和丙烯酸酯,所以在天然產物的合成中得到了廣泛的應用。生成α-取代的丙烯醛的反應大多情況下是將底物與Eschenmoser鹽在CH2Cl2中攪拌數小時即可。加入三乙胺或者升高反應的溫度可以達到增加反應速度的效果 (式6,式7)[9~11]。首先將羧酸與Meldrum’s酸縮合生成單烷基化的Meldrum’s酸衍生物,然后再與Eschenmoser鹽在甲醇中回流,則構成了一條獲得α-取代丙烯酸酯的方便途徑 (式8)[12]。
安全信息
危險運輸編碼:暫無
危險品標志: 刺激
刺激
危險標識:R36/37/38
文獻
1. Bryson, T. A.; Bonitz, G. H.; Reichel, C. J.; Dardis, R. E. J. Org. Chem., 1980, 45, 524. 2. Langlois, N.; Le Nguyen, B. K. J. Org. Chem., 2004, 69, 7558. 3. Wang, Z.; Huynh, H. K.; Han, B.; Krishnamurthy, R.; Eschenmoser, A. Org. Lett., 2003, 5, 2067. 4. Bream, R. N.; Ley, S. V.; Procopiou, P. A. Org. Lett., 2002, 4, 3793. 5. Cai, X.; Snieckus, V. Org. Lett., 2004, 6, 2293. 6. Fan, D.; Taniguchi, M.; Yao, Z.; Dhanalekshmi, S.; Lindsey, J. S. Tetrahedron, 2005, 61, 10291. 7. Shing, T. K. M.; Lee, C. M.; Lo, H. Y. Tetrahedron, 2004, 60, 9179. 8. Mihelcic, J.; Moeller, K. D. J. Am. Chem. Soc., 2004, 126, 9106. 9. Zhao, L.; Burnell, D. J. Org. Lett., 2006, 8, 155. 10. Smith, A. B., III; Sfouggatakis, C.; Gotchev, D. B.; Shirakami, S.; Bauer, D.; Zhu, W.; Doughty, V. A. Org. Lett., 2004, 6, 3637. 11. Wang, J.; Hsung, R. P.; Ghosh, S. K. Org. Lett., 2004, 6, 1939. 12. Hin, B.; Majer, P.; Tsukamoto, T. J. Org. Chem., 2002, 67, 7365. 13.參考書:現代有機合成試劑<性質、制備和反應>;胡躍飛 付華 編著;化學工業出版社;ISBN 7-5025-8542-7
備注
暫無
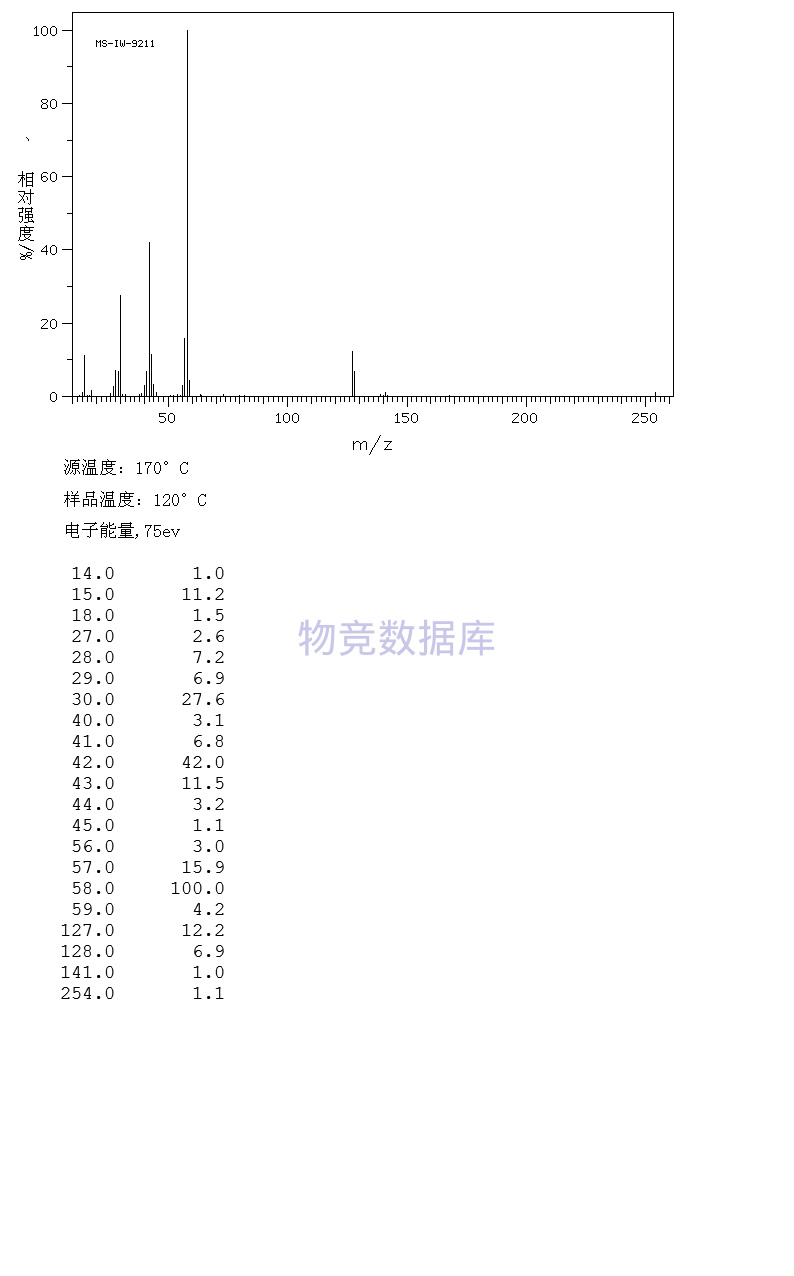
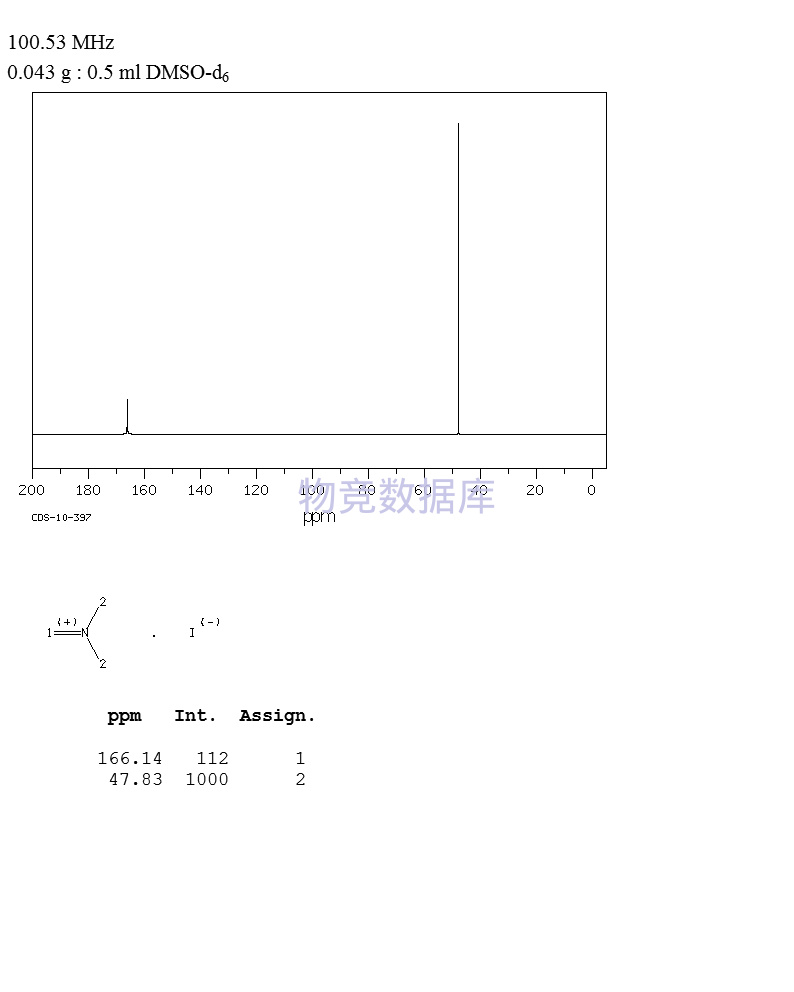
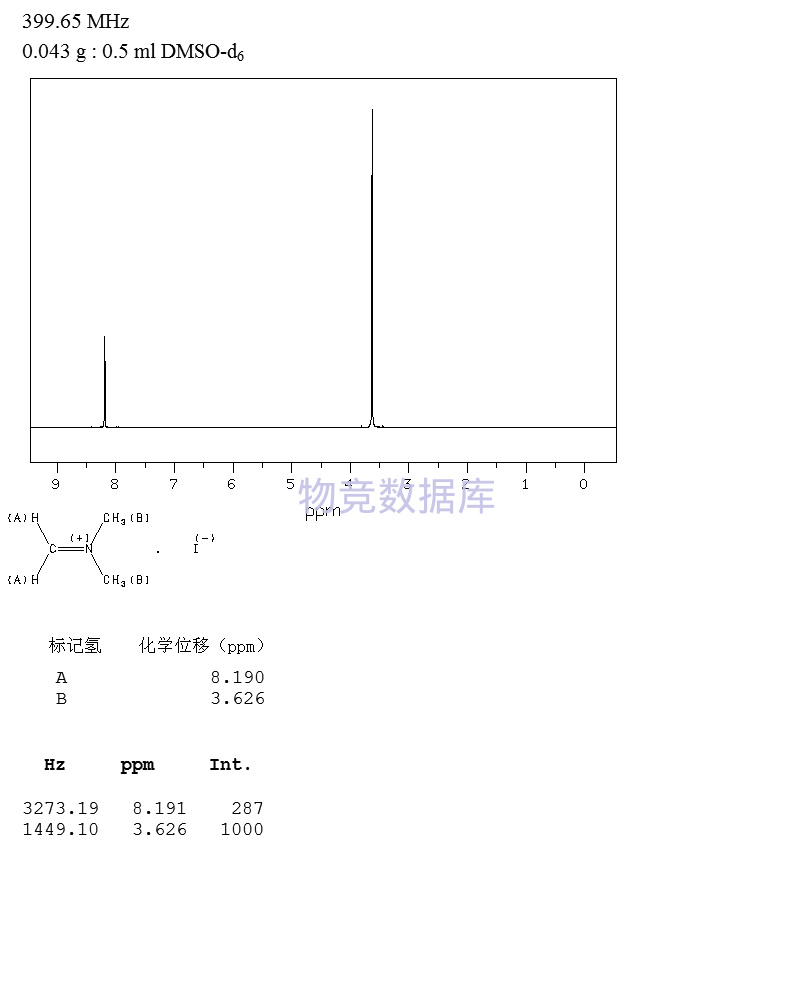
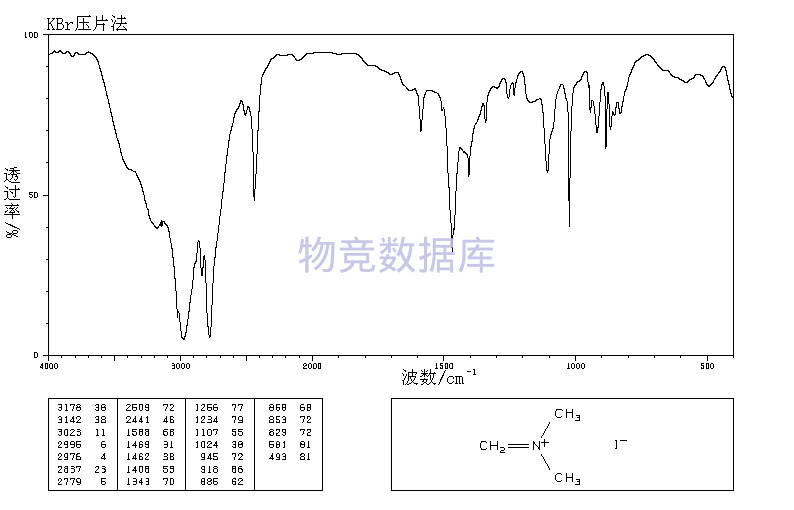
表征圖譜
統計數據
共收錄化學品數據
147579 條




 滬公網安備 31010602001115號
滬公網安備 31010602001115號