硼氫化鈉 Sodium borohydride
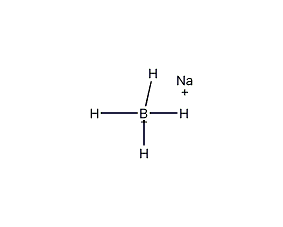
結構式
| 物競編號 | 0NF3 |
|---|---|
| 分子式 | NaBH4 |
| 分子量 | 37.83 |
| 標簽 | Sodium tetrahydroborate, 鈉硼氫, 發泡劑, 還原劑, 氫化劑, 處理劑 |
編號系統
CAS號:16940-66-2
MDL號:MFCD00003518
EINECS號:241-004-4
RTECS號:ED3325000
BRN號:暫無
PubChem號:24886165
物性數據
1. 性狀:白色結晶粉末,易吸潮,遇火可燃。
2. 密度(g/mL,25/4℃):1.074
3. 相對蒸汽密度(g/mL,空氣=1):1.074
4. 熔點(oC):36~37
5. 閃點(oC):69
6. 溶解性:水溶性550 g/L (25oC)。溶于水、液氨、胺類,微溶于四氫呋喃,不溶于乙醚、苯、烴。
毒理學數據
小鼠口經LD50:160 mg/kg
生態學數據
通常對水體是稍微有害的,不要將未稀釋或大量產品接觸地下水,水道或污水系統,未經政府許可勿將材料排入周圍環境。
分子結構數據
暫無
計算化學數據
1.疏水參數計算參考值(XlogP):無
2.氫鍵供體數量:0
3.氫鍵受體數量:1
4.可旋轉化學鍵數量:0
5.互變異構體數量:無
6.拓撲分子極性表面積0
7.重原子數量:2
8.表面電荷:0
9.復雜度:2
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:2
性質與穩定性
1.常溫常壓下穩定
避免的物料:水分/潮濕 氧化物 酸 還原劑 氯化氫。在真空400 ℃時分解。有吸濕性,在干空氣中穩定,在濕空氣中分解。溶于水、液氨、胺類,微溶于四氫呋喃,不溶于乙醚、苯、烴。與水作用產生氫氣。硼氫化鈉堿性溶液呈棕黃色。
2.與硼氫化鈉接觸后有咽喉痛、咳嗽、呼吸急促、頭痛、腹痛、腹瀉、眩暈、眼結膜充血、疼痛等癥狀。
3.吸入或者皮膚接觸該試劑對人體有害。試劑應干燥保存,使用時應特別小心,操作時在通風櫥中進行。
貯存方法
1.應貯存在陰涼、干燥的庫房中。
2.防潮,防震,勿與無機酸共貯混運,遠離熱源和火種及易燃物品。
合成方法
1. 氫化鈉硼酸甲酯法 將硼酸和適量甲醇加入精餾釜中,徐徐加熱,在54 ℃全回流2 h,然后收集硼酸甲酯與甲醇共沸液。共沸液經硫酸處理,精餾后可得較純產物。將由氫氣與鈉作用而得的氫化鈉送入縮合反應罐中,在攪拌下加熱至220 ℃左右開始加硼酸甲酯,至260 ℃時停止加熱;加料溫度控制在280 ℃以下,加料后繼續攪拌,使其充分反應。反應完成后冷卻至100 ℃以下,離心分離,得縮合產物濾餅。在水解器中加入適量的水,將濾餅緩慢加入水解器中,控制溫度在50 ℃以下,加料完畢后升溫至80 ℃,離心分離,水解液則送入分層器中,靜止1h后自動分層,下層水解液即為硼氫化鈉溶液。其反應式如下:

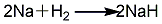
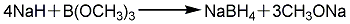
2. 硼氫化鈉的生產可分為干法和濕法兩類。干法是用無水硼砂和石英砂在高溫下熔融反應生成硼硅酸鈉,將后者粉碎后與金屬鈉和氫氣,在450~500℃溫度和(3.04~5.07)×105Pa壓力下反應,生成硼氫化鈉和硅酸鈉。濕法是先用硼酸和甲醇反應合成硼酸三甲酯。將金屬鈉分散于石蠟油中,通氫氣合成氫化鈉。然后硼酸三甲酯和氫化鈉在石蠟油介質中反應合成硼氫化鈉。
一般工業上主要是用濕法生產硼氫化鈉,整個工藝過程可分為四個步驟:
(1)酯化:在粗餾釜中加入化學計量的硼酸及甲醇,緩慢加熱。在54℃回流2h之后,開始收集硼酸三甲酯與甲醇的共沸液,控制溫度在54~55℃。超過55℃時停止收集。在56~69℃溫度下回收甲醇。粗餾殘液可回收硼酸。共沸液在酸洗槽中用硫酸脫醇,然后進行精餾,得到較純的硼酸三甲酯。精餾后的殘液回收硼酸三甲酯和甲醇。
(2)氫化:在氫化釜中放入石蠟油,經攪拌、靜置后,在溫度低于100℃時,將切成小塊的金屬鈉投入石蠟油中,攪拌,升溫。當溫度升至200℃時,停止加熱。通入氫氣,與分散于石蠟油中的金屬鈉進行反應。反應溫度應控制在300℃以下,溫度若高于300℃,應向氫化釜中加入冷石蠟油調節。待反應完成后,停止通入氫氣,金屬鈉基本上能全部轉化成氫化鈉。
(3)縮合:將氫化反應完成后的石蠟油料液送入縮合器中,開動攪拌。加熱至220℃時。開始加入硼酸三甲酯,這時溫度明顯上升,當溫度升至260℃時停止加熱。加料進程中,溫度不應超過280℃。硼酸三甲酯加完后,繼續攪拌,使其充分反應。反應溫度最好控制在275℃左右,反應完成后產率可達90%。將物料冷卻至100℃以下,進行離心分離得到硼氫化鈉濾餅。分離出的石蠟油可回收利用。
(4)水解:在水解器中加入計量的水,將上述硼氫化鈉濾餅徐徐加入水解器中,加料時水溫控制在50℃以下。加料完畢后溫度升至80℃。因水解時甲醇鈉分解成氫氧化鈉和甲醇,溶液呈強堿性,水解溫度稍高,硼氫化鈉亦無明顯分解。將此水解液離心分離,清液送入分層器中,靜置1h后自動分層。下層水解液中含硼氫化鈉和氫氧化鈉,這種硼氫化鈉堿性水溶液即可作為商品出售,其中硼氫化鈉含量要求不低于5%。
若要制取固體NaBH4產品,可在硼氫化鈉堿性水溶液中加入異丙胺(CH3)2CHNH2,在萃取器中將NaBH4萃取到有機相中。然后再在另一萃取器中用稀NaOH溶液反萃。異丙胺回收利用,堿液送去結晶。經過離心分離,得到NaBH4·2H2O結晶體,母液回收利用。濕晶體干燥之后得到NaBH4固體產品,其純度不應低于97%。
硼氫化鈉的分析是用碘量法間接滴定其中BH-4離子。在堿性試液中加入已知過量的KIO3溶液,硼氫陰離子被氧化為硼酸,然后加入KI,酸化試液。靜置一定時間后,用Na2S2O3標準溶液滴定由過量碘酸鉀所析出的碘。用途
1. 用作制造氫和硼氫化物。醛酮的還原。橡膠發泡劑。有機化合物中微量醛、酮、過氧化物的清除。
2. 是一種良好的還原劑,它的特點是性能穩定,還原時有選擇性。可用作醛類、酮類和酰氯類的還原劑,塑料的發泡劑,制造雙氫鏈霉素的氫化劑,制造硼氫化鉀的中間體,合成硼烷的原料,以及用于造紙工業和含汞污水的處理劑等。硼氫化鈉具有強還原性,用作化學鍍鎳、鈷等的還原劑。
3. 硼氫化鈉是一個溫和且具化學選擇性的還原試劑,屬于硼氫化合物家族的成員,在含有羥基的溶劑 (如水、醇) 中,室溫下能快速地將醛和酮還原;對羰基具有極強的還原性,作為還原劑廣泛地應用于有機合成中;通過控制反應條件或選擇不同的反應溶劑,可以實現對官能團的選擇性還原。
羰基化合物的還原 硼氫化鈉能夠還原包括醛、酮在內的很多類物質。如以乙醇為溶劑,硼氫化鈉能夠將醛類化合物還原為一級醇,該還原反應的產率很高,達到90%以上 (式1)[1,2]。
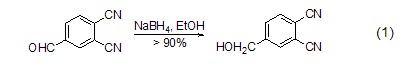
同樣,在醇溶劑中,硼氫化鈉也可將酮還原為二級醇 (式2)[3~5]。
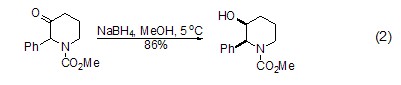
由于它的強還原性,它可以還原酯等相對來說較難還原的物質,如利用膠束來實現酯的還原 (式3)[6]。酯的還原也可在醇等溶劑中實現[7,8]。
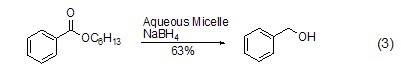
另外,硼氫化鈉對酰胺鍵也具有還原作用(式4)[9],此反應的進行類似于多肽鏈的降解。
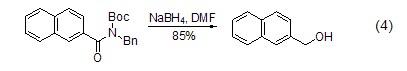
選擇性還原 硼氫化鈉雖然還原性較強,能夠還原很多官能團,但是在某些條件下具有還原選擇性。比如雖然它可以還原酮,但在一定情況下只與醛反應,將醛還原成醇,而同時存在的酮羰基不反應。利用硼氫化鈉的這種選擇性還原,可以進行很多有用的特殊合成。例如用硼氫化鈉對酰胺基和酯基的選擇性還原(式5)[10,11]。
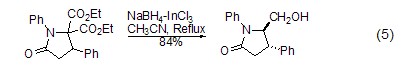
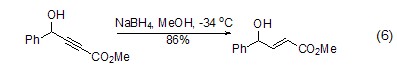
對雙鍵、三鍵的還原 硼氫化鈉除了可用在羰基化合物的還原上,也可對雙鍵 (如碳-氮雙鍵[12]) 或三鍵 (如炔烴[13]) 化合物進行還原。如在硼氫化鈉的作用下,炔烴化合物還原為烯烴,還原得到的烯烴不會進一步被硼氫化鈉還原 (式6)。
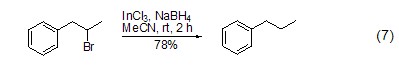
與鹵代烴的反應 在過渡金屬催化劑的存在下,硼氫化鈉能夠將鹵代烴轉化為烷烴 (式7)[14]。該反應可能經歷了自由基過程,首先是InCl3在NaBH4作用下形成InCl2自由基,然后通過自由基取代的方式,將鹵代烴轉化為相應的烷烴。使用類似的方法,還可實現炔烴到烯烴的轉化。
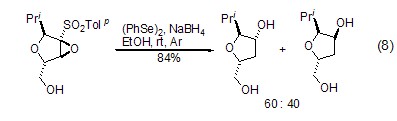
其它合成反應 硼氫化鈉還可與有機硒化合物作用,在硒元素部位引入其它的基團 (如鹵代甲基等,該鹵代甲基可以進一步與其它試劑作用,從而使得分子存在多種衍生化方式)[15],或者通過有機硒的催化作用發生開環反應等 (式8)[16]。
安全信息
危險運輸編碼:暫無
危險品標志: 易燃
易燃  有毒
有毒  有害
有害  腐蝕
腐蝕
安全標識:S22 S26 S43 S45 S36/S37/S39
文獻
1. Guldi, D. M.; Gouloumis, A.; Vázquez, P.; Torres, T.; Georgakilas, V.; Prato, M. J. Am. Chem. Soc., 2005, 127, 5811. 2. Zhong, G. F. Angew. Chem., Int. Ed., 2003, 42, 4247. 3. Kise, N.; Ohya, K.; Arimoto, K.; Yamashita, Y.; Hirano, Y.; Ono, T.; Ueda, N. J. Org. Chem., 2004, 69, 7710. 4. Correa, N. M.; Zorzan, D. H.; D′Anteo, L.; Lasta, E.; Chiarini, M.; Cerichelli, G. J. Org. Chem., 2004, 69, 8231. 5. Correa, N. M.; Zorzan, D. H.; Chiarini, M.; Cerichelli, G. J. Org. Chem., 2004, 69, 8224. 6. Das, D.; Roy, S.; Das, P. K. Org. Lett., 2004, 6, 4133. 7. Kwon, S. J.; Ko, S. Y. J. Org. Chem., 2001, 66, 6833. 8. Luo, W.; Yu, Q.-S.; Holloway, H. W.; Parrish, D.; Greig, N. H.; Brossi, A. J. Org. Chem., 2005, 70, 6171. 9. Ragnarsson, U.; Grehn, L.; Maia, H. L. S.; Monteiro, L. S. Org. Lett., 2001, 3, 2021. 10. Haldar, P.; Ray, J. K. Org. Lett., 2005, 7, 4341. 11. Leban, J. J.; Colson, K. L. J. Org. Chem., 1996, 61, 228. 12. Mori, S.; Shin, J.-Y.; Shimizu, S.; Ishikawa, F.; Furuta, H.; Osuka, A. Chem. Eur. J., 2005, 11, 2417. 13. Meta, C. T.; Koide, K. Org. Lett., 2004, 6, 1785. 14. Hayashi, N.; Shibata, I.; Baba, A. Org. Lett., 2004, 6, 4981. 15. Qin, Y.-Y.; Qiu, X.-L.; Yang, Y.-Y.; Meng, W.-D.; Qing, F.-L. J. Org. Chem., 2005, 70, 9040. 16. Fernandez de la Pradilla, R.; Alhambra, C.; Castellanos, A.; Fernandez, J.; Manzano, P.; Montero, C.; Urena, M.; Viso, A. J. Org. Chem., 2005, 70, 10693. 17.參考書:現代有機合成試劑<性質、制備和反應>;胡躍飛 付華 編著;化學工業出版社;ISBN 7-5025-8542-7
備注
暫無
表征圖譜
統計數據
共收錄化學品數據
147579 條




 滬公網安備 31010602001115號
滬公網安備 31010602001115號