硼氫化鋰 Lithium borohydride
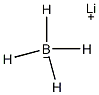
結構式
| 物競編號 | 0NFG |
|---|---|
| 分子式 | LiBH4 |
| 分子量 | 21.78 |
| 標簽 | 四氫硼酸鋰 |
編號系統
CAS號:16949-15-8
MDL號:MFCD00011088
EINECS號:241-021-7
RTECS號:ED2725000
BRN號:暫無
PubChem號:24882219
物性數據
1. 性狀:白色晶體粉末
2. 密度(g/mL,25/4℃):0.68
3. 相對蒸汽密度(g/mL,空氣=1):未確定
4. 熔點(oC):268
5. 沸點(oC,常壓):66°C/760mmHg
6. 沸點(oC,5.2kPa):未確定
7. 折射率:未確定
8. 閃點(oC):-1
9. 比旋光度(o):未確定
10. 自燃點或引燃溫度(oC):未確定
11. 蒸氣壓(kPa,25oC):未確定
12. 飽和蒸氣壓(kPa,60oC):未確定
13. 燃燒熱(KJ/mol):未確定
14. 臨界溫度(oC):未確定
15. 臨界壓力(KPa):未確定
16. 油水(辛醇/水)分配系數的對數值:未確定
17. 爆炸上限(%,V/V):未確定
18. 爆炸下限(%,V/V):未確定
19. 溶解性:溶于水,溶于低級醇,在無水乙醇和異丙醇中放置無明顯分解發生;還溶于醚、低級胺、二甘醇二甲醚,常常在這些醇和醚溶劑中使用。
毒理學數據
暫無
生態學數據
通常對水體是稍微有害的,不要將未稀釋或大量產品接觸地下水,水道或污水系統,未經政府許可勿將材料排入周圍環境。
分子結構數據
暫無
計算化學數據
1.疏水參數計算參考值(XlogP):無
2.氫鍵供體數量:0
3.氫鍵受體數量:1
4.可旋轉化學鍵數量:0
5.互變異構體數量:無
6.拓撲分子極性表面積0
7.重原子數量:2
8.表面電荷:0
9.復雜度:2
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:2
性質與穩定性
1.常溫常壓下穩定
避免的物料:水分/潮濕 酸 熱 酸 堿 胺 鹵素 氨
2.分解溫度380℃。它在熔點溫度下會緩慢地分解而放出氫氣,但在低于熔點的溫度下它是穩定的。它能溶解在正脂肪醚、環醚和多元醇醚中,并且同這些醚類生成醚合物(類似于鹵化鋰的性質)。
3.試劑的溶液、尤其是固體容易燃燒,固體還有可能會發生粉塵爆炸。建議在氮氣的保護下隔絕水氣保存,在通風櫥中操作和使用。
貯存方法
常溫密閉避光,通風干燥惰性氣體下。
合成方法
1.第一個堿金屬硼氫化物LiBH4是Schlessinger在1940年制備出來的,他們通過氫化鋰和乙硼烷的反應合成了這個化合物。不過在工業上它總是通過硼氫化鈉和氯化鋰的交換反應來合成的。異丙胺是這個反應的最合適溶劑。除去了異丙胺之后用乙醚進行一次萃取,即得到產率為75%和純度為97%~98%的硼氫化鋰。
用途
硼氫化鋰 (LiBH4) 是有機化學中最重要的還原劑之一,屬于硼氫化合物家族的成員。鋰的金屬性比鈉和鉀弱,因而在有機溶劑中比NaBH4和KBH4 有較好的溶解度。硼氫化鋰的還原能力比NaBH4和KBH4強,但是可以通過使用不同的溶劑來調控,次序大致為Et2O > THF > i-PrOH。加入鋰鹽或者叔胺可以增加它的反應速度,但NaBH4和KBH4沒有這種效應。它的還原能力比LiAlH4弱,但具有較好的化學選擇性。
該試劑基本完全覆蓋了NaBH4和KBH4 的還原功能,甚至可以在低溫下來完成。由于在低溫下反應增加了試劑的可控性,因此LiBH4常常被用于一些具有特殊要求的羰基還原或者環氧還原[1~4]。例如:1,3-氨基醇或者1,3-羥基醚等 (式1,式2)[3,4]。

LiBH4與同類試劑最大的差異,或者說最重要的用途是將酯基還原成為相應的醇。雖然LiAlH4也可以完成該過程,但是LiBH4在酯基還原過程中具有非常好的選擇性,羧酸、羧酸鹽、氰基和N,N′-二取代酰胺均不受到影響 (式3,式4)[5~8]。
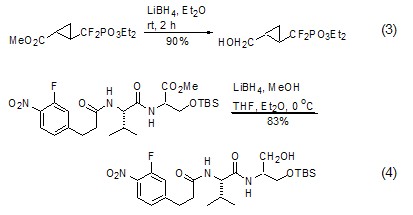
LiBH4 與環酰胺需要在溶劑中長時間回流才能將酰基部分還原為醇[9],但對二酰亞胺的還原卻非常容易。如果使用手性環狀酰胺作為輔助試劑與羧酸反應生成二酰亞胺結構,待完成手性輔助任務后,使用LiBH4不僅可以方便地切除輔助試劑,而且直接得到相應的醇 (式5,式6)[10~12]。

安全信息
危險運輸編碼:UN 3399 4.3/PG 1
危險品標志: 很易燃
很易燃  有毒
有毒  腐蝕
腐蝕
安全標識:S26 S43 S45 S36/S37/S39
危險標識:R11 R34 R20/21/22 R23/24/25 R14/15
文獻
1. Lynch, J. E.; Choi, W.-B.; Churchill, H. R. O.; Volante, R. P.; Reamer, R. A.; Ball, R. G. J. Org. Chem., 1997, 62, 9223. 2. Bartoli, G.; Bellucci, M. C.; Bosco, M.; Dalpozzo, R.; Marcantoni, E.; Sambri, L. Tetrahedron Lett., 1999, 40, 2845. 3. Yoshimatsu, M; Naito, M; Shimizu, H; Muraoka, O; Tanabe, G; Kataoka, T. J. Org. Chem., 1996, 61, 8200. 4. Blaskovich, M. A.; Evindar, G.; Rose, N. G. W.; Wilkinson, S.; Luo, Y.; Lajoie, G. A. J. Org. Chem., 1998, 63, 3631. 5. Laib, T.; Zhu, J. Synlett, 2000, 1363. 6. Yokomatsu, T.; Abe, H.; Yamagishi, T.; Suemune, K.; Shibuya, S. J. Org. Chem., 1999, 64, 8413. 7. Bharathi, P.; Zhao, H.; Thayumanavan, S. Org. Lett., 2001, 3, 1961. 8. Liao, L.; Zhang, F.; Yan, N.; Golen, J. A.; Fox, J. M. Tetrahedron, 2004, 60, 1803. 9. Snider, B. B.; Ahn, Y.; O'Hare, S. M. Org. Lett., 2001, 3, 4217. 10. atsunaga, H.; Ishizuka, T.; Kunieda, T. Tetrahedron, 1997, 53, 1275. 11. Pilli, R. A.; Riatto, V. B.; Vencato, I. Org. Lett., 2000, 2, 53. 12. Wu, Y.; Shen, X.; Yang, Y.; Hu, Qi; Huang, J. J. Org. Chem., 2004, 69, 3857. 13.參考書:現代有機合成試劑<性質、制備和反應>;胡躍飛 付華 編著;化學工業出版社;ISBN 7-5025-8542-7
備注
暫無
表征圖譜
統計數據
共收錄化學品數據
147579 條




 滬公網安備 31010602001115號
滬公網安備 31010602001115號