氧化鋁 Alumina oxide

結構式
| 物競編號 | 098A |
|---|---|
| 分子式 | Al2O3 |
| 分子量 | 101.96 |
| 標簽 | 三氧化二鋁, 鋁氧, Alumina, γ-Alumina, 脫水吸附劑, 催化劑, 膠黏劑, 拋光劑, 研磨劑, 陶瓷封裝用材料 |
編號系統
CAS號:1344-28-1
MDL號:MFCD00003424
EINECS號:215-691-6
RTECS號:BD1200000
BRN號:暫無
PubChem號:暫無
物性數據
1. 性狀:白色粉末
2. 密度(g/mL,25/4℃):3.5-3.9
3. 相對蒸汽密度(g/mL,空氣=1):未確定
4. 熔點(oC):2045
5. 沸點(oC,常壓):未確定
6. 沸點(oC,5.2kPa):2980
7. 折射率:未確定
8. 閃點(oC):未確定
9. 比旋光度(o):未確定
10. 自燃點或引燃溫度(oC):未確定
11. 蒸氣壓(kPa,25oC):未確定
12. 飽和蒸氣壓(kPa,60oC):未確定
13. 燃燒熱(KJ/mol):未確定
14. 臨界溫度(oC):未確定
15. 臨界壓力(KPa):未確定
16. 油水(辛醇/水)分配系數的對數值:未確定
17. 爆炸上限(%,V/V):未確定
18. 爆炸下限(%,V/V):未確定
19. 溶解性:不溶于水、醇、和醚,微溶于堿和酸。
毒理學數據
主要的刺激性影響:
在皮膚上面:可能引起發炎。
在眼睛上面:可能引起發炎
致敏作用:沒有已知的敏化作用。
生態學數據
對是水稍微有危害的不要讓未稀釋或大量的產品接觸地下水、水道或者污水系統,若無政府許可,勿將材料排入周圍環境。
分子結構數據
1、摩爾折射率:無可用的
2、摩爾體積(cm3/mol):無可用的
3、等張比容(90.2K):無可用的
4、表面張力(dyne/cm):無可用的
5、介電常數:無可用的
6、極化率(10-24cm3):無可用的
7、單一同位素質量:101.94782 Da
8、標稱質量:102 Da
9、平均質量:101.9613 Da
計算化學數據
1、 氫鍵供體數量:0
2、 氫鍵受體數量:3
3、 可旋轉化學鍵數量:0
4、 拓撲分子極性表面積(TPSA):43.4
5、 重原子數量:5
6、 表面電荷:0
7、 復雜度:34.2
8、 同位素原子數量:0
9、 確定原子立構中心數量:0
10、 不確定原子立構中心數量:0
11、 確定化學鍵立構中心數量:0
12、 不確定化學鍵立構中心數量:0
13、 共價鍵單元數量:1
性質與穩定性
1.如果遵照規格使用和儲存則不會分解,未有已知危險反應,避免氧化物。
2.用氧化鋁纖維強化金屬時,與金屬的溶合性良好。另外,對金屬不引起化學反應,是理想的金屬強化纖維。氧化鋁纖維是多晶耐火纖維的一個重要品種。氧化鋁纖維導熱率、加熱收縮率和熱容量都較低。具有耐高溫、高熱的特性,長期使用溫度為1300~1400℃,高于普通硅酸鋁纖維(1000~1100℃),其最高使用溫度為1500~1700℃。與碳纖維、碳化硅纖維等非氧化物纖維相比,氧化鋁纖維不僅具有高強度、高模量、耐高溫等優良性能,而且還有很好的高溫抗氧化性、耐腐蝕性和電絕緣性。可在酸性環境、氧化氣氛、還原氣氛和真空條件下使用,對堿性環境也有一定耐蝕性,但易受鉛蒸氣和五氧化二釩的侵蝕。
3.易吸水但不潮解。為兩性化合物。
4.能夠導致呼吸困難,最好在通風櫥中進行操作,在干燥和惰性條件下存儲。
貯存方法
應貯存于干燥、通風庫房中,嚴防受潮。
合成方法
(1)其制備方法有酸法,堿法和醇鋁法三種。目前國內主要采用堿法,少數廠家采用醇鋁法。
酸法將硫酸鋁配成6%的水溶液,加入中和槽中,再將液氨配成15%~20%的氨水,按計算量將氨水快速加入,在強烈攪拌下于室溫反應40~60 min,至pH值達到8~9左右時,反應基本完成。將生成的沉淀物經壓濾、用無離子水洗滌除去雜質離子,洗滌水中一般加少量氨水調節pH值為8~9,以防洗滌過程中氫氧化鋁發生膠凝過程而引起物料損失。將洗滌過的沉淀物加入少量33%的硝酸溶液,在強烈攪拌下生成膠狀料漿(此過程稱為打漿)。再經噴霧干燥,將得到的微球形氫氧化鋁擠條成型,在550℃下焙燒活化4h,即脫水形成活性氧化鋁。其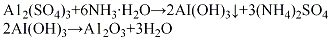
(2)堿法把工業固體燒堿加水配成濃度為600 g/L的燒堿溶液,在50~80℃下加入氫氧化鋁后升溫至110℃,保溫3 h進行反應,將所得溶液用水稀釋至含氧化鋁為100g/L,靜置0.5~1h,經過濾,除去氫氧化鐵等不溶性雜質,再將清液和20%硝酸溶液按照一定比例進行中和反應,溫度控制在30~50℃下,控制pH 7~7.5,反應10 min 左右以后,再將反應液在常溫攪拌下老化2h,經過濾、用無離子水多次洗滌、于110℃烘干、擠條成型、干燥、500℃活化4h,制得活性氧化鋁。其
(3)醇鋁法將金屬鋁片加入異丙醇溶液中進行反應,生成異丙醇鋁,通過水蒸氣鼓泡(入口溫度180℃,水解溫度175℃),使異丙醇鋁水解,生成水合氧化鋁,經熟化、過濾、于100℃干燥、500℃脫水活化,制得活性氧化鋁。其
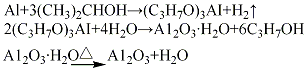
(4)高溫快脫法:將氫氧化鋁(水合氧化鋁)經高溫快速脫水、成型、水熱處理及干燥后制得成品。
(5)炭化鋁膠法:將氫氧化鋁和氫氧化鈉混合,再經中和、二氧化碳碳化、水洗、壓濾、干燥、粉碎、捏合、擠條、干燥、煅燒等過程制得成品。
(6)噴霧干燥法:將氫氧化鋁與工業硫酸反應,再經堿液中和、水洗、噴霧干燥、煅燒等過程制得成品。
(7)油柱成型法:將鋁錠用工業鹽酸溶解,再經油柱成球、水洗、干燥、煅燒等過程制得成品。
制備過程中各種條件,特別是沉淀條件對產品的晶型、表面積、孔結構等影響很大,一般地,低溫、低 pH 值下易得到無定形氫氧化鋁及擬薄水鋁石,高 pH 值易生成三水鋁石。擬薄水鋁石在 430~500℃下,煅燒得到γ-Al2O3,β三水鋁石在 300℃煅燒得到 η-Al2O3。
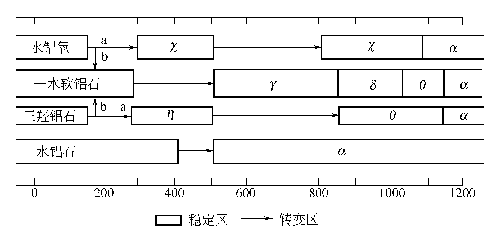
圖XIII-14 氫氧化鋁的脫水途徑
(8)高純銨明礬熱解法以硫酸鋁、硫酸銨為原料合成銨明礬(硫酸鋁銨),經脫水、熱解生成氧化鋁,再經轉相制得γ-,α-氧化鋁。
利用有機鋁化合物聚合生成黏稠的聚鋁氧烷溶液,將聚鋁氧烷溶液進行干式紡絲,得到有機鋁化合物纖維,再經煅燒制得氧化鋁纖維。
使有機鋁化合物聚合,生成黏稠的聚鋁氧烷溶液,將其利用普通的干式紡絲法,制成有機鋁化合物纖維。再經煅燒制得氧化鋁纖維。
9.制法 方法1.用蒸餾水溶解結晶硫酸鋁,然后在不斷攪拌下慢慢加入硫酸銨溶液,制得硫酸鋁銨:
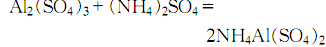
然后加熱至100~200℃,除去結晶水后,研成粉末進行高溫灼燒,開始在800℃ 灼燒,然后升溫至1250~1300℃灼燒4h,冷卻后即得氧化鋁:
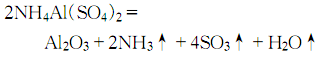
用途
1.用作催化劑和催化劑載體,是石油煉制和石油化工中主要的催化劑和載體。還用作空氣及其他氣體的脫濕劑,變壓器油和透平油的脫酸劑。
2.用于鍛造的加熱爐、均熱爐等工業用的高溫爐。可作密封材料和填充材料。還可作強化用補強纖維,窯爐的爐襯,電子元件(IC板、鐵氧體)的煅燒爐等。
3.氧化鋁纖維主要用于高溫絕熱材料和增強復合材料。氧化鋁短纖維具有突出的耐高溫性能,可與樹脂、金屬或陶瓷進行復合制備高性能復合材料,制造加熱爐、窯爐襯里及電子元件煅燒爐等工業用高溫爐。由于其密度小。絕熱性好、熱容量小,不僅可以減輕爐體質量,而且可以提高控溫精度,節能效果顯著。氧化鋁纖維在高溫爐中的節能效果比一般的耐火磚或高溫涂料好。將其用于增強金屬時,與金屬完全不起化學作用,耐腐蝕性好,因此氧化鋁纖維是金屬的增強纖維。還可用于編織無紡布、編織帶、繩索等各種形狀的纖維制品。
4.用于制造加熱爐、均熱爐等工業用高溫爐。用作密封材料、填充材料、FRM用增強纖維、窯爐襯里及電子元件(IC基板、鐵氧體)煅燒爐等。
5.主要用作化纖纖維填料,也用于化妝品磨面膏的磨面劑、牙膏摩擦劑及冶金和化學品中。
6.分析試劑,有機溶劑的脫水吸附劑,研磨劑,低熔點鉛玻璃的配制。
7.氧化鋁是色譜中最常用的一種填充材料,有酸性、堿性和中性。是一種能進行催化脫水、消除、加成、縮合、環氧化物開環、氧化和還原反應的試劑,對于均相反應來說反應條件通常更溫和、更具有選擇性[1]。
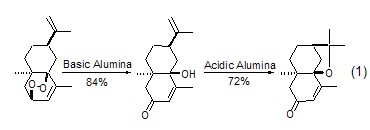
加成與縮合反應 無論是親電反應還是親核反應,氧化鋁都可促進各類雜原子的加成反應。氧化鋁也能使羥基和烷氧基發生分子內加成生成相應的烯烴 (式1)[2]。
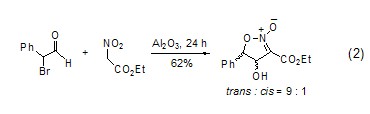
在氧化鋁的作用下,醛和不同活性的亞甲基化合物之間的醇醛縮合反應、Michael反應和Wittig反應常在無溶劑、溫和的條件下進行。硝基醇醛環化生成2-異唑啉的2-氧化物的反應具有很好的立體選擇性 (式2)[3]。
氧化鋁有利于Diels-Alder反應、烯烴反應和Carroll重排等受軌道對稱性控制的反應。這些反應條件溫和且有很高的立體選擇性。
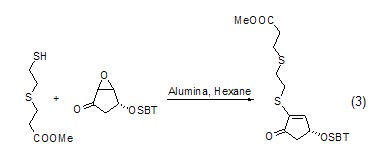
在Al2O3的作用下,S可與環氧丙烷更易進行親核加成反應,而后脫水形成烯 (式3)[4]。
以氧化鋁為固相載體微波照射后反應物中的S、Se和Te可以與炔進行親核加成,產物為α,β-不飽和酯 (式4)[5]。
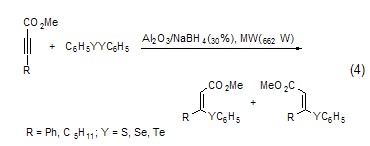
環氧化反應 在溫和的、選擇性的條件下,用醇、硫醇、硒醇、胺、羧酸和過氧化物等親核試劑可以使環氧化物發生開環反應。這種方法可用于順烯胺的合成 (式5)[6]。

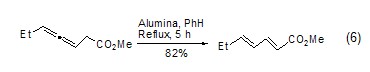
氧化鋁可催化許多重排反應。活性的氧化鋁使O-磺酰肟發生Beckmann重排生成預期的酰胺,而堿性的氧化鋁生成相應的唑啉。在氧化鋁作用下,β,γ-不飽和酮可異構化為共軛酮、炔烴異構化成烯烴、烯烴異構化成共軛雙烯醇化 (式6)[7]。
氧化鋁可促進伯醇乙酸酯水解作用、酰亞胺的脫酰作用、磺酰肟的水解作用和β-酮酸酯和氨基甲酸鹽的脫烷氧羰基化作用[8]。
安全信息
危險運輸編碼:暫無
危險品標志:暫無
安全標識:暫無
危險標識:暫無
文獻
1. Posner, G. H. Angew. Chem., Int. Ed., 1978, 17, 487. 2. McPhail, A. T.; Onan, K. D. Tetrahedron Lett., 1973, 4641. 3. Rosini, G.; Galarini, R.; Marotta, E.; Righi, E. P. J. Org. Chem., 1990, 55, 781. 4. Maruyama, T.; Asada, M.; Shiraishi, T.; Egashira, H.; Yoshida, H.; Maruyama, T.; Ohuchida, S.; Nakai, H.; Kondo, K.; Toda, M. Bio. Med. Chem., 2002, 10, 975. 5. Perin, G.; Jacob, R. G.; de Azambuja, F.; Botteselle, G. V.; Siqueira, G.M.; Freitag, R. A.; Lenardao, E. J. Tetrahedron Lett., 2005, 46, 1679. 6. Hudrlik, P. F.; Hudrlik, A. M.; Kulkarni, A. K. Tetrahedron Lett., 1985, 26, 139. 7. Tsuboi, S.; Matsuda, T.; Mimura, S.; Takeda, A. Org. Synth.Chem., 1993, 8, 251. 8. (a) Greene, A. E.; Crabbé, P. Tetrahedron Lett., 1976, 2707. (b) van Leusen, A. M.; Strating, J. Org. Synth. Chem., 1988, 6, 981. 9.參考書:現代有機合成試劑<性質、制備和反應>;胡躍飛 付華 編著;化學工業出版社;ISBN 7-5025-8542-7
備注
曾用CAS:1302-74-5
表征圖譜
統計數據
共收錄化學品數據
147579 條




 滬公網安備 31010602001115號
滬公網安備 31010602001115號