三溴化硼 Boron tribromide
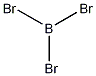
結構式
| 物競編號 | 0KW3 |
|---|---|
| 分子式 | BBr3 |
| 分子量 | 250.57 |
| 標簽 | 溴化硼, 晶堿石, 絲光晶堿石, 碳酸鈉石, 三溴硼烷, 催化劑, 溴化劑 |
編號系統
CAS號:10294-33-4
MDL號:MFCD00011312
EINECS號:233-657-9
RTECS號:ED7400000
BRN號:暫無
PubChem號:暫無
物性數據
1.性狀:無色或稍帶黃色的發煙液體,有強烈的刺激性臭味。[8]
2.熔點(℃):-46[9]
3.沸點(℃):90~91.2[10]
4.相對密度(水=1):2.65[11]
5.飽和蒸氣壓(kPa):5.33(14℃)[12]
6.辛醇/水分配系數:1.43[13]
7.溶解性:溶于四氯化碳、二氧化硫(液體)、二硫化碳。[14]
毒理學數據
1.急性毒性 暫無資料
2.刺激性 暫無資料
生態學數據
該物質對環境可能有危害,對水體應給予特別注意。
分子結構數據
1、摩爾折射率:28.67
2、摩爾體積(cm3/mol):90.0
3、等張比容(90.2K):225.5
4、表面張力(dyne/cm):39.3
5、介電常數:無可用的
6、極化率(10-24cm3):11.36
7、單一同位素質量:247.764296 Da
8、標稱質量:248 Da
9、平均質量:250.523 Da
計算化學數據
1.疏水參數計算參考值(XlogP):無
2.氫鍵供體數量:0
3.氫鍵受體數量:0
4.可旋轉化學鍵數量:0
5.互變異構體數量:無
6.拓撲分子極性表面積0
7.重原子數量:4
8.表面電荷:0
9.復雜度:8
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:1
性質與穩定性
1.易被水和醇等分解,受熱會爆炸,對人體組織有強烈刺激作用,其蒸氣劇毒,腐蝕性較強,具有強吸水性,見光、遇熱易分解,接觸空氣冒白煙。為強路易式酸,能與堿反應形成絡合物和加成物。
2.在干燥空氣中不變化。溶于無機酸并劇烈起泡。天然堿產于不同的鹽湖沉積物中,主要產于堿湖及古代沉積礦床中,常與針碳鈉鈣石、水堿、泡堿、石鹽、芒硝、鈣芒硝、無水芒硝和石膏共生。遇空氣中的濕氣很容易水解。
3.穩定性[15] 穩定
4.禁配物[16] 堿類、水、醇類
5.避免接觸的條件[17] 受熱、潮濕空氣、光照
6.聚合危害[18] 不聚合
貯存方法
儲存注意事項[19] 儲存于陰涼、干燥、通風良好的庫房。遠離火種、熱源。包裝必須密封,切勿受潮。應與堿類、醇類等分開存放,切忌混儲。不宜久存,以免變質。儲區應備有泄漏應急處理設備和合適的收容材料。
合成方法
1.直接合成法 將干燥的元素硼粉裝入管式反應爐的反應管中,為使反應能充分進行,反應管內應放入一定量的填料,填料材質與管壁同。將反應管加熱至850℃,另外將溴素在溴釜中也同時加熱至微沸,然后通人反應管。反應生成的溴化硼液體在脫溴器中與活性炭、鋅粉和鋁屑共同加熱回流至生成的溴化硼為無色為止,再經粗餾、精餾,制得完全無色的溴化硼成品。其反應方程式如下: 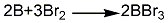
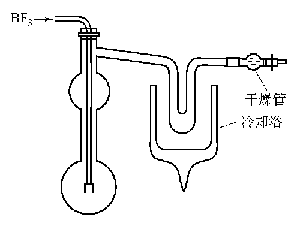 圖XIII-10 三氯化硼的制備裝置
圖XIII-10 三氯化硼的制備裝置

圖XIII-11 三氯化硼的合成裝置
2.用三氟化硼制備。可以使用圖所示的裝置。1L圓底燒瓶用一根直徑約30mm、長25cm的玻璃管與500mL蒸餾燒瓶的底熔接在一起。三氟化硼的進料管通過軟木塞插到蒸餾燒瓶之中,并延伸到大燒瓶的中央。500mL燒瓶是為避免大量三氯化鋁與三氯化硼一起升華,起著冷凝器的作用。蒸餾燒瓶上有支管與U形管連接,U形管用干冰甲醇冷卻,在U形管的出口裝有干燥管。在反應燒瓶中裝入67g無水三氯化鋁(0.5mol)。將BF3發生裝置通過硫酸洗氣瓶與反應燒瓶連接起來。發生裝置必須是足以發生132g(2mol)BF3的才行。BF3的流速大約為30min通過2mol的氣體。在裝置內通入BF3將空氣逐出以后,用小火焰慢慢地加熱裝有三氯化鋁的反應燒瓶。當溫度上升時,反應立即開始,繼續加熱,再用兩個加熱器強烈加熱兩個燒瓶,使產物從反應混合物中分離出來,直到三氯化硼全部蒸餾出來為止。分離出生成的三氯化硼后,加熱時,則三氟化鋁就成為白色粉末,從燒瓶器壁上剝落下來。三氯化硼則集聚在U形管中。反應結束以后,將U形管取下密封。可用蒸餾法進行提純。可得47g產品(80%)。
3.用KBF4制備。可用制法1的裝置,以KBF4代替BF3。用133g無水三氯化鋁(1mol)及62g KBF4(05mol),用油浴加熱4h,緩緩地使溫度從150℃上升至175℃。生成的三氯化硼用液氮冷凝,再進行蒸餾。可得30g產品(對KBF4而言,收率為52%)。
用途
1.重要的工業原料,廣泛用于玻璃、化工、輕工、紡織、漂染、冶金、石油加工、醫藥、食品等方面。燒堿主要用于人造纖維、造紙、染料、肥皂、塑料、醫藥、農藥等方面。小蘇打主要用于食品、塑料、橡膠、醫藥、印染、鞣革、農業浸種等領域。
2.用作半導體的摻雜材料,有機合成的催化劑、中間體和溴化劑。是制造高純硼及其他有機硼化合物的原料。
3.是一種用途廣泛的合成試劑,用作有機合成的催化劑和溴化劑,也是制造高純硼及其它有機硼化合物的原料。溴化硼可以參與促進醚鍵、胺鍵、硫醇鍵的斷裂反應,以及丙二烯、炔烴等化合物的加成反應等。它也可以用于醫藥化學領域[1],天然產物化學領域[2]及新材料等領域。
溴化硼易于和C-O鍵反應生成烷氧基硼化物和溴代烴,水解后得到相應的醇類產物。尤其在芳甲醚的斷裂反應中,溴化硼的活性明顯高于其它試劑。多取代的芳環醚化合物分別和溴化硼反應可以高收率得到相應酚類物質 (式1[3],式2[4])。
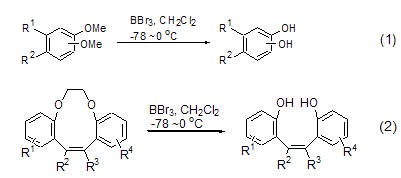
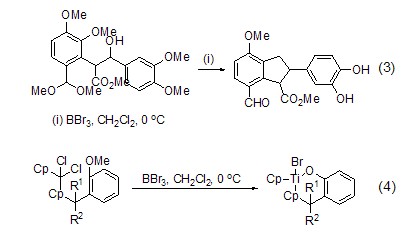
溴化硼在斷裂醚鍵后生成的溴代烴也可以發生分子內環合反應形成環化物。如多取代芳醚化合物和溴化硼反應后生成苯并呋喃類衍生物 (式3)[5];二茂鈦化合物和溴化硼反應形成鈦雜環化物 (式4)[6],該反應實際是首先發生鹵素交換反應,然后分子內消除反應關環而成。該反應可用于合成系列天然產物分子中的骨架結構。
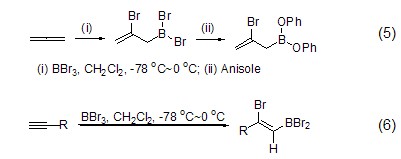
溴化硼很容易和丙二烯、炔烴等化合物進行加成反應。它和丙二烯反應得到 (2-溴烯丙基)二溴硼烷 (式5)[7],該化合物再和苯甲醚反應得到取代二苯氧基硼烷。溴化硼和炔烴通常進行順式加成反應得到高度立體選擇性的產物 (式6)[7]。
4.用于有機硼化合物和高純硼的制取,也用作半導體的摻雜材料,有機合成的催化劑、溴化劑等。[20]
安全信息
危險運輸編碼:UN 2692 8/PG 1
危險品標志: 極毒
極毒  腐蝕
腐蝕
安全標識:S9 S26 S28 S45 S36/S37/S39
文獻
1. Lisowski, V.; Léonce, S.; Kraus, L. B.; Sopková, O. S.; Pierré, A.; Atassi, G.; Caignard, D.; Renard, P.; Rault, S. J. Med. Chem., 2004, 47, 1448. 2. Brimble, M. A.; Brenstrum, T. J. J. Chem. Soc., Perkin Trans 1, 2001, 1624. 3. Barluenga, J.; Aznar, F.; Palomero, M. A. J. Org. Chem., 2003, 68, 537. 4. Mayekar, N. V.; Chattopadhyay, S.; Nayak, S. K. Synthesis, 2003, 2041. 5. Detterbeck, R.; Hesse, M. Helv. Chim. Acta., 2003, 86, 343. 6. Qian, Y.; Huang, J.; Ding, K.; Zhang, Y.; Huang, Q.; Chen, X.; Chan, A.; Wong, W. J. Organomet. Chem., 2002, 645, 59. 7. Hara, S.; Suzuki, A. Tetrahedron Lett., 1991, 32, 6749. [1~7]參考書:現代有機合成試劑<性質、制備和反應>;胡躍飛 付華 編著;化學工業出版社;ISBN 7-5025-8542-7 [8~20]參考書:危險化學品安全技術全書.第一卷/張海峰主編.—2版.北京;化學工業出版社,2007.6 ISBN 978-7-122-00165-8
備注
暫無
表征圖譜
統計數據
共收錄化學品數據
147579 條




 滬公網安備 31010602001115號
滬公網安備 31010602001115號