氯化銅 Copper(II) chloride
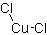
結構式
| 物競編號 | 0JS1 |
|---|---|
| 分子式 | CuCl2 |
| 分子量 | 134.45 |
| 標簽 | 媒染劑, 氧化劑, 防腐劑, 食品添加劑, 消毒劑 |
編號系統
CAS號:7447-39-4
MDL號:MFCD00010972
EINECS號:231-210-2
RTECS號:暫無
BRN號:暫無
PubChem號:24845369
物性數據
1. 性狀:黃色或黃褐色的、具有潮解性的結晶性粉末。
2. 密度(g/mL,25/4℃): 3.386
3. 相對蒸汽密度(g/mL,空氣=1):無可用
4. 熔點(oC):620
5. 沸點(oC,常壓):993
6. 沸點(oC,5.2kPa): 無可用
7. 折射率: 無可用
8. 閃點(oC): 無可用
9. 比旋光度(o):無可用
10. 自燃點或引燃溫度(oC):無可用
11. 蒸氣壓(kPa,25oC):無可用
12. 飽和蒸氣壓(kPa,60oC):無可用
13. 燃燒熱(KJ/mol):無可用
14. 臨界溫度(oC):無可用
15. 臨界壓力(KPa):無可用
16. 油水(辛醇/水)分配系數的對數值:無可用
17. 爆炸上限(%,V/V):無可用
18. 爆炸下限(%,V/V): 無可用
19. 溶解性:溶于醇、丙酮和醚。
毒理學數據
1 。
試驗方法:腹腔
攝入劑量: 7400微克/千克
測試對象:嚙齒動物-鼠
毒性類型:急性
毒性作用:詳細的毒副作用沒有報告以外的其他致死劑量值
2 。
試驗方法:靜脈
攝入劑量: 1.75萬微克/千克
測試對象:嚙齒動物-鼠
毒性類型:急性
毒性作用: 詳細的毒副作用沒有報告以外的其他致死劑量值
3 。
試驗方法:吸入
攝入劑量: 20 ug/m3/26W-I
測試對象:嚙齒動物-鼠
毒性類型: MutipleDose
毒性作用: 1.改變白細胞(白血球)計數
2.體內的氯變化
生態學數據
該物質對環境可能有危害,對水體應給予特別注意。
分子結構數據
1、 摩爾折射率:無可用
2、 摩爾體積(cm3/mol): 無可用
3、 等張比容(90.2K):無可用
4、 表面張力(dyne/cm):無可用
5、 極化率:無可用
計算化學數據
1.疏水參數計算參考值(XlogP):無
2.氫鍵供體數量:0
3.氫鍵受體數量:0
4.可旋轉化學鍵數量:0
5.互變異構體數量:無
6.拓撲分子極性表面積0
7.重原子數量:3
8.表面電荷:0
9.復雜度:2.8
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:1
性質與穩定性
1. 如果遵照規格使用和儲存則不會分解。
2. 無水氯化銅在993℃時分解為氯化亞銅;氯化銅易溶于水及乙醇,也溶于丙酮。
貯存方法
密封于陰涼干燥環境。
合成方法
1.將純的二水合氯化銅CuCl2·2H2O用稀鹽酸重結晶,以除去其中的堿式鹽。然后將其放在干燥的氯化氫氣流中,于140~150℃下脫水,直至重量不再減少時為止。將所得無水物置于盛有濃硫酸和氫氧化鈉的干燥器中,以除去附著在晶體上的氯化氫。
用途
1.用作媒染劑、氧化劑、木材防腐劑、食品添加劑、消毒劑等,也用于石油餾分的脫臭和脫硫、金屬提煉、照相等。
2.氯化銅可以作為氯化試劑、氧化試劑和路易斯酸試劑。
氯化銅是一個對多種官能團化合物有效的氯化試劑,能實現羰基化合物如丁醛的α-氯化反應。反應通常在含氯化鋰的極性溶劑中進行。當反應在質子溶劑如甲醇中進行時,則得到α-氯化二甲基乙羧醛 (式1)[1]。
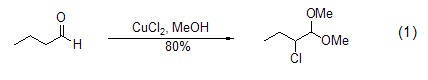
氯化銅也能實現芳香環化合物的氯化反應,如在四氯化碳中作用于苯酚或烷氧基苯化合物實現鄰位或對位的氯化反應 (式2)[2]。
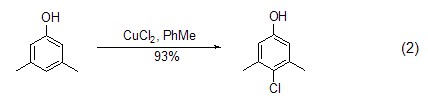
含活潑亞甲基的化合物如9-烷氧基-10-甲基蒽與氯化銅反應能得到偶聯產物 (式3),然而結構相似的9-烷基-芐基蒽在氯化銅作用下則發生自由基反應得到10-苯亞甲基蒽 (式4)[3]。
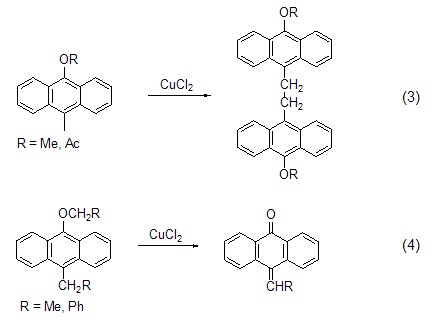
酮或酯在二異丙基氨基鋰LDA作用下得到的鋰化烯醇式結構能被氯化銅氧化為1,4-二羰基化合物。如叔丁基甲基酮和苯乙酮在LDA和氯化銅作用下發生交叉偶聯反應 (式5)[4]。
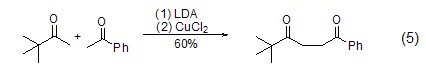
氯化銅能催化β-二羰基化合物對芳基偶氮烯烴的1,4-加成反應,得到相應的吡咯衍生物 (式6)[5]。此外,氯化銅還能催化水、醇和芳香胺對芳基偶氮烯烴的加成反應 (式7)[6]。
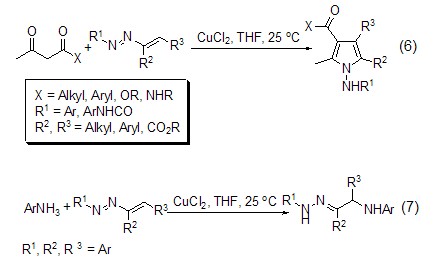
在氧氣存在下,氯化銅能氧化苯酚為苯醌化合物。如在CuCl2/胺/O2催化下將2,3,6-三甲基苯酚轉換為三甲基對苯醌 (式8)[7]。此外,烷氧基苯酚,甚至苯并唑也能被氯化銅和氯化鐵體系氧化 (式9)[8]。
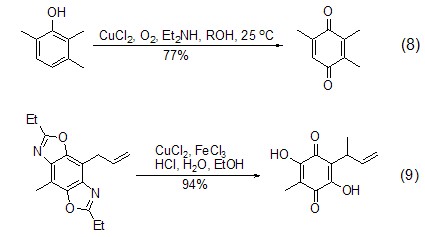
氯化銅和胺形成的配合物能有效催化2-萘酚的氧化偶聯反應,得到對稱的1,1' -二萘基-2,2'-二酚 (式10)[9]。
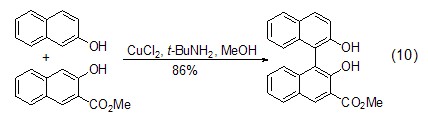
除了胺配體外,烷氧基配體也能與氯化銅作用實現萘酚的氧化偶聯,并且選擇不同的配體和控制氯化銅與配體的比例能選擇性實現底物的自身偶聯或交叉偶聯反應。如在芐胺配體存在下實現萘酚與萘胺的交叉偶聯反應 (式11)[10]。
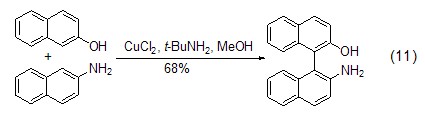
氯化銅還能催化烷基和芳基磺酰氯對不飽和鍵的加成反應,如苯磺酰氯與烯烴在氯化銅和堿作用下發生加成反應得到乙烯基砜 (式12)[11],苯磺酰氯與苯乙炔在氯化銅和不同添加劑作用下得到順式或反式β-氯乙烯基砜的反應 (式13)[12]。
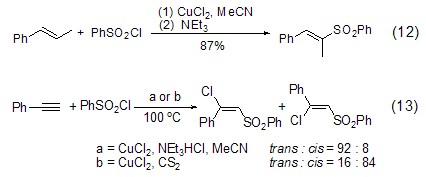
氯化銅還能與鈀配合物反應,如π-烯丙基鈀配合物在氯化銅作用下發生氧化斷裂反應,釋放出氯化鈀,同時得到烯丙基氯化合物(式14)[13]。這種氯化銅對鈀配合物的作用可用于實現烯丙基化合物的二聚反應,如1,5-二亞甲基環辛烷在氯化鈀和氯化銅作用下發生關環反應 (式15)[14]。
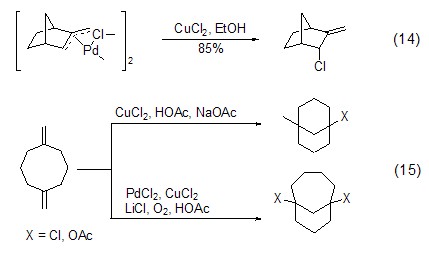
此外,氯化銅還能作為鈀試劑催化反應中的氧化劑,將還原消除反應后得到的低價鈀試劑重新氧化為Pd(II) 進入催化循環,從而實現催化反應 (式16)[15]。
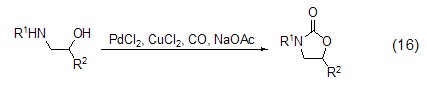
安全信息
危險運輸編碼:UN 3264 8/PG 3
危險品標志: 危害環境
危害環境
安全標識:S61
危險標識:R51/53
文獻
Gastro, C. E.; Gaughan, E. J.; Owsley, D. C. J. Org. Chem., 1965, 30, 587. 2. Crocker, H. P.; Walser, R. Chem. Commun., 1970, 1982. 3. Nonhebel, D. C.; Russell, J. A.Tetrahedron, 1970, 26, 1123. 4. Ito, Y.; Konoike, T.; Tarada, T.; Saegusa, T. J. Am. Chem. Soc., 1977, 99, 1487. 5. Attansi, O.; Santeusanio, S. Synthesis, 1983, 742. 6. Attansi, O.; Filippone, P. Synthesis, 1984, 422. 7. Shimizu, M. Watanabe, Y. Orita, H.; Hayakawa, T.; Takehira, K. Bull. Chem. J., 1992, 65, 1522. 8. Hegedus, L. S.; Odle, R. R.; Winton, P. M; Weider, P. R. J. Org. Chem., 1982, 47, 2607. 9. Brussee, J.; Groenendijk, J. L. G.; Koppele, J. M.; Jansen, A. C. A. Tetrahedron, 1985, 41, 3313. 10. Smrcina, M.; Lorenc, M.; Hanus, V.; Kocovky, P. Synlett, 1991, 231. 11. Asscher, M.; Vofsi, D. J. Chem. Soc., 1964, 4962. 12. Amiel, Y. Tetrahedron Lett., 1971, 661. 13. Castanet, Y.; Petit, F. Tetrahedron Lett., 1979, 34, 3221. 14. Heumann, A.; Reglier, M.; Waegell, B. Tetrahedron Lett., 1983, 24, 1971. 15. Tam, W. J. Org. Chem., 1986, 51, 2977.
備注
暫無
表征圖譜
統計數據
共收錄化學品數據
147579 條




 滬公網安備 31010602001115號
滬公網安備 31010602001115號