乙二胺 Ethylenediamine
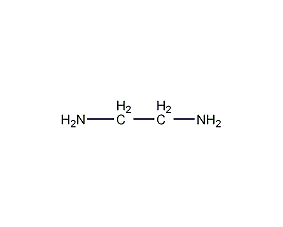
結構式
| 物競編號 | 02UT |
|---|---|
| 分子式 | C2H8N2 |
| 分子量 | 60.12 |
| 標簽 | 1,2-乙二胺, 1,2-二氨基乙烷, 二氨基乙烷, 1,2-亞乙基二胺, 亞乙基二胺, 1,2-Diaminoethane, 1,2-Ethanediamine, DAE, EDA |
編號系統
CAS號:107-15-3
MDL號:MFCD00008204
EINECS號:203-468-6
RTECS號:KH8575000
BRN號:605263
PubChem號:24894420
物性數據
1.性狀:無色或微黃色黏稠液體,有類似氨的氣味。[10]
2.pH值:11.9(25%溶液,25℃)[11]
3.熔點(℃):8.5[12]
4.沸點(℃):116~117.2[13]
5.相對密度(水=1):0.90(20℃)[14]
6.相對蒸氣密度(空氣=1):2.07[15]
7.飽和蒸氣壓(kPa):1.43(20℃)[16]
8.燃燒熱(kJ/mol):-1891.9[17]
9.臨界壓力(MPa):6.48[18]
10.辛醇/水分配系數:-2.04~-1.2[19]
11.閃點(℃):33.9(OC);43.3(CC)[20]
12.引燃溫度(℃):385[21]
13.爆炸上限(%):16.6[22]
14.爆炸下限(%):2.7[23]
15.溶解性:溶于水、乙醇,不溶于苯,微溶于乙醚。[24]
16.黏度(mPa·s,15oC):1.722
17.黏度(mPa·s,25oC):1.54
18.黏度(mPa·s,30oC):1.226
19.閃點(oC,閉口):43.3
20.閃點(oC,開口):33.9
21.蒸發熱(KJ/mol,20oC):46.89
22.熔化熱(KJ/mol):19.34
23.生成熱(KJ/mol):-26.63
24.比熱容(KJ/(kg·K),30oC,定壓):2.95
25.溶解熱(J/mol,15oC):1.82
毒理學數據
1.急性毒性[25]
LD50:1298mg/kg(大鼠經口);730mg/kg(兔經皮)
LC50:300mg/m3(小鼠吸入)
2.刺激性[26]
家兔經皮:450mg,中度刺激(開放性刺激試驗)。
家兔經眼:675μg,重度刺激。
3.亞急性與慢性毒性[27] 大鼠反復在本品1188mg/m3下染毒,見動物脫毛及肺、腎、肝損害;在307mg/m3下連續暴露37h未見損傷。
生態學數據
1.生態毒性[28]
LC50:115.7mg/L(96h)(黑頭呆魚);230mg/L(48h)(虹鱒魚,一年生);0.88mg/L(48h)(水蚤)
IC50:0.08~0.85mg/L(72h)(藻類)
2.生物降解性[29] MITI-I測試,初始濃度100ppm,污泥濃度30ppm,4周后降解39%~94%。
3.非生物降解性[30] 空氣中,當羥基自由基濃度為5.00×105個/cm3時,降解半衰期為6h(理論)。
分子結構數據
1、摩爾折射率:18.38
2、摩爾體積(cm3/mol):68.9
3、等張比容(90.2K):169.7
4、表面張力(dyne/cm):36.8
5、極化率:7.28
計算化學數據
1.疏水參數計算參考值(XlogP):無
2.氫鍵供體數量:2
3.氫鍵受體數量:2
4.可旋轉化學鍵數量:1
5.互變異構體數量:無
6.拓撲分子極性表面積52
7.重原子數量:4
8.表面電荷:0
9.復雜度:6
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:1
性質與穩定性
1.化學性質:在空氣中放置時吸濕,或吸收二氧化碳生成氨基甲酸鹽(白色固體)。化學性質活潑,溶于水放熱,水溶液呈強堿性。與無機酸生成結晶性、水溶性的鹽。其硝酸鹽加熱時脫去2分子水,生成具有爆炸性的乙二硝胺。
2.與有機酸、酯、酸酐或酰鹵反應,生成一取代酰胺或二取代酰胺。將一取代酰胺加熱時,縮合生成2-烷基咪唑啉。與二元酸縮合生成聚酰胺樹脂。與鹵代烷反應得到一烷基或二烷基乙二胺。與丙烯腈反應,生成腈乙基化合物。與環氧化合物反應,生成加成化合物。與醛反應主要生成(Schiff)堿。與甲醛作用得到組成復雜的混合物。與氯代乙酸反應得到乙二胺四乙酸鹽(EDTA),是一種有用的螯合劑。與尿素、碳酸二乙酯、光氣或二氧化碳反應,主要生成2咪唑啉酮。在鎳、鈷或銅催化劑存在下加熱到350℃生成哌啶。與二硫化碳反應生成二硫代乙二氨基甲酸,加熱脫去硫化氫得到聚硫脲樹脂。
3.穩定性[31] 穩定
4.禁配物[32] 酸類、酰基氯、酸酐、強氧化劑
5.聚合危害[33] 不聚合
6.分解產物[34] 氨
貯存方法
儲存注意事項[35] 儲存于陰涼、通風的庫房。遠離火種、熱源。庫溫不宜超過30℃。包裝要求密封,不可與空氣接觸。應與氧化劑、酸類等分開存放,切忌混儲。采用防爆型照明、通風設施。禁止使用易產生火花的機械設備和工具。儲區應備有泄漏應急處理設備和合適的收容材料。
合成方法
1、二氯乙烷法:由二氯乙烷與氨直接合成,在鉬鈦不銹鋼反應管道內進行,反應溫度控制在160~190℃,壓力為2.452 MPa,反應時間1.5min,反應后的合成液經蒸發一部分水分和過量氨進人中和器,用30%堿液中和,然后經濃縮、脫鹽、粗餾得粗乙二胺、粗三胺、粗多胺等混合物,最后再將粗乙二胺在常壓精餾得乙二胺成品,其含量70%,在加壓下蒸餾可得90%純度的產品。反應方程式如圖:
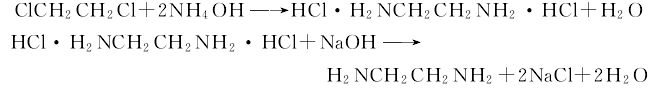
2、乙醇胺法:將乙醇胺、氨和循環物料蒸發成氣相混合物通入固定床反應器,反應在氫氣流中進行,反應溫度為300℃,壓力為25 MPa,反應生成物部分冷凝后分出氣相的氨和氫氣,經壓縮返回反應器,液相反應物經脫氨后脫水塔后進入精餾塔,從塔頂蒸出乙二胺和哌嗪,進一步分解得乙二胺成品。
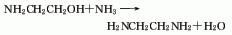
3、單乙醇胺胺化法:將乙醇胺、催化劑和水加入反應器中,催化劑(Ni5132p、G49B)用量為100ml液體中含有5g。用氮氣吹掃反應器中的空氣。并用氨吹掃掉氮氣,然后依次把氨、氫加入反應器內。在反應溫度160-240℃、壓力9.81-29.42MPa下反應5-10h,而得粗品,再經后處理而得成品,轉化率為50%。
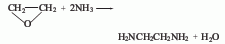
4、采用強0固體酸為催化劑,以二氯乙烷和過量的氨為原料制備乙二胺。(1)催化劑的制備:以一定濃度的氯化銨溶液與Na型分子篩(Na-MOR)在回流攪拌離子交換器中加熱回流4-12h,抽濾,烘干得NH4-MOR。再與一定量活性氧化鋁混合,造粒,打成片狀催化劑(沖壓壓力≈19.6MPa),片劑厚度1.5-2.0mm,于500℃煅燒得強固體酸催化劑,該催化劑為強酸性擇性催化劑。(2)乙二胺的合成:反應在通用型常壓固定床催化劑反應裝置中進行。原料NH3和載氣惰性氣體N2,在預熱混合器中混合預熱至一定溫度后通入催化反應器中。在反應溫度320-390℃,催化劑裝量為單乙醇胺的1%,NH3/NEA摩爾比為36-70,NH3的壓力0.5-0.7MPa,主要生成乙二胺和哌嗪(PIP)。(3)產物的分解:反應產物中含有NH3、水、乙二胺、哌嗪、乙醇胺及其他一些副產物。首先采用簡單精餾方法,[在100℃前蒸餾出NH4+環乙胺+少量水;再在100-118℃蒸出乙二胺+水;繼續在120-140℃之間蒸出其他高沸點副產物。由于乙二胺與水形成共沸物,因此采用萃取、恒沸等特殊分餾方法,才能達到產品要求。哌嗪脫除結晶水,采用鋅粉共精餾法或以烴類作共沸劑共沸蒸餾,可得無水哌嗪。未反應完的乙醇胺和氨經分離后可以返回系統重復使用。
精制方法:于乙二胺中加入10%粒狀氫氧化鈉或氫氧化鉀,振動數小時除去大部分水分和二氧化碳后,再用金屬鈉(2%~3%),分子篩或液態鈉鉀合金等適當的干燥劑加熱回流3小時后分餾。乙二胺與水雖能形成共沸混合物,但其共沸點比乙二胺沸點只高約2℃,故不宜用共沸蒸餾脫水。可以加入與水形成共沸混合物而與乙二胺不形成共沸混合物的第三種溶劑如苯、二異丙醚、哌啶等進行蒸餾精制。
5、在二氯乙烷中加入氨水,加熱至115~120℃反應。將反應溶液蒸發至開始有結晶,過濾、用乙醇洗滌。再于氮氣浴中蒸餾得無水乙二胺。
用途
與金屬離子形成配合物 1,2-二氨基乙烷與重金屬離子可形成穩定的配合物。在金屬或DAE定量分析中可以用DAE與CdII、CoII、CuII或HgII形成配合物。可以用1,2-二氨基乙烷制備的帶有2n氮原子的10~18個原子的大環與金屬離子生成多配位基的配合物,這些配合物在催化反應中用于特殊產物的制備[1]。鉻(II)鹽與DAE反應很容易制備還原劑,而DAE能大大提高CrII的還原能力,可將一級烷基鹵化物還原成烷烴,將芳基溴化物或碘化物還原成芳烴。
還原反應 在THF中,B2H2與DAE按1:1比例形成的配合物是一種高選擇性的還原劑,與硼氫化鈉有相同的反應活性。在KI3的DAE溶液中可以發生苯酚、苯胺、酪氨酸、吡咯和羥基苯甲酸的碘代。鋰與DAE體系是一種強的還原體系,可還原烯烴、芳香烴、苯酚和醇等。
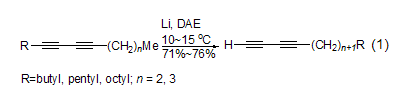
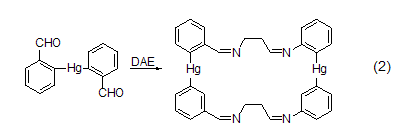
DAE可以與親電試劑反應生成單或雙的衍生物。DAE可用作對稱的結構單元來形成1,2-二氨基、1,2-二亞氨基、1,2-二酰氨基、二酰亞胺或二亞甲基將分子片段連接 (式2)[3]。
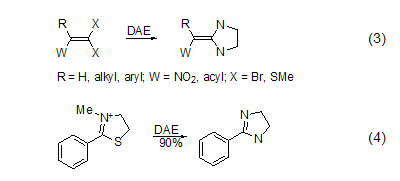
在兩個原子雜環體系的合成中DAE是非常好的試劑。與1-鹵代炔烴發生相似的反應可生成2-亞烷基咪唑啉或2-烷基咪唑啉。DAE和R(W)C=CX2類型的化合物反應生成取代的2-亞甲基咪唑啉 (式3)[4]。DAE與酸、酯、酰胺、二硫代酯、亞氨基、腈、2-芳基唑啉或2-苯基噻唑鹽反應,生成2-取代咪唑啉 (式4)[5]。
DAE與CS2反應可生成咪唑啉-2-硫醇。DAE與乙酸三步反應可生成2-甲基咪唑。DAE與O-烷基硫代氨基甲酸酯或N-烷基二硫代氨基甲酸酯反應可生成環狀胍。這些化合物也可由亞氨基鹵化物或異硫氰酸酯的二烷基硫縮醛與DAE反應來制得 (式5)[6]。
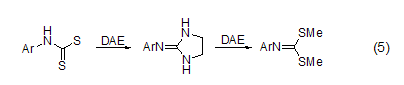
DAE與二醛、二酮、二羧酸及其衍生物反應生成包括有(N-C-C-N)片段的環狀化合物 (式6)[7]。1,2-二羰基化合物 (α-二酮、o-醌、烷基草酸酯) 會生成二氫吡嗪,而后環氧化反應生成吡嗪。
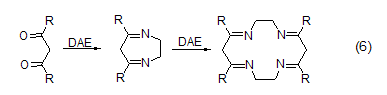
有兩個反應點的分子與DAE反應生成雙環產物 (式7,式8)[8,9]。由此方法制備的雜環包括吡咯[1,2-a]咪唑、咪唑[3,4-a]咪唑、咪唑[1,2-b]喹啉、咪唑[1,2-c]嘧啶等。

6.用于有機合成和農藥、活性染料、醫藥、環氧樹脂固化劑等的制取。[36]
安全信息
危險運輸編碼:UN 1604 8/PG 2
危險品標志: 腐蝕
腐蝕
安全標識:S23 S26 S45 S36/S37/S39
文獻
1. Mandal, S. K.; Nag, K. J. Org. Chem., 1986, 51, 3900. 2. Balova, I. A.; Remizova, L. A.; Makarycheva, V. F.; Rumyantseva, E. G.; Favorskaya, I. A. J. Org. Chem. USSR (Engl. Transl.), 1991, 27, 55. 3. Patel, U.; Singh, H. B.; Wolmersh, G. Angew. Chem. Int. Ed., 2005, 44, 1715. 4. (a) Nguyen, N. V.; Baum, K. Tetrahedron Lett., 1992, 33, 2949. (b) Wang, X. J.; Huang, Z. T. Chem. Ber., 1990, 123, 2141. (c) Huang, Z. T.; Shi, X. Synth. Commun., 1990, 20, 1321. 5. Singh, H.; Sarin, R. Indian J. Chem., Sect. B, 1986, 25B, 81. 6. Fukada, N.; Hayashi, M.; Suzuki, Y. Bull. Chem. Soc. Jpn., 1985, 58, 3379. 7. (a) Bergeron, R. J.; Hoffman, P. J. Org. Chem., 1980, 45, 161. (b) Liao, C. C.; Hsieh, H. P.; Lin, S. Y. Chem. Commun., 1990, 545. 8. Urleb, U.; Stanovnik, B.; Ti?ler, M. J. Heterocycl. Chem., 1990, 27, 643. 9. Bodtke, A.; Langer, P. Tetrahedron Lett., 2004, 45, 8741. [1~9]參考書:現代有機合成試劑<性質、制備和反應>;胡躍飛 付華 編著;化學工業出版社;ISBN 7-5025-8542-7 [10~36]參考書:危險化學品安全技術全書.第一卷/張海峰主編.—2版.北京;化學工業出版社,2007.6 ISBN 978-7-122-00165-8
備注
暫無
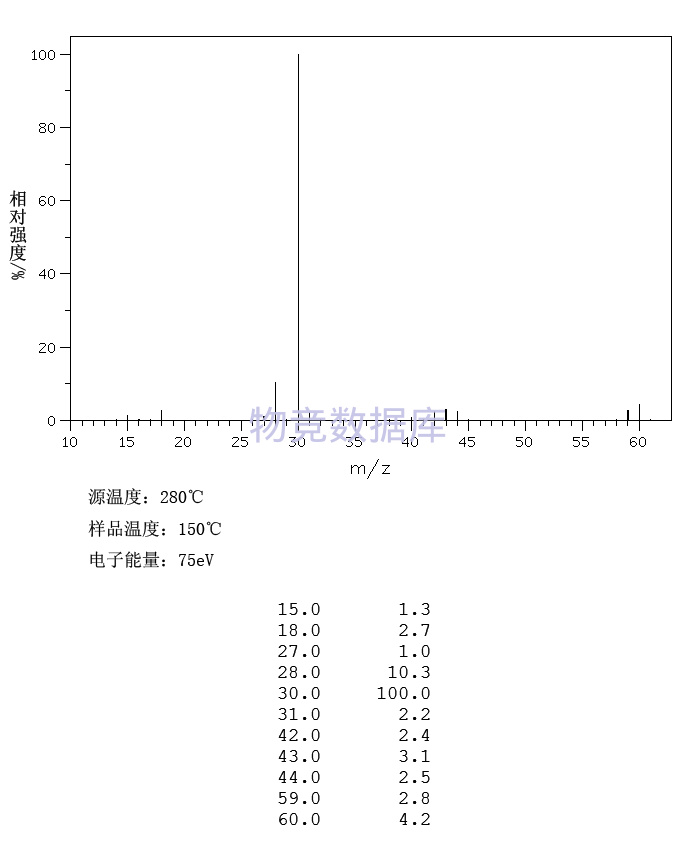
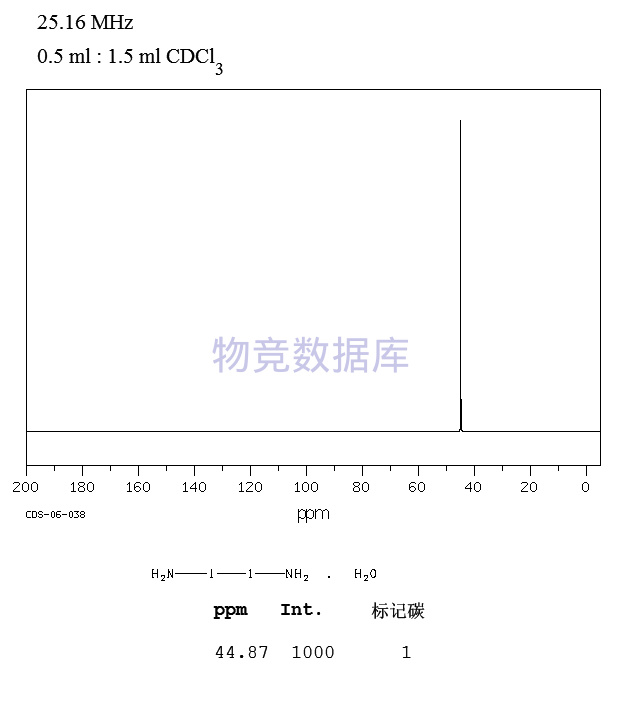
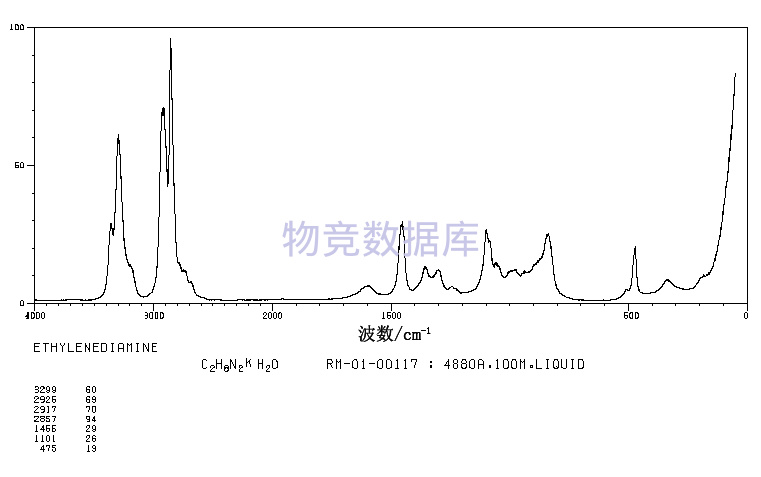
表征圖譜
統計數據
共收錄化學品數據
147579 條





 滬公網安備 31010602001115號
滬公網安備 31010602001115號