尿素過氧化氫復合物 Urea hydrogen peroxide adduct
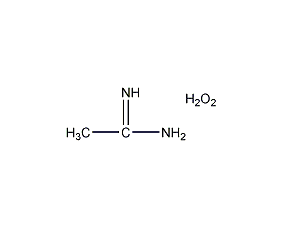
結構式
| 物競編號 | 03J8 |
|---|---|
| 分子式 | CH6N2O3 |
| 分子量 | 94.07 |
| 標簽 | Carbamide perhydrate, Carbamide-Peroxide, Urea hydrogen peroxide adduct, UHP, Percarbamide, 脂肪族化合物 |
編號系統
CAS號:124-43-6
MDL號:MFCD00013119
EINECS號:204-701-4
RTECS號:暫無
BRN號:3680414
PubChem號:暫無
物性數據
1.性狀:白色結晶
2.熔點(℃):90~93
3.溶解性:易溶于水、乙醇、乙二醇和二氯甲烷等有機溶劑中。
毒理學數據
暫無
生態學數據
暫無
分子結構數據
暫無
計算化學數據
1.疏水參數計算參考值(XlogP):無
2.氫鍵供體數量:4
3.氫鍵受體數量:3
4.可旋轉化學鍵數量:0
5.互變異構體數量:2
6.拓撲分子極性表面積110
7.重原子數量:6
8.表面電荷:0
9.復雜度:29
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:2
性質與穩定性
1.基本性質:水溶液兼有尿素和雙氧水的性質,在水中能緩慢放出氧氣。與過碳酸鈉等無機過氧化物相比,其性能更優越,具有活性氧含量高、在水中溶解度大、穩定性好、可溶于有機溶劑等優點。
2.潮濕的試劑在40 oC以上會分解出水和氧氣,有腐蝕性和氧化性,建議在干燥陰涼處存儲。
貯存方法
貯存于干燥、潔凈、通風良好、室溫15℃~25℃的倉庫內。遠離火種、熱源和避免陽光直射,注意防潮和雨淋。
合成方法
1. 有濕法工藝和干法工藝兩種,干法工藝要求的雙氧水濃度較高(85(wt)%左右), 且存在設備復雜、技術條件苛刻、能耗高、產品穩定性差等缺點。大多數過碳酰胺的制備采用濕法工藝,即采用低濃度的雙氧水與飽和或過飽和的尿素溶液反應,添加一定量的穩定劑并控制反應溫度經過濾、干燥得產品,母液循環使用。
2. 通過尿素在30% 的過氧化氫水溶液中重結晶來制備[1]。
用途
1. 在醫藥和制藥工業上,過氧化尿素可用作一種高效、安全、方便的固體消毒劑,亦可用水溶液。與雙氧水、過氧乙酸比較具有明顯的殺菌力強、殺菌譜廣,使用濃度低,不留殘毒等優點,還可抑制細菌與霉菌生長,殘留無刺激。在癌癥治療中用于抗肝腹水等。在日化工業中:過氧化尿素可用作人及動物毛發的漂白劑、拉直劑、燙發、染發的中和劑,特別是在牙膏中添加后,能起到一般牙膏所起不到的作用:減少牙斑和細菌,減少牙周疾病和齲齒。同時能使牙齒釉質變硬,對齲齒產生很強的抑制作用。此外,過氧化尿素可以作為漂白劑應用于中性洗滌劑。在農業和養殖業中:過氧化尿素在水產養殖業中可用于魚塘增氧劑、消毒劑和翻塘缺氧時的急救劑。還可作小家禽飼料消毒供氧劑。還可用作水果、蔬菜的富氧催熟劑。在紡織造紙工業中:過氧化尿素可用于棉花、羊毛、人造絲、亞麻纖維的漂白劑。聚酰胺纖維的柔軟劑、抗靜電劑和脫色劑。還用于造紙業作漂白劑,礦石浮選改良劑等。
2. 尿素過氧化氫復合物 (UHP) 是由尿素和過氧化氫間的強氫鍵作用產生的配合物。它將不穩定的過氧化氫轉變為易操作、安全的、穩定于室溫的固體,且價格低廉。UHP在不同的溶劑和催化劑下顯示出不同的氧化能力,是有機合成中一種重要的氧化試劑。最近發表的一篇論文對UHP在合成中的應用做了簡單的介紹[2]。
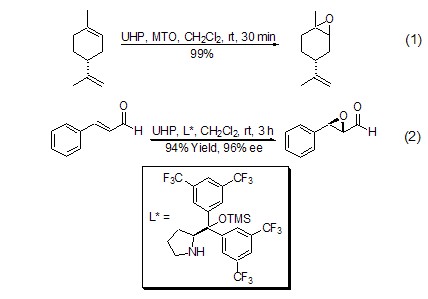
UHP具有過氧化氫的性質,常用于雙鍵的環氧化反應,并具有高度的區域和立體選擇性以及較高的轉化率。UHP與酸酐聯用 (例如:乙酸酐、馬來酸酐),可以原位生成有機過氧酸,這種方法可以代替使用高濃度的有機過氧酸。對于α,β-不飽和酮和苯醌的環氧化反應,一般需要堿的催化,如K2CO3[3]。UHP與甲基三氧化錸 (MTO) 聯用,使得烯烴的環氧化反應具有優秀的區域和立體選擇性 (式1)[4]。對于α,β-不飽和醛的不對稱氧化,UHP顯示了較其它氧化劑更好的立體選擇性和轉化率 (式2)[5]。
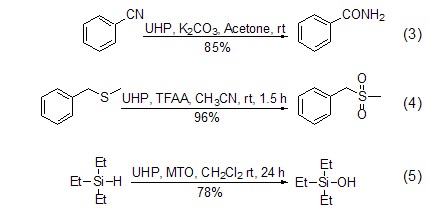
由于UHP的氧化性能可以方便地進行調控,所以可以用于多種官能團的轉化,例如:將氰基轉化成為酰胺,肟成為硝基,醛成為酸等 (式3,式4)[6]。UHP的另一個重要用途是對 N、S、P、I[2,6]和Si (式5)[7] 等雜原子的氧化反應,在多數情況下其選擇性要好于過氧化氫水溶液。
UHP同有機過酸一樣,也可以完成Baeyer-Villiger重排反應,而且具有較高的立體選擇性 (式6)[8]。

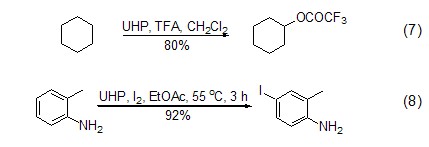
近期文獻報道,UHP還可以實現對于非活性C-H鍵的氧化,形成羥基或酯基(式7)[9];UHP與I2聯用可以方便有效地實現對芳基的碘化 (式8)[10]。
安全信息
危險運輸編碼:UN 1511 5.1/PG 3
危險品標志: 氧化劑
氧化劑  危害環境
危害環境
安全標識:S17 S26 S45 S36/S37/S39
文獻
1. Lu, C.-S.; Hughes, E. W.; Giguère, P. A. J. Am. Chem. Soc., 1941, 63, 1507. 2. Taliansky, S. Synlett, 2005, 12, 1962. 3. Fan, C. L.; Lee, W. D.; Teng, N. W.; Sun, Y. C.; Chen, K. J. Org. Chem., 2003, 68, 9816. 4. Spilling, C. D.; Borhlow, T. R. Tetrahedron Lett., 1996, 37, 2717. 5. Marigo, M.; Jranzén, J.; Toulsen, T. B.; Whuang, W.; Jorgensen, K. A. J. Am. Chem. Soc., 2005, 127, 6964. 6. Varma, R. S.; Naicker, K. P. Org. Lett., 1999, 1, 189. 7. Adam, W.; Mitchell, C. M.; Saha-Moller, C. R.; Weichold, O. J. Am. Chem. Soc., 1999, 121, 2097. 8. Katsuki, T.; Irie, R.; Uchida, T.; Watanabe, A. Proc. Natl.Acad. Sci. U. S. A., 2004, 101, 5737 9. Moody, C. J.; O’Connell, J. L. Chem. Commun., 2000, 1311. 10. Lulinski, P.; Kryska, A.; Sosnowski, M.; Skulski, L. Synthesis, 2004, 441. 11.參考書:現代有機合成試劑<性質、制備和反應>;胡躍飛 付華 編著;化學工業出版社;ISBN 7-5025-8542-7
備注
暫無
表征圖譜
統計數據
共收錄化學品數據
147579 條




 滬公網安備 31010602001115號
滬公網安備 31010602001115號