(1S,2S)-N,N'-雙(2-乙酰-3-氧代-2-亞丁烯基)-1,2-二均三甲苯基乙二胺合鈷(II) (1S,2S)-N,N'-Bis(2-acetyl-3-oxo-2-butenylidene)-1,2-dimesitylethylenediaminato Cobalt(II)
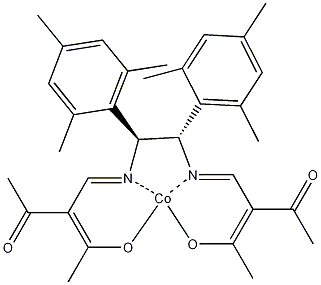
結(jié)構(gòu)式
| 物競(jìng)編號(hào) | 108B |
|---|---|
| 分子式 | C32H38CoN2O4 |
| 分子量 | 573.59 |
| 標(biāo)簽 | (S)-AMAC, 不對(duì)稱催化劑, 手性鈷(II)配合物, 硼氫化還原用光學(xué)活性酮亞胺鈷(II)配合物 |
編號(hào)系統(tǒng)
CAS號(hào):259259-80-8
MDL號(hào):暫無(wú)
EINECS號(hào):暫無(wú)
RTECS號(hào):暫無(wú)
BRN號(hào):暫無(wú)
PubChem號(hào):暫無(wú)
物性數(shù)據(jù)
1. 性狀:紅黃色-深紅黃色晶體粉末
2. 密度(g/mL):未確定
3. 相對(duì)蒸汽密度(g/mL,空氣=1):未確定
4. 熔點(diǎn)(oC):未確定
5. 沸點(diǎn)(oC,常壓):未確定
6. 沸點(diǎn)(oC60mmHg):未確定
7. 折射率:未確定
8. 閃點(diǎn)(o C):未確定
9. 比旋光度(o):未確定
10. 自燃點(diǎn)或引燃溫度(oC):未確定
11. 蒸氣壓(kPa,):未確定
12. 飽和蒸氣壓(kPa,60oC):未確定
13. 燃燒熱(KJ/mol):未確定
14. 臨界溫度(oC):未確定
15. 臨界壓力(KPa):未確定
16. 油水(辛醇/水)分配系數(shù)的對(duì)數(shù)值:未確定
17. 爆炸上限(%,V/V):未確定
18. 爆炸下限(%,V/V):未確定
19. 溶解性:未確定
毒理學(xué)數(shù)據(jù)
暫無(wú)
生態(tài)學(xué)數(shù)據(jù)
暫無(wú)
分子結(jié)構(gòu)數(shù)據(jù)
暫無(wú)
計(jì)算化學(xué)數(shù)據(jù)
暫無(wú)
性質(zhì)與穩(wěn)定性
暫無(wú)
貯存方法
暫無(wú)
合成方法
合成方法:首先將1,3-二羰基化合物的活性亞甲基甲酰化,然后在光學(xué)活性 1,2-二芳基乙二胺作用下得到光學(xué)活性酮亞胺配體,配體與甲醇鈉、二氯化鈷作用生成光學(xué)活性酮亞胺鈷(II)配合物。具體步驟如圖所示:
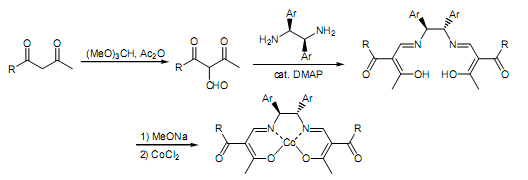
用途
1. 酮類(lèi)還原
由向山,Yamada和同事開(kāi)發(fā)的旋光性酮亞胺鈷(II)配合物的不對(duì)稱還原法很有可能成為獲得光學(xué)活性醇的一個(gè)很簡(jiǎn)便流行經(jīng)濟(jì)的方法
不對(duì)稱還原法很簡(jiǎn)單,膽色素中加入1 mol%的(S)-MPAC, 使用經(jīng)過(guò)四氫化呋喃甲醇和乙醇預(yù)先處理過(guò)的硼氫化物還原2,2-二甲基-1-四氫萘酮,得到產(chǎn)品(S)-2,2-二甲基-1-四氫萘醇,產(chǎn)率為96%,91%e.e.. 此外,在(S)-MPAC的參與下,(S)-2-甲基-1-四氫萘酮被優(yōu)先還原為(1S,2S)-2-甲基-1-四氫萘醇,未參加反應(yīng)的(R)-2-甲基-1-四氫萘酮可以除去。因此,可以進(jìn)行α-取代羰基化合物的動(dòng)力學(xué)光學(xué)分割。

2.光學(xué)活性1,3-二醇的合成
1,3-二芳基-1,3-丙二醇和它的衍生物因其作為手性助劑或者是手性配合物來(lái)源的用途,廣為人知。1,3-二酮利用金屬鍺配合物催化劑的不對(duì)稱氫化作用來(lái)生產(chǎn)二醇。由于這個(gè)反應(yīng)需要高壓環(huán)境,所以更為簡(jiǎn)便的方法接待解決。
Yamada和同事已經(jīng)證實(shí)1,3-二芳基-1,3-丙二酮利用光學(xué)活性酮亞胺鈷(II)配合物作為催化劑,硼氫化鈉做氫化來(lái)源,能夠?qū)崿F(xiàn)高外消旋選擇性和對(duì)映體選擇性還原。當(dāng)使用AMAC(不對(duì)稱碳原子上有一個(gè)三甲苯基基團(tuán))時(shí),可以得到具有高外消旋選擇性和對(duì)映體選擇性的1,3-二醇。
這個(gè)不對(duì)稱還原方法非常簡(jiǎn)單,提純操作方便。當(dāng)1,3-二苯基-1,3-丙二酮被用來(lái)作為基質(zhì)材料時(shí),還原產(chǎn)物從乙酸乙酯中從結(jié)晶出來(lái)。光學(xué)純1,3-二苯基-1,3-丙二醇大概可以得到近60%的產(chǎn)量。
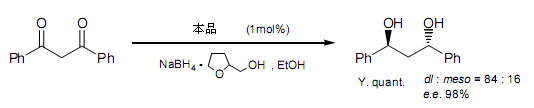
3.光學(xué)活性反式-羥醛縮合化合物的合成
光學(xué)活性反式-羥醛縮合化合物合成,一些有效的方法包括Abiko,Masamune和其同事利用手性助劑的合成方法已經(jīng)報(bào)道。Yamada和同事已經(jīng)論證了由克萊森縮合反應(yīng)而得的2-取代基-1,3-二羰基化合物不對(duì)稱還原反應(yīng)生成反式-羥醛縮合化合物。比如:2-甲基-1,3-二苯基-1,3-丙二酮,加入5 mol%AMAC,預(yù)先處理過(guò)的硼氫化鈉還原生成3-羥基酮。
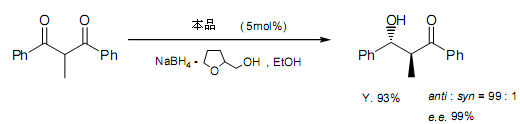
為了推廣這個(gè)反應(yīng),反應(yīng)也可應(yīng)用在2-取代基-1-烷基-1,3-二酮的還原中。3-羥基酮可以從2,4-二甲基-1-苯基-1,3-丙二酮而得,產(chǎn)率為46%,伴有99%的化學(xué)選擇性,99%反式-選擇性產(chǎn)品,99%e.e.兩個(gè)通常認(rèn)知的2-取代-1-烷基-3-芳基-丙二酮部分不對(duì)稱還原反應(yīng)是利用Ru-BINAP 配合物做催化劑還原反應(yīng)和利用光學(xué)活性Ru-配合物請(qǐng)轉(zhuǎn)移反應(yīng)。在這些例子中,烷基邊上的羰基空間位阻小被還原。另一方面,利用酮亞胺鈷(II)配合物還原的烷基邊上的羰基基團(tuán)的方法經(jīng)Yamada和同事進(jìn)一步研究,效率更高。
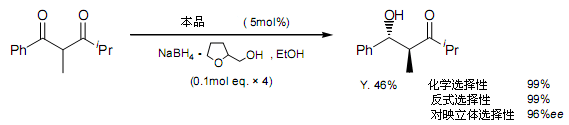
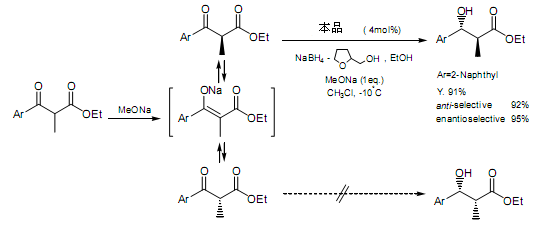
此外,Yamada和同事將這個(gè)還原方法應(yīng)用到2-取代-3-酮酸酯中,并且已經(jīng)報(bào)道了其動(dòng)態(tài)動(dòng)力學(xué)拆分原理。根據(jù)這個(gè),2-甲基-3-(2-萘基)-3-羰基丙酸乙酯生產(chǎn)出光學(xué)活性3-羥基-2-甲基-3-(2-萘基)丙酸乙酯,91%產(chǎn)率,92%反式-選擇性產(chǎn)品,95%e.e.
4.胺的還原
1 mol%的(S)-MPAC,N-磷亞胺被四氫化呋喃甲醇、乙醇處理過(guò)的硼氫化鈉還原,產(chǎn)物(S)- N-磷酰胺基,產(chǎn)率很高,光學(xué)純度高。比如:N-二苯基磷酰-1,2,3,4-四氫-1-萘亞胺還原得到相應(yīng)的 (S)- N-磷酰胺產(chǎn)率88%-92%。
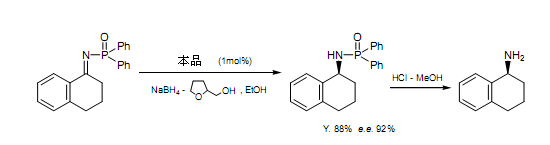
N-磷酰胺中的磷酰基溫和的條件下可以移除,得到光學(xué)活性胺,光學(xué)純度為虧損。
5.α,β-不飽和胺的1,4-還原
0.5mol%的(S)-MPAC,四氫化呋喃-2-甲醇預(yù)先處理過(guò)的硼氫化鈉,還原(Z)-3-環(huán)己基-2-丁烯酰胺,產(chǎn)物(S)-丁基酰胺,產(chǎn)率99%。91%e.e. (E) -丁烯酰胺時(shí)產(chǎn)物(R)-丁基酰胺.
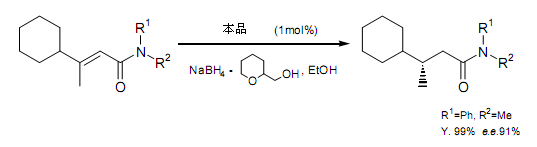
總之,光學(xué)活性酮亞胺鈷(II)配合物做催化劑的還原反應(yīng),在溫和條件下使用硼氫化鈉即可完成,這是獲得高光學(xué)純度的一個(gè)極為有效的還原試劑。因此,它可以合成光學(xué)活性醇、胺、1,3-二醇、3-羥基羰基化合物、β-不飽和胺等化學(xué)品,已經(jīng)逐漸引起廣泛的關(guān)注。
安全信息
危險(xiǎn)運(yùn)輸編碼:暫無(wú)
危險(xiǎn)品標(biāo)志:暫無(wú)
安全標(biāo)識(shí):暫無(wú)
危險(xiǎn)標(biāo)識(shí):暫無(wú)
文獻(xiàn)
Y. Ohtsuka, K. Koyasu, T. Ikeno, T. Yamada, Org. Lett., 2001, 3, 2543; Y. Ohtsuka, K. Koyasu, D. Miyazaki, T. Ikeno, T. Yamada, Org. Lett., 2001, 3, 3421; M. Sato, Y. Gunji, T. Ikeno, T. Yamada, Synthesis, 2004, 1434; T. Nagata, T. Yamada, WO 02038535 (Mitsui Chemicals Inc.). Reviews T. Yamada, T. Nagata, Y. Ohtsuka, T. Ikeno, T. Mukaiyama, Yuki Gosei Kagaku Kyokaishi (J. Synth. Org. Chem. Jpn), 2003, 61, 843; T. Yamada, T. Nagata, K. D. Sugi, K. Yorozu, T. Ikeno, Y. Ohtsuka, D. Miyazaki, T. Mukaiyama, Chem. Eur. J., 2003, 9, 4485.
備注
暫無(wú)
表征圖譜
統(tǒng)計(jì)數(shù)據(jù)
共收錄化學(xué)品數(shù)據(jù)
147579 條




 滬公網(wǎng)安備 31010602001115號(hào)
滬公網(wǎng)安備 31010602001115號(hào)