α-吡喃酮 alpha-Pyrone
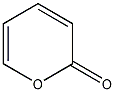
結構式
| 物競編號 | 116P |
|---|---|
| 分子式 | C5H4O2 |
| 分子量 | 96.08 |
| 標簽 | 2H-吡喃-2-酮, 2-吡喃酮, 2H-Pyran-2-one, 2-Pyrone |
編號系統
CAS號:504-31-4
MDL號:MFCD00006639
EINECS號:207-990-5
RTECS號:暫無
BRN號:1511
PubChem號:24869900
物性數據
1.性狀:淡黃色透明液體
2.沸點(℃):207.5
3.沸點(℃,3466Pa):110
4.熔點(℃):8~9
5.閃點(℃):94
6.相對密度d420:1.21
7.折射率nD20:1.53
8.溶解性:易溶于水、丙酮。
毒理學數據
生態學數據
對環境有危害,對水體有污染,禁止進入水體。
分子結構數據
暫無
計算化學數據
1.疏水參數計算參考值(XlogP):0.8
2.氫鍵供體數量:0
3.氫鍵受體數量:2
4.可旋轉化學鍵數量:0
5.互變異構體數量:無
6.拓撲分子極性表面積26.3
7.重原子數量:7
8.表面電荷:0
9.復雜度:133
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:1
性質與穩定性
1.加熱易分解。
2.存在形式:存在于煙葉中。
貯存方法
密封貯藏,儲存在陰涼、干燥地方,遠離火源。
合成方法
在650 oC加熱條件下裂解鄰吡喃酮酸脫羧可以得到。5,6-二氫吡喃-2-酮等二氫類似物可以用丁烯酸和甲醛通過催化縮合得到。
用途
2-吡喃酮及類似物主要用于環加成[1~4],這些產物又可以轉化為各種多官能團的環己二烯和苯。吡喃酮可和一系列標準的親雙烯體反應,包括順丁烯二酸酐、二甲基乙炔基羧酸酯、富馬酸、甲基乙烯酮以及丙烯酸酯等。在加熱條件下,無法分離得到二環內酯中間體,會原位脫羧形成環己二烯或苯。在前一種情況下,第2倍量的親雙烯體可以與第一步環加成的產物進一步發生環加成,得到一前一后的2:1加合物 (式1)[5]。
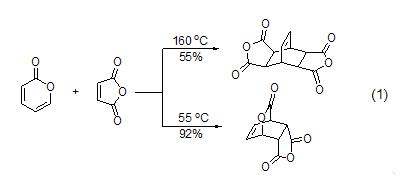
這種方法被用來合成桶烯以及拓撲環。兩個不活潑的親雙烯體發生分子內的前后環加成反應是合成天然產物中有趣的多環化合物的一個好方法 (式2)[6]。
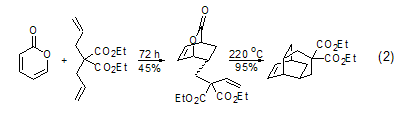
在加熱或者高壓下進行二聚,往往會得到多聚產物。高溫625 oC下,可逆的電環化開環可以得到烯酮醛中間體。乙醚中對2-吡喃酮進行直接照射,會得到二環[2.2.0]吡喃-2-酮 (式3)[7]。
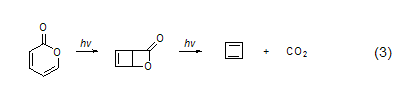
重氮甲烷和氰化物則進攻C-6 (式4)[8]。
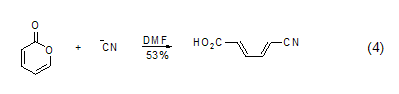
2-吡喃酮也能發生親電取代[3]。通過溴化或者氯化可以得到3-鹵-2-吡喃酮,這個反應通常是先連續的鹵化,然后脫去鹵化氫,而不是直接發生親電取代[9]。3-溴-2-吡喃酮自身可以與二甲基銅酸鋰發生金屬-鹵素的交換,得到3-銅-2-吡喃酮。
安全信息
危險運輸編碼:暫無
危險品標志:暫無
危險標識:暫無
文獻
1. Stauton, J. In Comprehensive Organic Chemistry, Barton, D. H. R.; Oills, W. D. Eds; Pergamon: New York, 1979, Vol. 4, p 629. 2. Posner, G. H.; Nelson, T. D.; Kinter, C. M.; Johnson, N. J. Org. Chem., 1992, 57, 4083. 3. Posner, G. H.; Bull, D. S. Recent Research Developments in Organic Chemistry, 1997, 1, 259. 4. West, F. G. Advances in Cycloaddition, 1997, 4, 1. 5. Tetsuro, S.; Kenichi, S. CRC Handbook of Organic Photochemistry and Photobiology, 2nd Ed, 2004. 6. Marko, I. E.; Seres, P.; Swarbrick, T. M.; Station, I.; Adams, H. Tetrahedron Lett., 1992, 33, 5649. 7. Arnold, B. R.; Brown, C. E.; Lusztyk, J. J. Am. Chem. Soc., 1993, 115, 1576. 8. Vogel, G. J. Org. Chem., 1965, 30, 203. 9. Pirkle, W. H.; Dins, M. J. Org. Chem., 1969, 34, 2239. 10.參考書:現代有機合成試劑<性質、制備和反應>;胡躍飛 付華 編著;化學工業出版社;ISBN 7-5025-8542-7 [1]Roberts D L, Rec. Adv. Tob. Sci., 1988, 14: 49-81. [2]LIDE D R. Editor-in-Chief, CRC Handbook of Chemistry and Physics on CD-ROM, Version 2003, CRC Press. [3]Baker R R. Tobacco:Production,chemistry and technology,Oxford,UK:Blackwell Science,1999,398-439 [4]參考書:(煙草與煙氣化學成分);謝劍平 主編;化學工業出版社;ISBN 978-7-122-09119-2
備注
暫無
表征圖譜
統計數據
共收錄化學品數據
147579 條




 滬公網安備 31010602001115號
滬公網安備 31010602001115號