草酸 Oxalic acid
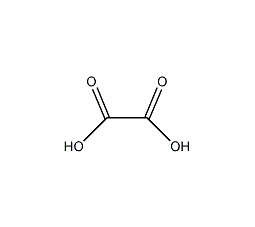
結構式
| 物競編號 | 03WJ |
|---|---|
| 分子式 | C2H2O4. |
| 分子量 | 90.03 |
| 標簽 | 乙二酸, Ethanedioic acid, 提煉稀有金屬的溶劑, 染料還原劑, 鞣革劑, 酸度調節劑 |
編號系統
CAS號:144-62-7
MDL號:MFCD00002573
EINECS號:205-634-3
RTECS號:RO2450000
BRN號:385686
PubChem號:24886864
物性數據
1. 性狀:無色、無味的有吸濕性物質,單斜片狀、棱柱體結晶或白色顆粒,易風化。在空氣中變為二水合物。
2. 熔點(oC):189.5 [α型(菱形)]
3. 熔點(oC):182 [β型(單斜晶形)]
4. 相對密度(g/mL,17oC):1.900 (α型)
5. 相對密度(g/mL,17oC):1.895 (β型)
6. 折射率(20oC):1.540
7. 燃燒熱(KJ/mol,25oC):-245.61
8. 標準生成熱(KJ/mol,25oC):-826.78
9. 溶解熱(KJ/mol,水中):-9.58
10. 升華熱(KJ/mol):90.58
11. 分解熱(KJ/mol):826.78
12. 熱導率(W/(m·K),0oC):0.9
13. 溶解性:易溶于乙醇,溶于水,微溶于乙醚,不溶于苯和氯仿。
毒理學數據
1、急性毒性:大鼠經口LD50:7500 mg/kg;小鼠腹腔LC50:270 mg/kg;
2、刺激數據:皮膚- 兔子 500 毫克/ 24小時 輕度; 眼- 兔子 0.25 毫克/ 24小時 重度
3、有腐蝕性,對皮膚和黏膜有刺激性,吸入蒸氣、粉塵會引起中毒,吞入后引起腸胃炎、嘔吐、腹瀉等癥狀。成人最低致死量為71 mg/kg。
生態學數據
該物質對環境可能有危害,對水體應給予特別注意。該品具有強烈刺激性和腐蝕性。其粉塵或濃溶液可導致皮膚、眼或黏膜的嚴重損害。具有較強毒性和腐蝕性。草酸對人的最低致死量為71mg/kg,對成年人的致死量為15~30g。人若口服5g草酸及草酸即發生胃腸道炎、虛脫、抽搐和休克等癥狀以至死亡。吸入草酸蒸氣發生慢性中毒者,有極度虛弱、鼻黏膜潰瘍、咳嗽、全身疼痛、嘔吐及體重減輕等癥狀并在尿中出現蛋白。
分子結構數據
1、 摩爾折射率:14.44
2、 摩爾體積(cm3/mol):50.8
3、 等張比容(90.2K):155.3
4、 表面張力(dyne/cm):87.3
5、 極化率(10-24cm3):5.72
計算化學數據
1.疏水參數計算參考值(XlogP):-0.3
2.氫鍵供體數量:2
3.氫鍵受體數量:4
4.可旋轉化學鍵數量:1
5.互變異構體數量:無
6.拓撲分子極性表面積74.6
7.重原子數量:6
8.表面電荷:0
9.復雜度:71.5
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:1
性質與穩定性
1.常溫常壓下穩定。禁配物:堿、酰基氯、堿金屬。
在干燥空氣中可加熱會失去結晶水,易升華,100℃開始升華,125℃時迅速升華,157℃開始分解為甲酸和CO2。二水化合物的熔點為101.5℃。易溶于熱水、乙醇,稍溶于冷水。草酸的酸性比其他的二元酸強,與甲酸類似。生成鹽和酸式鹽、酯和酸式酯。可溶于水、乙醇和乙醚。
2.本品有毒,有腐蝕性,對皮膚和黏膜有刺激性,內服草酸對腎會發生明顯傷害,腎小管內出現草酸鈣沉積,患者表現出軟弱無力,全身疼痛和體重減輕的癥狀。對人的最低致死量為71mg/kg。操作現場應有良好的通風條件,要穿戴好防護用具,特別是有草酸粉塵的地方,工作人員一定要戴好防毒面具。草酸誤服者最好是用含鈣和鎂的清毒劑洗胃,皮膚沾上草酸要用大量清水沖洗。貯存溫度不要超過40℃,應防潮、防曬、防雨,遠離氧化物和堿性物質。按有毒化學品規定貯運。
3.草酸具有強烈刺激性氣味,具有極大的腐蝕性。
4.存在于烤煙煙葉、白肋煙煙葉、主流煙氣中。
5.草酸具有無水和二水合兩種形式,是一個溫和的質子酸,在有機合成中具有非常重要的用途,如實現Beckmann反應,羰基的保護和去保護,多種選擇性斷裂和水解反應以及多種縮合反應等。草酸也是一個雙齒配體,在無機化學中廣泛地用作沉淀劑和螯合試劑。
草酸能夠非常有效地誘導實現Beckmann反應,即誘導酮肟底物向二級酰胺化合物的轉變 (式1)[1],反應不需要溶劑,放出氣體副產物CO和CO2,產率很高。

在羥胺鹽酸鹽存在下,草酸能夠高產率地一步實現酮類化合物向酰胺化合物的轉化 (式2)[1]。反應對各種芳基和烷基酮底物有效。

在水相草酸存在下,烯醇醚能發生快速水解反應得到對應的酮,而不會發生雙鍵位移的副反應 (式3)[2]。相反,在其它無機酸誘導下,烯醇醚則會發生雙鍵位移得到共軛酮產物。
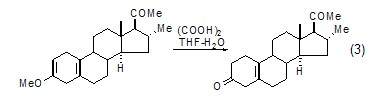
草酸既能用于制備縮醛或縮酮,也能用于斷裂縮醛或縮酮。在無水草酸作用下,酮或醛能與乙烯乙二醇或乙醇反應得到縮醛或縮酮 (式4)[3];在水合草酸作用下,縮醛或縮酮又會發生斷裂反應獲得相應的醛或酮 (式5)[4]。
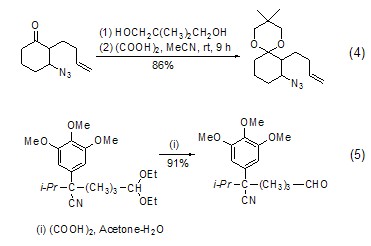
醇類底物在無水草酸中加熱或在水合草酸中回流都能轉化為烯烴產物,對于特殊羥基酮底物,則能在草酸作用下發生分子內關環反應得到環醚產物 (式6)[5]。
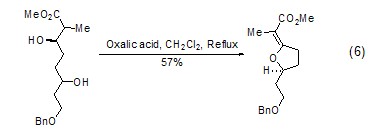
對于二氫吡啶底物,在草酸作用下能選擇性發生質子脫錫或質子脫硅反應 (式7)[6]。

β-酮酯在草酸水溶液中能發生選擇性酯基消除反應,得到相應的酮 (式8)[7]。

貯存方法
1.密封于干燥陰涼處保存。嚴格防潮、防水、防曬。貯存溫度應不超過40℃。
2.遠離氧化物及堿性物質。用聚丙烯編織袋內襯塑料袋包裝。
合成方法
1.草酸遍布于自然界,常以草酸鹽形式存在于植物如伏牛花、羊蹄草、酢漿草和酸模草的細胞膜,幾乎所有的植物都含有草酸鈣。草酸工業化生產方法主要有:甲酸鈉法、氧化法、羰基合成法、乙二醇氧化法、丙烯氧化法、一氧化碳偶聯法。
(1).甲酸鈉法一氧化碳凈化后在加壓情況下與氫氧化鈉反應,生成甲酸鈉,然后經高溫脫氫生成草酸鈉,草酸鈉再經鉛化(或鈣化)、酸化、結晶和脫水干燥等工序,得到成品草酸。一氧化碳與氫氧化鈉合成壓力一般為1.8-2.0MPa。脫氫溫度為400℃。

(2).氧化法以淀粉或葡萄糖母液為原料,在礬觸媒存在下,與硝酸-硫酸進行氧化反應得草酸。廢氣中的氧化氮送吸收塔回收生成稀硝酸。

(3).羰基合成法一氧化碳經提純到90%以上,在鈀催化劑存在下與丁醇發生羰基化反應,生成草酸二丁酯,然后通過水解得到草酸,此法分為液相法和氣相法兩種,氣相法反應條件較低,反應壓力為300-400kPa。而液相法反應壓力為13.0-15.0MPa。
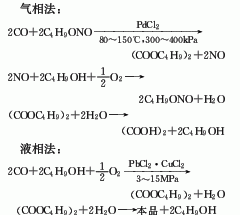
(4).乙二醇氧化法以乙二醇為原料,在硝酸和硫酸存在下,用空氣氧化而得。5.丙烯氧化法氧化過程分兩步進行。第一步用硝酸氧化,使丙烯轉化為α-硝基乳酸;然后進一步催化氧化得到草酸。第二步也可采用混酸為氧化劑。丙烯氧化法生產工業級草酸二水化合物,以丙烯計總收率大于90%。原料消耗定額:焦炭(84%)510kg/t、硫酸(100%)950kg/t、燒堿(100%)920kg/t。
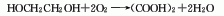
2.將二水合草酸H2C2O4·2H2O加熱到100℃或在脫水能力強的干燥器中可轉化為無水合物。
3.將爐煤氣精制加壓,與氫氧化鈉溶液在一定溫度下逆流接觸,生成甲酸鈉。甲酸鈉水溶液經蒸發濃縮,離心分離而得到甲酸鈉結晶。將甲酸鈉在煅燒爐中轉化為草酸鈉,經水洗、過濾除去碳酸鈉后,加入消石灰反應。生成的草酸鈣濾出并用硫酸分解。濾出硫酸鈣,所得草酸結晶用重結晶法精制。或者用含30%~40%硫酸和20%~25%硝酸的混合液及五氧化二釩催化劑,在一定溫度和壓力下氧化乙二醇制得。也可以葡萄糖、蔗糖、淀粉、糊精和糖漿等碳水化合物為原料,在釩催化劑存在下,通過硝酸硫酸氧化而制得草酸。粗品用母液和熱水再溶解,經脫脂、分離、過濾和重結晶制得。
4.碳水化合物氧化法 以葡萄糖、蔗糖、淀粉、糊精和糖漿等碳水化合物為原料,在釩催化劑存在下,通過硝酸-硫酸氧化而制得草酸。粗晶經冷卻、結晶、離心、干燥得成品。廢氣中的氧化氮送入吸收塔回收稀硝酸。在73~80℃的溫度下,將約含85%純淀粉的原料加到草酸母液中,分散成漿液并回流水解約6h。所得淀粉溶液含有50%~60%的葡萄糖,送入裝有釩催化劑的反應器中與回收的較濃草酸母液混合,用蒸汽將葡萄糖母液加熱至約63℃,在攪拌下逐漸加入硝酸進行氧化反應。反應熱通過冷卻盤管吸收,生成的NO煙霧通過鼓入空氣除去。氧化反應完成后送入粗結晶器,攪拌冷卻到24~30℃,排入沉淀槽進一步結晶,然后離心分離。母液經蒸發濃縮供下批循環使用。粗產物用母液和熱水再溶解,經脫脂、分離、過濾和重結晶,最 終 產 品 純 度 達99%以 上,草 酸 二 水 化 合 物 產 率 為63%~65%。
5.在實驗室用的烘箱中,放盡可能多的瓦盤或搪瓷盤。將烘箱內的溫度調節至98一99℃。當溫度恒定時,取出盤子,迅速在其中鋪一層(厚度不超過3一4mfn)研細了的結晶草酸。然后迅速地放回烘箱內;在幾分鐘內溫度稍有降低。當烘箱內重新達到調節好的溫度后,再烘2小時。稍冷,取出產物,如果有結塊的現象,研碎,迅速裝入瓶中。從100克結晶草酸可得無水草酸69-70克〔為理論產量的96-98%。用標準堿液滴定,證明產物純度為99.5-100%
此外,無水草酸還可利用四氯化碳揮發時帶走結品草酸的水而制得。此法裝置較復雜,脫水時間長。
6. 煙草:FC,50;BU,39;FC,38。
用途
1.草酸主要用于生產抗菌素和冰片等藥物以及提煉稀有金屬的溶劑、染料還原劑、鞣革劑等。此外,草酸還可用于合成各種草酸酯、草酸鹽和草酰胺等產品,而以草酸二乙酯及草酸鈉、草酸鈣等產量最大。草酸還可用于鈷-鉬-鋁催化劑的生產、金屬和大理石的清洗及紡織品的漂白。用于合成脲醛樹脂、三聚氰胺甲醛樹脂等膠黏劑的酸度調節劑。醫藥工業用于制造土霉素、金霉素等藥物。
2.主要用作還原劑和漂白劑,印染工業的媒染劑,亦用于提煉稀有金屬,合成各種草酸酯、草酸鹽和草酰胺等。
3.用作合成脲醛樹脂、三聚氰胺甲醛樹脂等膠黏劑的酸度調節劑。還可加入聚乙烯醇縮甲醛水溶性膠黏劑中提高干燥速度和粘接強度。為重要的有機合成原料,用于生產各種草酸鹽、草酸酯、草酰胺、對苯二酚、季戊四酯、沒食子酸等產品。醫藥工業用于制造金霉素、土霉素、四環素、鏈霉素、冰片、維生素B12、苯巴比妥等藥物。印染工業用作顯色助染劑、漂白劑。塑料工業用于生產聚氯乙烯、氨基塑料、脲醛塑料。冶金工業用于生產高純鎳、炭精棒及沉淀稀土金屬。還用作金屬洗滌處理劑、鞣革劑、螯合劑、催化劑、厭氧膠黏劑及丙烯酸酯快固膠的阻聚劑、機加工除銹劑、電鍍絡合劑、木材漂白、大理石清洗和油脂精制等。
4.在化妝品中可用作洗發水的添加劑;主要用于化學工業產品制造,醫藥工業用以制造抗生素等藥品,印染工業、皮革工業用途廣泛;油脂化學中用作松油醇、甘油及硬脂酸酯的精制劑等;此外在鋁制品加工、硬質合金制作中都有應用。
安全信息
危險運輸編碼:UN3261 8/PG 3
危險品標志: 有害
有害
安全標識:S23 S26 S27 S24/25 S36/S37/S39
文獻
1. Chadrasekhar, S.; Gopalaiah, K. Tetrahedron Lett., 2003, 44, 7437. 2. Weinstein, B.; Fenselau, A. H. J. Org. Chem., 1965, 30, 3209. 3. Andersen, N. H.; Uh, H.-S. Synth. Commun., 1973, 3, 125. 4. Martin, V. A.; Murray, D. H.; Pratt, N. E.; Zhao, Y.-b.; Albizati, K. F. J. Am. Chem. Soc., 1990, 112, 6965.. 5. Bartlett, P. A.; Meadows, J. D.; Ottow, E. J. Am. Chem. Soc., 1984, 106, 5304. 6. Comins, D. L.; Hong, H. J. Am. Chem. Soc., 1991, 113, 6672. 7. Giles, M.; Hadley, M. S.; Gallagher, T. J. Chem. Soc, Chem. Commun., 1990, 1047. 8.參考書:現代有機合成試劑<性質、制備和反應>;胡躍飛 付華 編著;化學工業出版社;ISBN 7-5025-8542-7
備注
暫無
表征圖譜
統計數據
共收錄化學品數據
147579 條




 滬公網安備 31010602001115號
滬公網安備 31010602001115號