鈀 Palladium

結(jié)構(gòu)式
| 物競編號 | 0004 |
|---|---|
| 分子式 | Pd |
| 分子量 | 106.4 |
| 標簽 | 純元素, 催化劑, 電子高純單質(zhì)原料及中間體 |
編號系統(tǒng)
CAS號:7440-05-3
MDL號:MFCD00011167
EINECS號:231-115-6
RTECS號:RT3480500
BRN號:暫無
PubChem號:暫無
物性數(shù)據(jù)
1. 性狀:銀白色金屬。(面心立方結(jié)晶)。延展性強。
2. 密度(g/mL,20℃):12.02
3. 相對蒸汽密度(g/mL,空氣=1):未確定
4. 熔點(oC):1554
5. 沸點(oC,常壓):2970
6. 沸點(oC,5.2kPa):未確定
7. 折射率:未確定
8. 閃點(oC):未確定
9. 比旋光度(o):未確定
10. 自燃點或引燃溫度(oC):未確定
11. 蒸氣壓(mmHg,25oC):未確定
12. 飽和蒸氣壓(kPa, oC):未確定
13. 燃燒熱(KJ/mol):未確定
14. 臨界溫度(oC):未確定
15. 臨界壓力(KPa):未確定
16. 油水(辛醇/水)分配系數(shù)的對數(shù)值:未確定
17. 爆炸上限(%,V/V):未確定
18. 爆炸下限(%,V/V):未確定
19. 溶解性:溶于王水、熱硝酸、硫酸,微溶于鹽酸,不溶于冷水和熱水。
毒理學數(shù)據(jù)
1、其它多劑量毒性:大鼠經(jīng)口TDLo:9100mg/kg/26W-I,對眼睛和皮膚有刺激作用。
生態(tài)學數(shù)據(jù)
該物質(zhì)對環(huán)境有危害,應(yīng)特別注意對水體的污染。
分子結(jié)構(gòu)數(shù)據(jù)
1、摩爾折射率:無可用的
2、摩爾體積(cm3/mol):無可用的
3、等張比容(90.2K):無可用的
4、表面張力(dyne/cm):無可用的
5、介電常數(shù):無可用的
6、極化率(10-24cm3):無可用的
7、單一同位素質(zhì)量:105.903483 Da
8、標稱質(zhì)量:106 Da
9、平均質(zhì)量:106.42 Da
計算化學數(shù)據(jù)
1、 疏水參數(shù)計算參考值(XlogP):
2、 氫鍵供體數(shù)量:0
3、 氫鍵受體數(shù)量:0
4、 可旋轉(zhuǎn)化學鍵數(shù)量:0
5、 互變異構(gòu)體數(shù)量:
6、 拓撲分子極性表面積(TPSA):0
7、 重原子數(shù)量:1
8、 表面電荷:0
9、 復雜度:0
10、 同位素原子數(shù)量:0
11、 確定原子立構(gòu)中心數(shù)量:0
12、 不確定原子立構(gòu)中心數(shù)量:0
13、 確定化學鍵立構(gòu)中心數(shù)量:0
14、 不確定化學鍵立構(gòu)中心數(shù)量:0
15、 共價鍵單元數(shù)量:1
性質(zhì)與穩(wěn)定性
1.避免與氧化物,強酸,堿,鹵素接觸。溶于王水、 熱硝酸、硫酸,微溶于鹽酸,不溶于冷水和熱水。超細鈀粉:灰黑色粉末。微米級粒度的鈀粉,有鱗片狀、無定形和球狀。鱗片狀鈀粉的松裝密度0.67~0.95g/cm3。搖實密度1.6~2.00g/cm3。平均粒度0.35~0.48μm,比表面積3.3~5.2m2/g。電性能穩(wěn)定,對氫吸附能力大。其粉體遇高溫、明火能燃燒。與甲酸或四氫硼酸鈉反應(yīng)放出氫氣。與異丙醇發(fā)生劇烈反應(yīng)。
在空氣中加熱至800℃,生成暗淡無光的氧化膜,高于此溫度即分解。能大量吸附多種氣體,尤其是H2。室溫下能抗氫氟酸、磷酸、鹽酸和硫酸的侵蝕。溶于王水、熱HNO3、H2SO4。微溶于鹽酸。
貯存方法
儲存于陰涼、通風的庫房。遠離火種、熱源。應(yīng)與酸類、鹵素分開存放,切忌混儲。配備相應(yīng)品種和數(shù)量的消防器材。儲區(qū)應(yīng)備有合適的材料收容泄漏物。應(yīng)貯存在干燥、清潔的庫房內(nèi)。
合成方法
1.工業(yè)生產(chǎn)可從礦石用干法制造;亦可以銅、鎳的硫化礦制取銅、鎳的生產(chǎn)過程中生成的副產(chǎn)物作為原料,用濕法冶煉制得。
濕法把已提取鎳、銅后的殘留組分作為原料,加入王水進行抽提,過濾,向濾液中加入氨和鹽酸進行反應(yīng),生成氯鈀酸銨沉淀。經(jīng)精煉,過濾,把氯鈀酸銨用氫氣還原,制得約99.95%鈀成品。
超細鈀粉制法:化學處理金屬鈀制取球形超細鈀粉。
2.在PdCl2或Na2PdCl4中加入NH4Cl使可能存在的微量Pt生成(NH4)2PtCl6沉淀。濾液中加入過量氨水并煮沸,必要時再次過濾。然后用鹽酸酸化,生成很純的黃色[PdCl2(NH3)2]沉淀。若所得沉淀呈暗濁的黃色,其中即含有少量不溶于冷氨水的[RhCl(NH3)5]Cl2。可將沉淀與氨水共煮,取出濾液,再次用鹽酸酸化,可得亮黃色的很純的[PdCl2(NH3)2]晶體。將晶體在H2氣流中灼燒還原,得到淺灰色的海綿鈀。
3.工業(yè)生產(chǎn)可以礦石用干法制造;亦可以銅、鎳的硫化礦制取銅、鎳的生產(chǎn)過程中生成的副產(chǎn)物作為原料,用濕法冶煉制得。
濕法 將已提取鎳、銅后的殘留組分作為原料,加入王水進行抽提、過濾,向濾液中加入氨和鹽酸進行反應(yīng),生成氯化鈀酸銨沉淀。經(jīng)精煉、過濾,將氯化鈀酸銨用氫氣還原,制得約99.95%的鈀成品。
4.在0.443克(2 .5摩爾)氯化把溶于40毫升絕對甲醇(或其它溶劑)的溶液中,在攪拌和室溫下,5~10分鐘內(nèi)分次加入0.19克(5.0毫摩爾)粉狀氫化硼鈉。繼續(xù)攪拌20分鐘,或直到不再放出氣體為止。攪拌停止后,黑色的反應(yīng)產(chǎn)物很快就沉降下來用傾倒并洗滌的辦法更換溶劑兩次。此催化劑可以直接使用,或貯放在有塞瓶中的液體下面。
用途
1.用于電器儀表、精密合金等。電氣儀表,化學工業(yè)及制造精密合金等工業(yè)用。主要用于制催化劑,還用于制造牙科材料、手表和外科器具等。用于制合金、鐘表軸承及零件、鏡面、加氫催化劑等。超細鈀粉用途:產(chǎn)品主要用于制作厚膜導體漿料及凈化材料。
2.商品化的鈀催化劑本篇介紹三種:①鈀-硫酸鋇催化劑,也叫羅森蒙德催化劑;②鈀-碳催化劑,黑色粉末或者是含有0.5%~30%鈀的小球,不溶于所有的有機溶劑和酸性溶液;③鈀-碳酸鈣-乙酸鉛催化劑,異相催化劑,不溶于水合有機溶劑。
①鈀-硫酸鋇催化劑
鈀催化的將酰氯轉(zhuǎn)變?yōu)槿┑臍浠磻?yīng),也稱為“羅森蒙德反應(yīng)” (式1)[1]。該反應(yīng)初期的方法,都是采用將氫氣通入到酰氯的二甲苯或甲苯溶液中來完成的。盡管這一方法能夠適用于大部分酰氯化合物,但是進一步的還原反應(yīng)如將醛轉(zhuǎn)變?yōu)榇迹约斑M一步形成酯、醚和烴類化合物等副反應(yīng)會嚴重影響羅森蒙德反應(yīng)的產(chǎn)率。
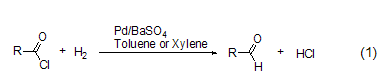
后續(xù)研究發(fā)現(xiàn)了一種更為可行的操作方法,即在二甲苯或甲苯溶劑中,采用鈀/硫酸鋇作催化劑,采用喹啉-硫作調(diào)節(jié)劑,通入氫氣后回流反應(yīng)能夠高產(chǎn)率地實現(xiàn)萘酰氯的氫化反應(yīng) (式2)[2]。
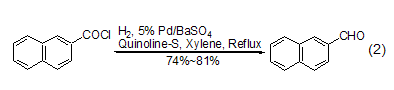
為了進一步克服傳統(tǒng)羅森蒙德反應(yīng)中使用的高溫以及通氫氣的危險,將鈀/硫酸鋇替換為鈀/碳,并加入無水乙酸鈉作為鹽酸的吸收劑,能夠在溫和條件下實現(xiàn)密閉體系的羅森蒙德反應(yīng) (式3)[3],從而為其工業(yè)化應(yīng)用打下了良好的基礎(chǔ)。
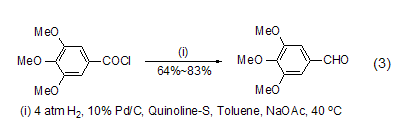
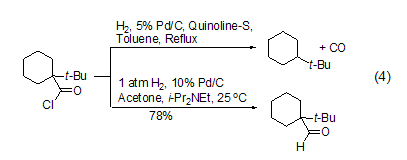
在反應(yīng)體系中加入鹽酸吸收劑如N,N-二甲基乙酰胺、乙酸鈉和乙基二異丙基胺等都能有效促進反應(yīng)的進行,能夠在溫和條件下實現(xiàn)立體禁阻的酰氯底物的氫化反應(yīng),如采用傳統(tǒng)羅森蒙德反應(yīng)方法,1-叔丁基環(huán)己酰氯的氫化反應(yīng)得到的主要是叔丁基環(huán)己烷產(chǎn)物,而加入鹽酸吸收劑乙基二異丙基胺后,能夠高產(chǎn)率得到相應(yīng)的醛化合物 (式4)[4]。
近年來的研究表明,不管是傳統(tǒng)方法還是新方法,在實現(xiàn)酰氯到醛的轉(zhuǎn)換中都是非常成功的,如采用傳統(tǒng)方法,能夠有效實現(xiàn)不飽和酰氯到不飽和醛的轉(zhuǎn)換 (式5)[5]。
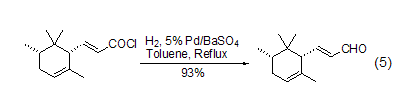
②鈀-碳催化劑
Pd/C能夠催化氫化烯烴、炔烴、酮、腈、亞胺、疊氮化物、硝基化合物、苯環(huán)以及雜環(huán)芳香化合物;可用于環(huán)丙烷、苯基衍生物、環(huán)氧化物、肼以及鹵化物的氫解;同時也可以用于芳香化合物脫氫和醛的去酰基化反應(yīng)。
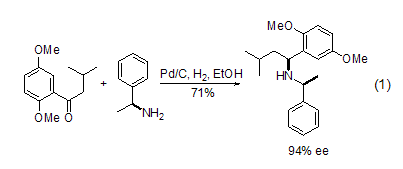
碳氮鍵 Pd/C在酸性或者銨溶液中,可以將腈氫化為一級胺。在沒有酸性或者銨溶液時,將得到一級和二級胺的混合物。在酸性溶液中可以氫化得到醛或者醇。同腈一樣,在酸性條件下,肟也能烷基化反應(yīng)得到二級胺,用α-甲基苯胺作為手性輔助劑,可以實現(xiàn)對中間體亞胺的高度非對映異構(gòu)選擇性還原 (式1)[6]。這種方法提供了一種得到含氮雜環(huán)的很好途徑。
Pd/C也能用于一些其它胺的前體,比如疊氮化物的還原烷基化反應(yīng)。例如,呋喃糖環(huán)被開環(huán)后再關(guān)環(huán),可以形成哌啶環(huán) (式2)[7]。而吡喃基疊氮化合物可以發(fā)生類似的反應(yīng)得到氮雜七元環(huán)。
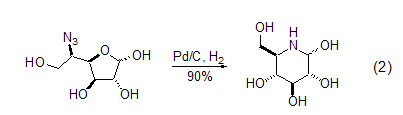
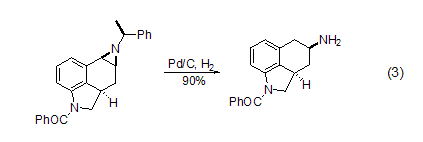
苯胺能被氫化得到較少烷基化的胺。碳氮鍵在轉(zhuǎn)移氫化和常規(guī)氫化的條件下都能夠斷裂。烯丙胺也可以在Pd/C催化下發(fā)生去烯丙基化反應(yīng)。1-氮雜環(huán)丙烷氫解可以得到開環(huán)胺,而且活性強的碳氮鍵能選擇性地優(yōu)先裂解 (式3)[8]。
碳鹵鍵 芳香族鹵化物(Cl, I, Br)可以用Pd/C催化氫化。反應(yīng)中一般要用適量堿中和形成的酸。在沒有酸中和劑的情況下,脫鹵非常緩慢,甚至可能停止反應(yīng) (式4)[9]。
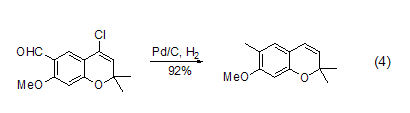
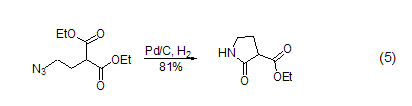
氮氮鍵 疊氮、重氮化合物可以在Pd/C作用下還原為胺。這些基團也可以看作是潛在的胺,發(fā)生氫化反應(yīng)后再與分子內(nèi)和對胺敏感的基團反應(yīng),得到不同的胺 (式5)[10]。
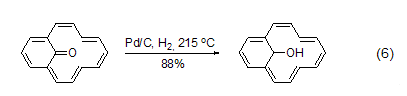
脫氫 在高溫下,對碳環(huán)和雜環(huán)芳香化合物而言,Pd/C也是一種有效的脫氫試劑。烯酮可以轉(zhuǎn)化為酚 (式6)[11]。
最近發(fā)現(xiàn)了一種新的復合材料——碳納米纖維,由于碳納米纖維有更大的比表面積,所以更適合作為金屬催化劑的載體。在液相條件下,應(yīng)用碳納米纖維/鈀催化劑,可以使四氫化萘發(fā)生脫氫化反應(yīng)生成萘 (式7)[12]。
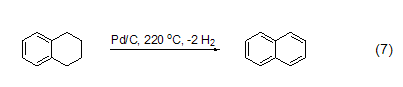
③鈀-碳酸鈣-乙酸鉛催化劑
鉛毒化的碳酸鈣負載鈀催化劑 (Lindlar催化劑)[13]是有機合成中最常用的異相氫化催化劑之一。Lindlar催化劑可以催化氫化還原多種有機官能團,例如:將芳環(huán)取代的硝基還原成為胺,但是與其它試劑相比較沒有明顯的特色。該試劑最獨特的反應(yīng)是高度選擇性地將炔鍵還原至順式雙鍵。
炔鍵是有機化合物中最容易被還原的官能團之一,可以被部分還原生成烯烴,也可以徹底還原生成烷烴。如果被部分還原生成烯烴,可能得到順式烯烴或者反式烯烴。對大多數(shù)已知的過渡金屬催化劑來講,不僅使產(chǎn)物停留在烯烴非常困難,而且缺乏立體選擇性。Lindlar催化劑通過“毒化”和“去活”使其還原能力變得非常溫和,高度選擇性地將炔鍵還原至順式雙鍵。
使用Lindlar催化劑催化氫化炔鍵至雙鍵的反應(yīng)一般在室溫和常壓下進行,高純氫氣是最方便的氫源。反應(yīng)一般在數(shù)分鐘至數(shù)小時內(nèi)完成,主要取決于底物的結(jié)構(gòu)。反應(yīng)的后處理非常簡單,產(chǎn)物的產(chǎn)率一般很高或者接近定量。由于反應(yīng)條件溫和,該反應(yīng)對其它官能團一般不產(chǎn)生明顯的影響 (式1,式2)[14~17]。
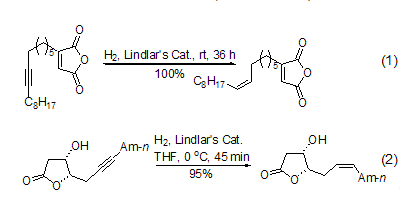
在反應(yīng)體系中加入催化量的吡啶或者喹啉可以進一步使催化劑“去活”,增大生成烯烴的選擇能力。在含有雙鍵或者含有多個雙鍵的分子中,高選擇性和高產(chǎn)率地將炔鍵催化氫化至順式雙鍵最能夠顯示該試劑的優(yōu)越性,特別適合復雜天然產(chǎn)物的合成 (式3)[18~20]。它可以將分子中多個炔鍵同時轉(zhuǎn)化成為相應(yīng)的順式雙鍵,使得復雜的合成變的異常簡單 (式4)[21]。
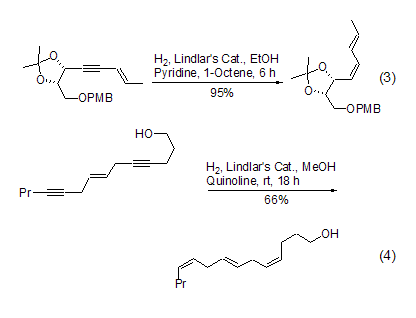
在Lindlar催化劑的反應(yīng)中,含有游離胺的炔烴化合物在選擇性方面較差。如果在反應(yīng)體系中加入適量的二亞乙基三胺,便可得到非常滿意的結(jié)果 (式5)[22]。
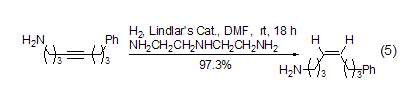
安全信息
危險運輸編碼:UN 3089 4.1/PG 2
危險品標志: 易燃
易燃  有毒
有毒  刺激
刺激
安全標識:暫無
危險標識:暫無
文獻
1. Rylander, P. N. Hydrogenation Methods, Academic: New York, 1985. 2. Hershberg, E. B.; Cason, J. Org. Synth., Coll. Vol. 1985, 3, 551. 3. Wagner, D. P.; Gurien, H.; Rachlin, A. I. Ann. N. Y. Acad. Sci., 1970, 172, 186. 4. Peters, J. A.; van Bekkum, H. Recl. Trav. Chim. Pays-bas, 1971, 90, 1323. 5. Maurer, B.; Hauser, A.; Froidevaux, J.-C. Helv. Chim. Acta, 1989, 72, 1400. 6. Bringmann, G.; Kunkel, G.; Geuder, T. Synlett, 1990, 5, 253. 7. Dax, K.; Gaigg, B.; Grassberger, V.; Kolblinger, B.; Stutz, A. E. J. Carbohydr. Chem., 1990, 9, 479. 8. Martinelli, M. J.; Leanna, M. R.; Varie, D. L.; Peterson, B. C.; Kress, T. J.; Wepsiec, J. P.; Khau, V. V. Tetrahedron Lett., 1990, 31, 7579. 9. (a) Eszenyi, T.; Timar, T. Synth. Commun., 1990, 20, 3219. (b) Comins, D. L.; Weglarz, M. A. J. Org. Chem., 1991, 56, 2506. 10. (a) Lohray, B. B.; Ahuja, J. R. Chem. Comm., 1991, 95. (b) Lindstrom, K. J.; Crooks, S. L. Synth. Commun., 1990, 20, 2335. (c) Machinaga, N.; Kibayashi, C. Tetrahedron Lett., 1990, 31, 3537. (d) Chen, L.; Dumas, D. P.; Wong, C. H. J. Am. Chem. Soc., 1992, 114, 741. 11. Nelson, P. H.; Nelson, J. T. Synthesis, 1991, 192. 12. (a) Dung, T. P.; Morisaka, H.; Satoh, T.; Miura, M.; Nomura, M.; Matsui, H.; Yamaguchi, C.; Energy Fuels, 2003, 17, 658. (b) Dung, T. P.; Satoh, T.; Miura, M.; Nomura, M. Energy Fuels, 2005, 19, 731. 13. Lindlar, H. Helv. Chim. Acta, 1952, 35, 446. 14. Qin, D.; Byun, H.-S.; Bittman, R. J. Org. Chem., 1996, 61, 8709. 15. Leeuwenburgh, M.A.; Kulker, C.; Duynstee, H. I.; Overkleeft, H. S.; Van der Marel, G. A.; Van Boom, J. H. Tetrahedron, 1999, 55, 8253. 16. Kates, M. J.; Schauble, J. H.; J. Org. Chem., 1996, 61, 4164. 17. Han, X.; Crane, S. N.; Corey, E. J. Org. Lett., 2000, 2, 3437. 18. Kumar, P.; Naidu, S. V.; Gupta, P. J. Org. Chem., 2005, 70, 2843. 19. Ivanova, D. I.; Eremin, S. V.; Shvets, V. I. Tetrahedron, 1996, 52, 9581. 20. Wipf, P.; Graham, T. H. J. Am. Chem. Soc., 2004, 126, 15346. 21. Akira Tai, F.; Matsumura, H. C. C. J. Org. Chem., 1969, 34, 2180. 22. Campos, K. R.; Cai, D.; Journet, M.; Kowal, J. J.; Larsen, R. D.; Reider, P. J. J. Org. Chem., 2001, 66, 3634. 23.參考書:現(xiàn)代有機合成試劑<性質(zhì)、制備和反應(yīng)>;胡躍飛 付華 編著;化學工業(yè)出版社;ISBN 7-5025-8542-7
備注
53092-86-7
表征圖譜
統(tǒng)計數(shù)據(jù)
共收錄化學品數(shù)據(jù)
147579 條




 滬公網(wǎng)安備 31010602001115號
滬公網(wǎng)安備 31010602001115號