鈉 Sodium

結構式
| 物競編號 | 000G |
|---|---|
| 分子式 | Na |
| 分子量 | 23 |
| 標簽 | 曹打, Natrium, 純元素, 還原劑, 脫水劑, 冷卻劑, 電子高純單質原料及中間體 |
編號系統
CAS號:7440-23-5
MDL號:MFCD00085307
EINECS號:暫無
RTECS號:VY0686000
BRN號:暫無
PubChem號:24871915
物性數據
1.性狀:銀白色柔軟的輕金屬,常溫下質軟如蠟。[1]
2.熔點(℃):97.8[2]
3.沸點(℃):881.4~892[3]
4.相對密度(水=1):0.97[4]
5.飽和蒸氣壓(kPa):0.16(440℃)[5]
6.燃燒熱(kJ/mol):-209.5[6]
7.臨界壓力(MPa):34.7[7]
8.辛醇/水分配系數:-0.77[8]
9.引燃溫度(℃):>115[9]
10.溶解性:不溶于煤油、乙醚、苯,溶于液氨。[10]
毒理學數據
1.急性毒性[11] LD50:4000mg/kg(小鼠腹腔)
2.刺激性 暫無資料
生態學數據
1.生態毒性 暫無資料
2.生物降解性 暫無資料
3.非生物降解性 暫無資料
4.其他有害作用[12] 該物質對環境有危害,應特別注意對水體的污染。
分子結構數據
1、摩爾折射率:無可用的
2、摩爾體積(cm3/mol):無可用的
3、等張比容(90.2K):無可用的
4、表面張力(dyne/cm):無可用的
5、介電常數:無可用的
6、極化率(10-24cm3):無可用的
7、單一同位素質量:22.98977 Da
8、標稱質量:23 Da
9、平均質量:22.9898 Da
計算化學數據
1.疏水參數計算參考值(XlogP):無
2.氫鍵供體數量:0
3.氫鍵受體數量:0
4.可旋轉化學鍵數量:0
5.互變異構體數量:無
6.拓撲分子極性表面積0
7.重原子數量:1
8.表面電荷:0
9.復雜度:0
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:1
性質與穩定性
1.化學性質極活潑,能與許多有機物及無機物發生反應;與金屬或非金屬可直接化合,如與鉛生成鉛鈉合金、與汞生成鈉汞齊等。在空氣中急速氧化。燃燒時呈黃色火焰。與皮膚接觸易引起燒傷。 遇醇分解,不溶于醚和苯。常溫時為蠟狀,易用刀切開。其蒸氣帶有紫色,高溫時呈黃色,有極好的傳熱性。新切面有光澤,在空氣中氧化轉變為暗灰色。質軟而輕,在-20℃時變硬。遇水劇烈分解,生成氫氧化鈉和氫氣并產生熱量而自燃或爆炸。燃燒時發亮黃色火焰。與鹵素和磷直接化合。能還原許多氧化物成元素狀態,也能還原金屬氯化物。溶于液氨時成藍色溶液。在氨中加熱生成氨基鈉。溶于汞生成鈉汞齊。
2.穩定性[13] 穩定
3.禁配物[14] 強氧化劑、水、氧、酸類、鹵素(氯、氟、溴蒸氣)、磷、許多氧化物
4.避免接觸的條件[15] 空氣、潮濕空氣
5.聚合危害[16] 不聚合
貯存方法
儲存注意事項[17] 浸于煤油中。儲存于陰涼、干燥、通風良好的專用庫房內,遠離火種、熱源。庫溫不超過32℃,相對濕度不超過75%。包裝要求密封,不可與空氣接觸。應與氧化劑、酸類、鹵素等分開存放,切忌混儲。采用防爆型照明、通風設施。禁止使用易產生火花的機械設備和工具。儲區應備有合適的材料收容泄漏物。
合成方法
1.將含有氯化鈉33%、氯化鍶24%、氯化鈣28%、氯化鋇15%的四元點解質經干燥脫水精制后進行電解。
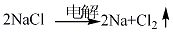
電解溫度控制在590-630 oC,槽電流強度24000A、槽電壓605-705V,陰極電流密度0.97A/cm2、陽極電流密度1A/cm2 。陰極收集到的粗鈉于120-150 oC進行熔化、澄清,上層清液即為精制鈉。下層殘液經蒸餾可回收鈉。陰極收集鈉需用氮氣防護。方法2:經精制后的二元電解質氫氧化鈉和碳酸鈉進行電解,溫度為285-305 oC,槽電流強度為2500A,槽電壓4.5-5V,陽極電流密度0.89A/cm2,陰極電流密度0.94-1.03A/ cm2。陰極手機的粗鈉于110-120 oC精制得成品。
2.用堿金屬的疊氮化合物在高真空下加熱分解,可以制得很純的不含氣體的堿金屬。
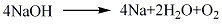
分解疊氮化合物的儀器裝置如圖I-8所示:
圖I-8 由疊氮化物制取堿金屬的裝置
1--分解反應管;2,3--冷阱;4--汞封活門;5,6--接受器;7,8--燒封處;9--盛裝制得的金屬用的安瓿
儀器是由在高溫下能夠耐堿腐蝕的硬質玻璃制成。為防止由于疊氮化合物的分解而引起裝置內的壓力突然升高,所有導管的直徑都應大于12~16mm。將疊氮化合物在瑪瑙研缽中研細,裝入分解反應管中,約占反應體積的1/4,使其均勻分布,然后將反應管與整個裝置熔接在一起,反應管放在電熱套中,將蓋斯勒(Geisler)放電管真空規與裝置妥善連接,兩個冷阱均浸入液化空氣中。開啟前級真空泵將裝置抽真空,并加熱至200℃,保溫12h,若放電管中無放電現象,說明裝置中達到并維持良好的真空狀。調高電爐的溫度使之逐漸升至275℃(疊氮化鈉的分解溫度),關閉汞封活門4,不致使疊氮化物分解時放出的N2將疊氮化物挾帶至接受器5中,與金屬鈉混雜在一起。一旦分解反應開始,裝置內的壓力會突然增高,為了減低壓力,要調低溫度,同時打開聯接緩沖容器的閥門(緩沖容器是一個用前級真空泵已抽成真空的8L的圓底燒瓶)。另外還要注意避免疊氮化合物因過熱而引起的爆炸性分解,而將裝置炸碎。當蓋斯勒放電管中放電現象消失時,標志分解反應完成。金屬鈉由反應管被蒸餾到接受器6中,在聯接管7處將反應管1熔封拉下,同時將導管8熔封,隔斷前級真空,開啟高真空泵,并打開汞封活門4,加熱接受器6,使更純的金屬鈉進入5。將5中的金屬鈉熔融,金屬鈉即流入安瓿9,最后將安瓿的熔封拉下,純金屬鈉即在真空安瓿中保存。
3.用鋯還原制取金屬鈉。因為在制備過程中不與氣體接觸,因此不含反復真空蒸餾也難于去除的氣體,可以保證金屬鈉的純度。所用原料為堿金屬的鉻酸鹽或重鉻酸鹽、鉬酸鹽、鎢酸鹽與鋯粉。Na2MoO4或Na2WO4與Zr粉的質量比為1∶4,將兩者的細粉末混合均勻,壓成小棒狀,放在一根已加熱排過氣體的石英管中,然后抽到高真空,加熱至約550℃(Na2WO4為450℃)A,B—燒瓶生分解反應。得到的金屬鈉凝附在石英管壁上溫度較低的部分。用鉬酸鈉Na2MoO4作原料時得到的金屬鈉的產率幾乎為理論量。
鈉的提純方法:用真空蒸餾法將金屬鈉提純。
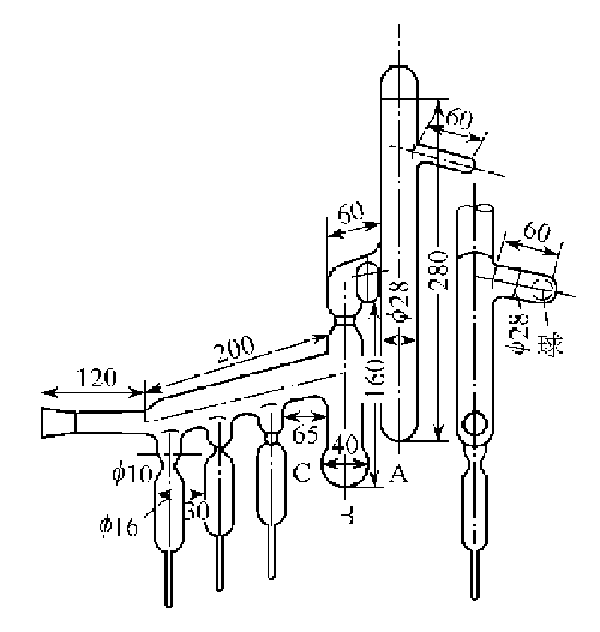
圖I-9 鈉的蒸餾裝置(圖中單位為毫米)A,B--燒瓶
將裝置抽真空,同時加熱1~2h使其干燥,然后充入無氧無水的高純氬氣。在干燥箱中除去金屬鈉表層的氧化物,截下燒瓶A的頂端將處理好的金屬鈉裝入燒瓶A中,熔封截口。抽真空,將真空度達到10-3~10-4Pa時加熱裝置,燒瓶A中的金屬鈉被蒸餾流向B中。燒瓶A中的殘留物用球封住。調節溫度使燒瓶B中的金屬鈉被蒸餾逐滴滴入安瓿中。蒸餾完畢,待裝置冷卻充入氬氣,將安瓿熔封切斷,金屬鈉即可在充有氬氣的安瓿中保存。
4.方法一:取比需用覺多一點的鈉放在廠’口錐形瓶或高燒杯中,用干燥二甲苯復蓋。將瓶加熱至鈉熔融而留下表面氧化物殼皮。移去熱源,溫和地旋動瓶子使鈉生成若干球體。然后將瓶在不太攪動的情況下冷卻以免鈉球又結在一起。在冷卻過程中向溶劑中通入氮氣。待鈉固化后,用一支尖銳的鐵絲或其它器械取出清潔的球休,迅速用濾紙拭干,放在容器中。氧化物殼皮中只含很少的鈉,傾去溶劑,用叔了醇處理使之與殘留的鈉相作用。在裝有短的回流冷凝器和強力機械攪拌器的2升兩頸燒瓶中,放400毫升干燥二甲苯和29克(1.26克原子)上述方法制得的金屬鈉球體或小塊。把燒瓶放在油浴中加熱,使金屬鈉完全熔融。開動攪拌器使金屬鈉粉碎成很小的顆粒,移去油浴,但繼續攪拌,直到金屬鈉凝固成很細的顆粒為止。然后傾出二甲苯。方法二:取100毫升園底燒瓶,安裝冷凝器,上附一鈉石灰干燥管。將2克切去外皮的潔凈金屬鈉切成小片,放入瓶內,并加入無水二甲苯復蓋,于油浴內加熱近佛騰。移去油浴,迅速將瓶取下,用塞子塞緊,并用雙層毛巾或布包裹,用力搖幾下,即成細小鈉砂。
用途
1.測定有機物中的氯,還原和氫化有機化合物,檢驗有機物中的氮、硫、氟。去除有機溶劑(苯、烴、醚)中的水分,除去烴中的氧、碘或氫碘酸等雜質。
2.制備鈉汞齊、醇化鈉、純氫氧化鈉、過氧化鈉、氨基鈉等。
3.冶金工業用于還原鈦、鋯等金屬氧化物。可用于生產汽油抗震劑四乙基鉛。煉油工業用作油品的脫硫劑。無機工業用于制造氰化鈉、過氧化鈉、氨基鈉等。在工業上用作強力還原劑和脫水劑。利用金屬鈉較好的導電性能,可制造電纜。添加于鋁中可增加硬度,用以制造車輛軸承合金。電光源工業用于制造單色光源鈉光燈。醫藥工業用于生產西力生、維生素B1、咖啡因及其他醫藥產品。也用于合成靛藍染料和染料中間體,還用作合成橡膠的催化劑。原子能工業用作原子能高速增殖爐的冷卻劑。
4.用作分析試劑。制備鈉化合物及合金。在工業上用作強力還原劑和脫水劑,合成橡膠的催化劑、石油的脫硫劑。
5.用于制造氰化鈉、過氧化鈉和多種化學藥物,也用作還原劑。[18]
安全信息
危險運輸編碼:UN 1428 4.3/PG 1
危險品標志: 易燃
易燃  腐蝕
腐蝕
文獻
[1~18]參考書:危險化學品安全技術全書.第一卷/張海峰主編.—2版.北京;化學工業出版社,2007.6 ISBN 978-7-122-00165-8
備注
暫無
表征圖譜
統計數據
共收錄化學品數據
147579 條




 滬公網安備 31010602001115號
滬公網安備 31010602001115號