疊氮基三甲基硅烷 Trimethylsilylazide

結構式
| 物競編號 | 0DMY |
|---|---|
| 分子式 | (CH3)3SiN3 |
| 分子量 | 115.21 |
| 標簽 | 三甲基硅疊, Azidotrimethylsilane, TMSA, TMSN3 |
編號系統
CAS號:4648-54-8
MDL號:MFCD00001986
EINECS號:225-078-5
RTECS號:暫無
BRN號:1903730
PubChem號:24849336
物性數據
1. 性狀:無色液體
2. 密度:0.88
3. 熔點(oC):不確定
4. 沸點(oC):97
5. 閃點(oC):不確定
6. 溶解性:溶于大多數有機溶劑,通常在CH2Cl2、THF和MeCN 中使用。
毒理學數據
主要的刺激性影響
在皮膚上面:可能引起發炎
在眼睛上面:可能引起發炎
致敏作用:沒有已知的敏化影響
生態學數據
通常對水是不危害的,若無政府許可,勿將材料排入周圍環境。
分子結構數據
暫無
計算化學數據
1.疏水參數計算參考值(XlogP):無
2.氫鍵供體數量:0
3.氫鍵受體數量:2
4.可旋轉化學鍵數量:1
5.互變異構體數量:無
6.拓撲分子極性表面積14.4
7.重原子數量:7
8.表面電荷:0
9.復雜度:97.2
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:1
15.共價鍵單元數量:1
性質與穩定性
1.常溫常壓下穩定, 無色液體。熔點-95℃,沸點95℃(96kPa),52-53℃(23.3kPa),相對密度0.87(20/4℃),折光率1.4140(20℃).
2.對濕氣敏感,在500 oC會發生分解。建議在干燥陰涼處保存,在通風櫥中操作和使用。
貯存方法
常溫,避光,通風干燥處,密封保存。
合成方法
1.通過三甲基氯硅烷與疊氮化鈉反應來制備[1]。
2.注意!此反應應在通風櫥中安全屏后面進行。如果反應系統不是絕對于燥,存在毒性的疊氮酸是可能的。
方法一:在1升三頸燒瓶上安裝攪拌器、帶千燥管的回流冷凝器和恒壓漏斗。先在烘箱中干燥,然后趁熱裝k: i..}好,立即用千燥氮氣清掃,氮氣可以方便地從加料的漏斗頂上通入。之后在瓶中盛81克( 1.25摩爾)疊氮化鈉500毫升所蒸的二甘醇二甲醚。在烘箱巾干燥一套簡單蒸餾儀器,趁熱用慢速氮氣流清掃。蒸餾瓶中盛112克只甲其氧硅烷。在蒸出大約2克初餾分之后,把其余的物料直接蒸餾.反應瓶的加料漏斗中。蒸餾時很方便地把氮氣Y從加料漏斗頂部卻下而接入蒸餾瓶中。蒸餾完后,拆去蒸餾儀器,把氮氣再接到加料漏斗頂上。然后把108.6克(1.0摩爾)三甲基氧硅烷迅速地加到疊氮化鈉漿中,此混合物在70℃攪拌的60小時,此時,氮氣流可以停止。加熱完成,再次通氮,將混合物冷至30℃。把加料漏斗和回流冷凝器換成兩支帶玻璃寒的氣體導入管,一支連接氮氣原,另一支則連接到標準真空阱,其容量至少150毫升。15-20毫米的真空原連接冷卻至一78℃的阱。然后把產物在30C芯餾到阱中,須稍稍加熱以保持30℃。在吸收操作蔡個過程中,應連續快速攪拌。在此條件下5小時內蒸完揮發性物。用氮氣使整個系統慢慢恢復到常壓,產物經過5厘米松針形分餾柱重蒸餾。從總量121克的粗閃蒸液得到}i}克初餾液和98克(85%)的純疊氮三甲硅烷,沸點95-99℃。蒸餾時,用但溫油浴把釜溫保持在135一140℃。釜底殘余物含19克二甘醇二甲醚和微最疊氮三甲硅烷。核磁共振譜(四氯化碳)測定產物的純度為98%.

方法二:布烘于的500毫升三頸燒瓶中,盛71.5克(1.1摩爾)疊氮化鈉和150毫升HMPT。在攪拌下1小時內加入108.6克(1.0摩爾)三甲基氯硅烷,加入的速度以反應漿狀物的紅橙色不消失為準。加完后,把滴液漏斗換成部分回流蒸餾頭,收集沸點 90一102℃的餾分,為濁狀液體。將釜底殘余物過濾,濾液可重用作下次制備的溶劑。濁液經過30厘米Widmer分餾柱蒸餾而精制。
用途
1.用于有機合成。用作中間體。
2.合成氮雜環。從酰氯制異氰酸酯。疊氮酸的代用試劑。
3.疊氮基三甲基硅烷 (TMSA) 是有機合成中應用非常廣泛的試劑之一。它可以看作是金屬疊氮化物的替代物,幾乎能夠發生金屬疊氮化物的所有反應。但是,TMSA能夠在許多有機溶劑中反應,所以更容易操作和獲得較好的結果。該試劑的反應性質來自于分子的兩個組成部分,以疊氮基所發生的反應具有較高的合成價值。
TMSA可以方便地與鹵代烴或者磺酸酯發生反應,生成相應的疊氮化合物 (式1)[2,3]。反應也可以在無催化劑存在的情況下進行,但一般需要較高的反應溫度。
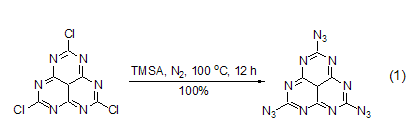
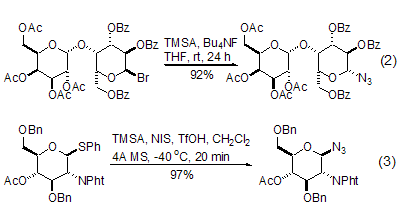
TMSA與那些容易生成碳正離子的縮醛衍生物的反應具有較高的合成價值,特別是在糖化學轉變中,用該方法可以方便地得到糖的疊氮化合物。鹵代縮醛或者硫代縮醛具有較高的反應活性 (式2,式3)[4,5],半縮醛或者半縮醛的羧酸酯可以在反應中原位轉化成為離去能力較強的官能團后再進行疊氮化反應[6,7]。
TMSA可以在金屬催化劑的作用下與環氧化合物發生開環反應,生成1(2)-羥基-2(1)-疊氮化合物。該產物進一步被還原就得到1(2)-羥基-2(1)氨基化合物,所以具有重要的合成價值。選擇適當的催化劑,該反應可以顯示出高度的立體選擇性 (式4)[8]。如果使用手性催化劑,可以實現高度的對映體選擇性[9]。
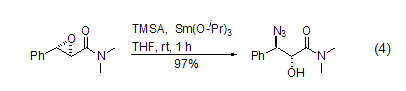
由于TMSA中的疊氮基具有1,3-偶極結構,所以很容易與缺電子炔烴發生[3+2]成環反應,生成三氮唑的衍生物 (式5)[10]。文獻報道,使用CuI為催化劑可以提高炔烴的反應活性[11]。如果反應底物為氰基的話,則生成四氮唑的衍生物[12~14]。該反應需要催化劑的存在下才能進行,許多路易斯酸金屬催化劑可以用于該目的。有時金屬疊氮化物不能夠進行的反應,TMSA 可能會給出很好的結果 (式6)[12]。

安全信息
危險運輸編碼:UN 1992 3/PG 2
危險品標志: 易燃
易燃  有毒
有毒
安全標識:S16 S45 S36/S37/S39
文獻
1. Nishiyama, K.; Yamaguchi, T. Synthesis, 1988, 106. 2. Lu, J.; Jayaprakash, K. N.; Schlueter, U.; Fraser-Reid, B. J. Am. Chem. Soc., 2004, 126, 7540. 3. Miller, D. R.; Swenson, D. C.; Gillan, E. G. J. Am. Chem. Soc., 2004, 126, 5372. 4. Ohlsson, J.; Larsson, A.; Haataja, S.; Alajaeaeski, J.; Stenlund, P.; Pinkner, J. S.; et al. Org. Biomol. Chem., 2005, 3, 886. 5. Pratt, M. R.; Bertozzi, C. R. J. Am. Chem. Soc., 2003, 125, 6149. 6. Bodine, K. D.; Gin, D. Y.; Gin, M. S. J. Am. Chem. Soc., 2004, 126, 1638. 7. Trost, B. M.; Yang, H.; Probst, G. D. J. Am. Chem. Soc., 2004, 126, 48. 8. Tosaki, S.-y.; Tsuji, R.; Ohshima, T.; Shibasaki, M. J. Am. Chem. Soc., 2005, 127, 2147. 9. Martinez, Luis E.; Leighton, James L.; Carsten, Douglas H.; Jacobsen, Eric N. J. Am. Chem. Soc., 1995, 117, 5897. 10. Roppe, J.; Smith, N. D.; Huang, D.; Tehrani, L.; Wang, B.; Anderson, J.; Brodkin, J. et al. J. Med. Chem., 2004, 47, 4645. 11. Jin, T.; Kamijo, S.; Yamamoto, Y. Eur. J. Org. Chem., 2004, 3789. 12. Terinek, M.; Vasella, A. Helv. Chim. Acta, 2003, 86, 3482. 13. Amantini, D.; Beleggia, R.; Fringuelli, F.; Pizzo, F.; Vaccaro, L. J. Org. Chem., 2004, 69, 2896. 14. Schulz, M. J.; Coats, S. J.; Hlasta, D. J. Org. Lett., 2004, 6, 3265. 15.參考書:現代有機合成試劑<性質、制備和反應>;胡躍飛 付華 編著;化學工業出版社;ISBN 7-5025-8542-7
備注
暫無
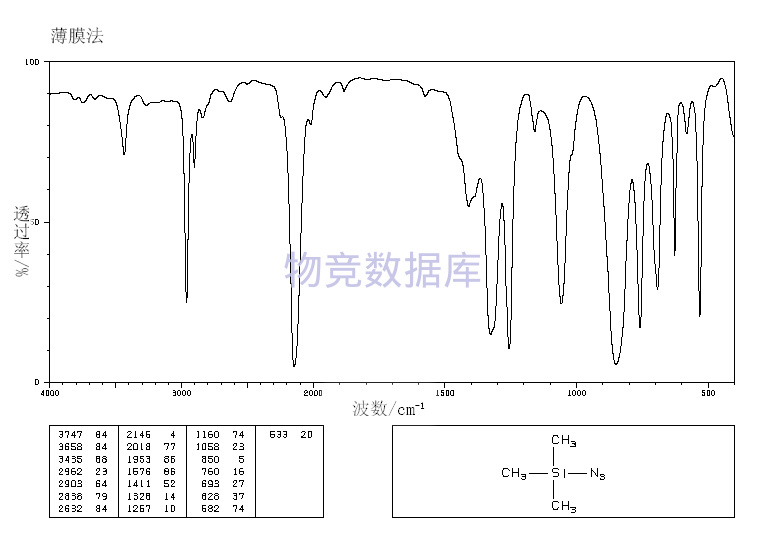
表征圖譜
統計數據
共收錄化學品數據
147579 條




 滬公網安備 31010602001115號
滬公網安備 31010602001115號