四正丁基氟化銨 Tetra-n-butylammonium fluoride
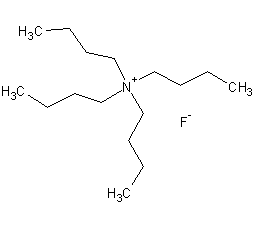
結構式
| 物競編號 | 04SU |
|---|---|
| 分子式 | C16H38FNO |
| 分子量 | 261.47 |
| 標簽 | 四-正丁基-氟化銨, 四正丁基氟化銨,四氫呋喃溶液, 四丁基氟化銨, 氟化四丁基胺, 氟化四丁銨, 四正丁基氟化銨, 1M SOLN. IN THF, 四正丁基氟化銨, 75% W/W AQ. SOLN., Tbaf, Tetranutylammonium fluoride hydrate, 1-Butanaminium,N,N,N-tributyl-,fluoride, n,n,n-tributyl-1-butanaminiufluoride, TBAF solution, Tetrabutylammonium fluoride solution, TetranbutylammoniumfluorideMsolninTHF, Tetrabutylammonium fluoride 1.0M solution in THF, 強堿試劑 |
編號系統
CAS號:429-41-4
MDL號:MFCD00011747
EINECS號:207-057-2
RTECS號:暫無
BRN號:3570522
PubChem號:24860012
物性數據
1.性狀:白色固體,極易吸濕。
2.密度(g/mL,25/4℃): 0.953
3.相對蒸汽密度(g/mL,空氣=1):不可用
4.熔點(oC):62-63
5.沸點(oC,常壓):不可用
6.沸點(oC,5.2kPa): 不可用
7.折射率: 1.456
8.閃點(oC): 不可用
9.比旋光度(o): 不可用
10.自燃點或引燃溫度(oC): 不可用
11.蒸氣壓(kPa,25oC): 不可用
12.飽和蒸氣壓(kPa,60oC): 不可用
13.燃燒熱(KJ/mol):不可用
14.臨界溫度(oC): 不可用
15.臨界壓力(KPa): 不可用
16.油水(辛醇/水)分配系數的對數值:不可用
17.爆炸上限(%,V/V):不可用
18.爆炸下限(%,V/V): 不可用
19.溶解性:溶于水、乙腈、THF。
毒理學數據
生態學數據
該物質對環境可能有危害,對水體應給予特別注意。
分子結構數據
暫無
計算化學數據
1.疏水參數計算參考值(XlogP):無
2.氫鍵供體數量:0
3.氫鍵受體數量:1
4.可旋轉化學鍵數量:12
5.互變異構體數量:無
6.拓撲分子極性表面積0
7.重原子數量:18
8.表面電荷:0
9.復雜度:116
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:2
性質與穩定性
該試劑必須在通風櫥中進行操作。
貯存方法
暫無
合成方法
1.通過氫氟酸水溶液與溴化四丁基銨的水溶液在離子交換樹脂中反應制備而成。反應完畢后,將樹脂用水反復洗滌,將洗脫液中水分蒸干即得油狀產物。
2.將氫氟酸水溶液(10%W/V》慢慢加到100毫升四正丁基氫氧化銨水溶激中,直到pH開始下降。用稀氫氟酸(3%)滴定到ph7所得淡棕色溶液用水稀釋至300毫升(約0.5M)。在冰中冷卻,析出籠形的(n-C4H9)4NF.32.8細小晶體。過濾,用冰水洗滌,最后在空氣中干燥。得72克,將母液濃縮,稀釋至約0.5M冷卻至0℃,還可以得第二份32克)籠形化合物。此籠形化合物可以在聚烯烴容器中O℃貯存幾星期。
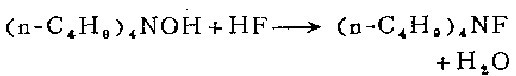
3.將25毫升工業品級10%四正丁基氫氧化按用稀的氫氟酸滴定至PH7-8.5。將溶液冷卻至10℃,生成白色籠形化合物。濾去液體,將籠形化合物用冷水洗兩次。在水泵抽吸下減去大部分水。所得糊狀物在30-40℃/0.5mml和五氧化二磷作用下于燥15-20小時。無水的四丁基氟化按在五氧化二磷上貯存。
用途
1. 裂解保護基團。甲硅烷基化和消去反應的催化劑。制備硒代醛和硫代醛。
2. 強堿試劑。氟化劑。醇的硅烷化催化劑。分裂硅烷醚。磷酸酯保護基的脫保護。Aldol縮合、烷化反應、羥基酰化反應等中的堿試劑。
3.氟化四丁基銨(TBAF)[1]在反應中可解離為(n-Bu)4N+與F–離子。它是一類常用的氟代試劑,可取代硝基、鹵素等基團,但其取代性能比氰基弱。它還是一類常用的去硅烷基試劑。
氟取代反應 TBAF可用于絕大部分的氟取代反應。例如:由2-硝基-4-溴-吡啶制備2-氟-4-溴-吡啶 (式1)[2]。溫和的反應條件和較高的反應產率是采用TBAF為氟代試劑的主要原因。
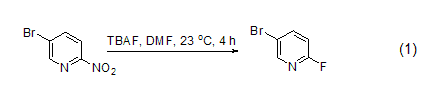
去硅烷基反應 TBAF廣泛用于去硅烷基的反應,這類反應通常可以在比較溫和的條件下進行,且產率很高,是切斷Si-O (式2)[3]、Si-N等共價鍵的常用方法,也適用于雜原子 (式3)[4]、羧基 (式4)[5] 的去硅烷基化反應。
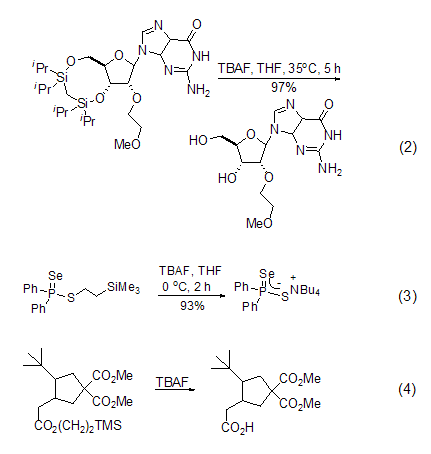
TBAF還是一種很強的脫烷硅化試劑,廣泛用于切斷Si-C鍵,特別是與雙鍵或三鍵相鄰的sp2-C-Si與sp3-C-Si鍵 (式5)[6]。若將TBAF與過渡金屬催化劑合用時,還可以使脫硅烷基反應與偶聯反應同時進行 (式6)[7]。
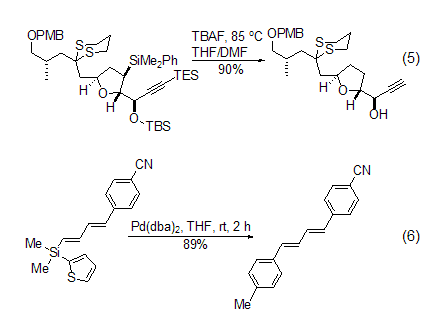
催化親核取代反應 TBAF可以催化二硝基苯上的親核取代反應,例如:對二硝基苯與三氟乙醇的反應 (式7)[8]。其催化機理是先用氟取代一個硝基,然后三氟乙醇的羥基親核進攻與氟相連的碳原子而得到目標產物。
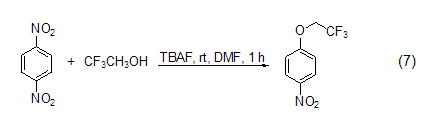
安全信息
危險運輸編碼:UN 1759 8/PG 2
危險品標志: 易燃
易燃  刺激
刺激  腐蝕
腐蝕
安全標識:S26 S27 S36/S37/S39
文獻
1. Amantini, D.; Beleggia, R.; Fringuelli, F.; Pizzo, F.; Vaccaro, L. J. Org. Chem., 2004, 69, 2896. 2. Kuduk, S. D.; DiPardo, R. M.; Bock, M. G. Org. Lett., 2005, 7, 577. 3. Wen, K.; Chow, S.; Sanghvi, Y. S.; Theodorakis, E. A. J. Org. Chem., 2002, 67, 7887. 4. Kimura, T.; Murai, T. J. Org. Chem., 2005, 70, 952. 5. Jonathan, C. T.; Carl, H. S.; Dennis, P. C. J. Am. Chem. Soc., 2005, 127, 5518. 6. Heitzman, C. L.; Lambert, W. T.; Mertz, E.; Shotwell, J. B.; Tinsley, J. M.; Va, P.; Roush, W. R. Org. Lett., 2005, 7, 2405. 7. Denmark, S. E.; Tymonko, S. A. J. Am. Chem. Soc., 2005, 127, 8004. 8. Tejero, I.; Huertas, I.; Gonzalez-Lafont, A.; Lluch, J. M.; Marquet, J. J. Org. Chem., 2005, 70, 1718. 9.參考書:現代有機合成試劑<性質、制備和反應>;胡躍飛 付華 編著;化學工業出版社;ISBN 7-5025-8542-7
備注
暫無
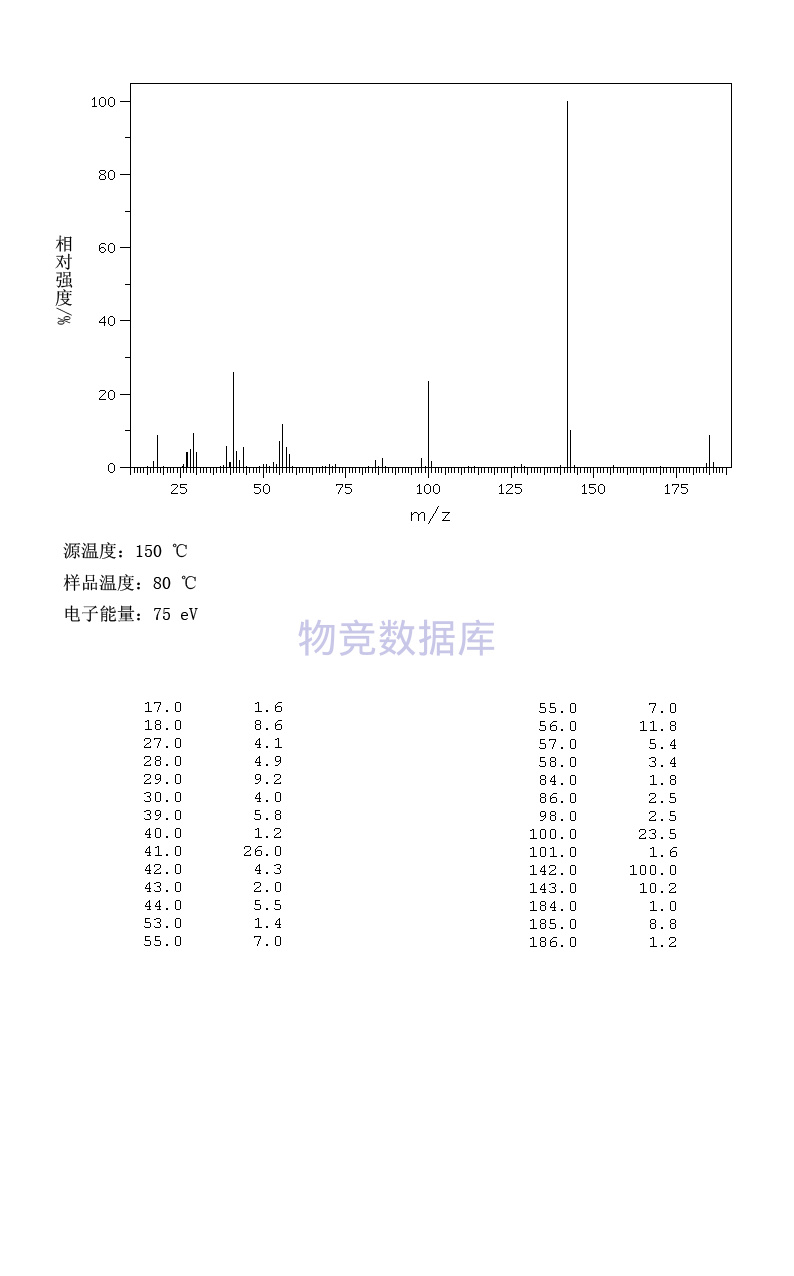
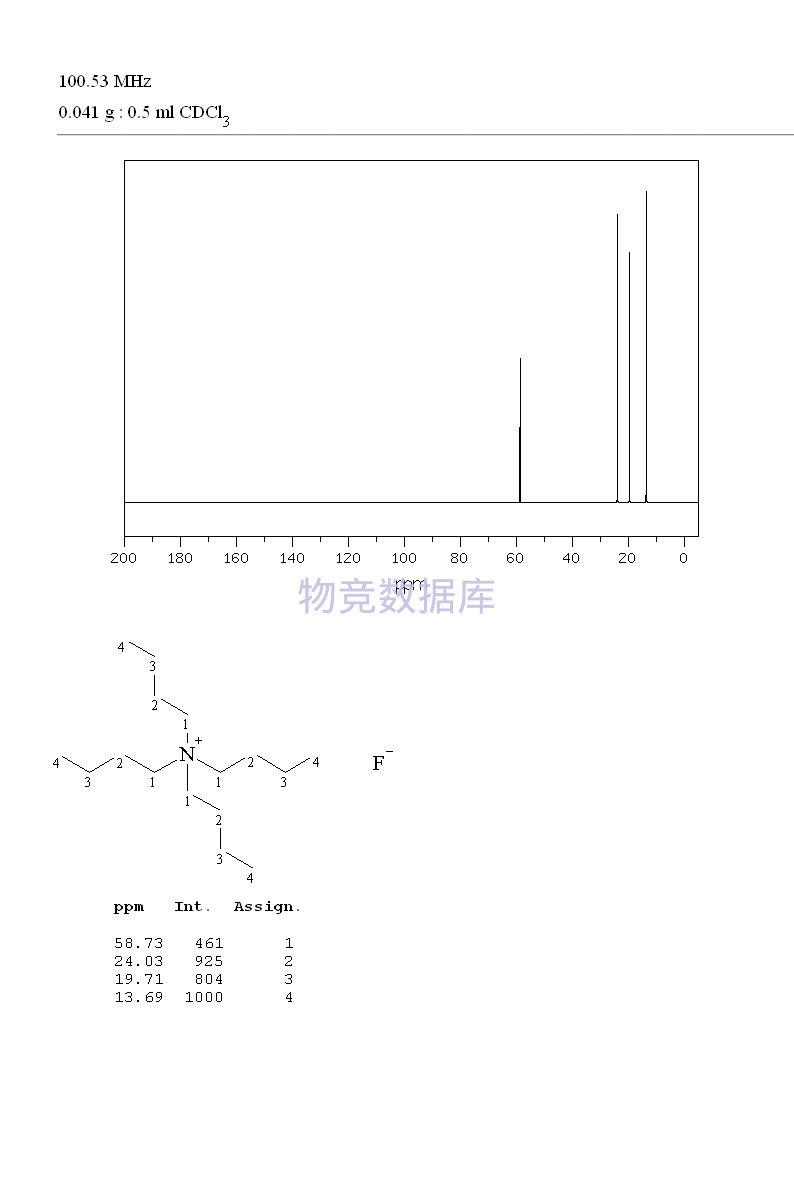
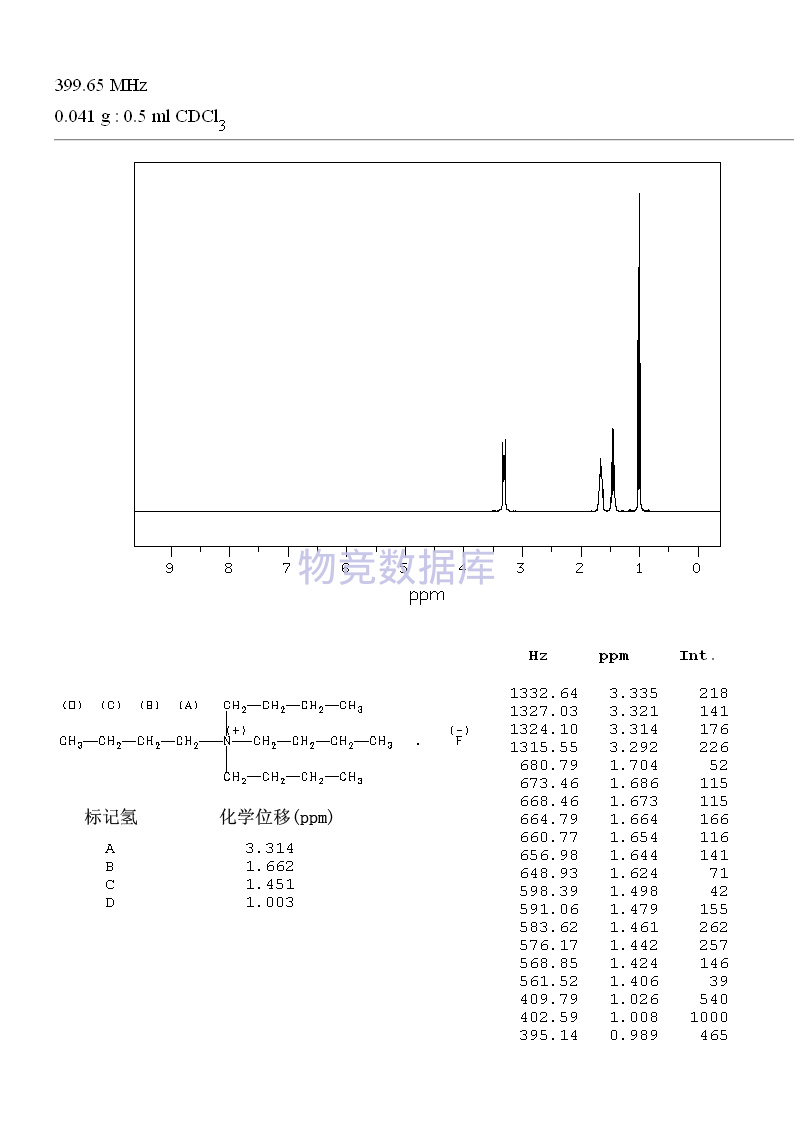
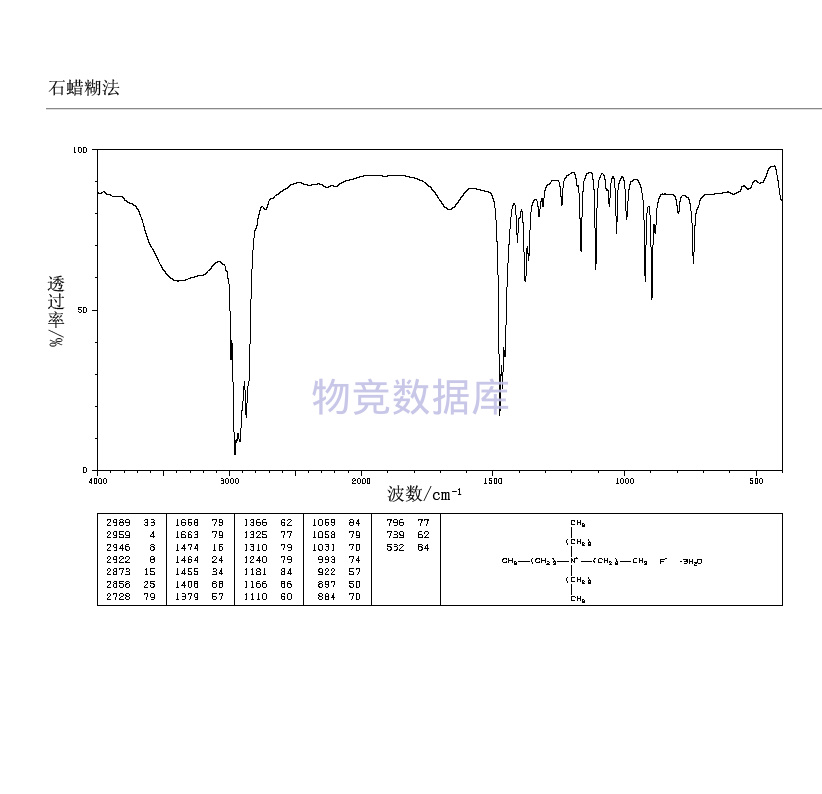
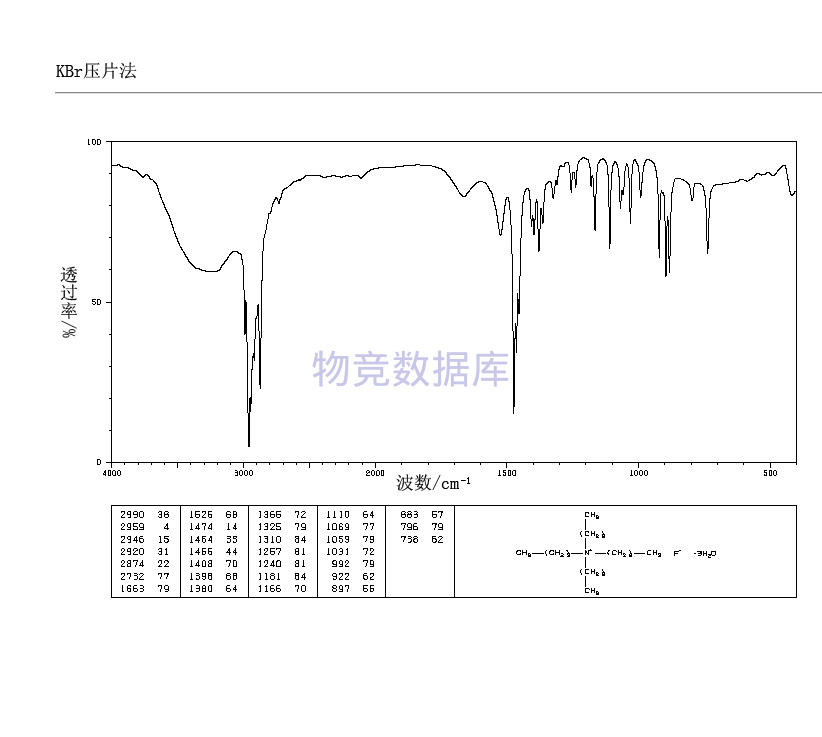
表征圖譜
統計數據
共收錄化學品數據
147579 條



 滬公網安備 31010602001115號
滬公網安備 31010602001115號