硫化氫 Hydrogen sulfide
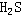
結構式
| 物競編號 | 174B |
|---|---|
| 分子式 | H2S |
| 分子量 | 34.08 |
| 標簽 | 還原劑, 催化劑 |
編號系統
CAS號:7783-06-4
MDL號:MFCD00011444
EINECS號:231-977-3
RTECS號:MX1225000
BRN號:3535004
PubChem號:24888266
物性數據
1.性狀:無色、有惡臭味的氣體[1]
2.pH值:4.5(1%水溶液)[2]
3.熔點(℃):-85.5[3]
4.沸點(℃):-60.3[4]
5.相對密度(水=1):1.54[5]
6.相對蒸氣密度(空氣=1):1.19[6]
7.飽和蒸氣壓(kPa):2026.5(25.5℃)[7]
8.臨界溫度(℃):100.4[8]
9.臨界壓力(MPa):9.01[9]
10.辛醇/水分配系數:0.23[10]
11.閃點(℃):-106[11]
12.引燃溫度(℃):260[12]
13.爆炸上限(%):46.0[13]
14.爆炸下限(%):4.0[14]
15.溶解性:溶于水、乙醇、二硫化碳、甘油、汽油、煤油等。[15]
毒理學數據
1、小鼠、大鼠吸入LC50:634×10-6/1h、712×10-6/1h;大鼠吸入LC50:444×10-6/4h。 硫化氫主要經呼吸道吸收,人吸入(70~150mg/m3)/(1~2h),出現呼吸道及眼刺激癥狀, 硫化氫可以麻痹嗅覺神經,吸2~5min后不再聞到臭氣。吸入(300mg/m3)/1h,6~8min出現眼急性刺激癥狀,稍長時間接觸引起肺水腫。吸入硫化氫能引起中樞神經系統的抑制,有時由于刺激作用和呼吸的麻痹而導致最終死亡。 在高濃硫化氫中幾秒內就會發生虛脫、休克,能導致呼吸道發炎、肺水腫,并伴有頭痛、胸部痛及呼吸困難。硫化氫貯存區附近不應有氧化可燃材料、酸或其他腐蝕性材料。避免暴露于高溫環境。
2.急性毒性[16] LC50:618mg/m3(444ppm)(大鼠吸入)
3.刺激性 暫無資料
4.亞急性與慢性毒性[17] 家兔吸入0.01mg/L,每天2h,3個月,引起中樞神經系統的機能改變,氣管、支氣管黏膜刺激癥狀,大腦皮層出現病理改變。小鼠長期接觸低濃度硫化氫,有小氣道損害。
5.其他[18] LCLo:600ppm(人吸入30min)
生態學數據
1.生態毒性[19]
TLm:0.0071~0.55mg/L(96h)(黑頭呆魚);0.0448~0.0478mg/L(96h)(藍鰓太陽魚)
2.生物降解性 暫無資料
3.非生物降解性 暫無資料
4.其他有害作用[20] 該物質對環境有危害,應注意對空氣和水體的污染。
分子結構數據
1、摩爾折射率:無可用的
2、摩爾體積(cm3/mol):無可用的
3、等張比容(90.2K):無可用的
4、表面張力(dyne/cm):無可用的
5、介電常數:無可用的
6、極化率(10-24cm3):無可用的
7、單一同位素質量:33.98772 Da
8、標稱質量:34 Da
9、平均質量:34.0809 Da
計算化學數據
1、疏水參數計算參考值(XlogP):0.5
2、氫鍵供體數量:1
3、氫鍵受體數量:1
4、可旋轉化學鍵數量:0
5、互變異構體數量:無
6、拓撲分子極性表面積(TPSA):1
7、重原子數量:1
8、表面電荷:0
9、復雜度:0
10、同位素原子數量:0
11、確定原子立構中心數量:0
12、不確定原子立構中心數量:0
13、確定化學鍵立構中心數量:0
14、不確定化學鍵立構中心數量:0
15、共價鍵單元數量:1
性質與穩定性
1.在有機胺中溶解度極大。在苛性堿溶液中也有較大的溶解度。在過量氧氣中燃燒生成二氧化硫和水,當氧氣供應不足時生成水與游離硫。室溫下穩定。可溶于水,水溶液具有弱酸性,與空氣接觸會因氧化析出硫而慢慢變渾。能在空氣中燃燒產生藍色的火焰并生成SO2和H2O,在空氣不足時則生成S和H2O。有劇毒,即使稀的硫化氫也對呼吸道和眼睛有刺激作用,并引起頭痛,濃度達1mg/L或更高時,對生命有危險,所以制備和使用H2S都應在通風櫥中進行。
2.穩定性[21] 穩定
3.禁配物[22] 強氧化劑、堿類
4.聚合危害[23] 不聚合
貯存方法
儲存注意事項[24] 儲存于陰涼、通風的易燃氣體專用庫房。遠離火種、熱源、庫溫不宜超過30℃。保持容器密封。應與氧化劑、堿類分開存放,切忌混儲。采用防爆型照明、通風設施。禁止使用易產生火花的機械設備和工具。儲區應備有泄漏應急處理設備。
合成方法
1.將20%~30%磷酸慢慢地從分液漏斗滴到Na2S?9RO濃水溶液中,將所產生的氣體經無水氯化鈣與五氧化二磷干燥,制得硫化氫氣體,經液化壓入鋼瓶。
2.用硫黃和氫直接合成制得硫化氫純度高
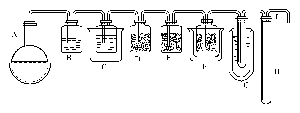
圖XVI-3 制備硫化氫的裝置
純氫減壓后進入干燥器進一步純化,然后經計量進入反應器底部與硫黃直接接觸反應,生成硫化氫,硫化氫經洗滌器洗滌,再進入硫蒸氣冷凝器將其中剩余的硫蒸氣冷凝下來。純凈的硫化氫氣體經壓機壓縮后進入硫化氫冷凝器,液體硫化氫收集在貯罐中。
用硫化鈣與氯化鎂反應制備液態硫化氫的反應裝置如圖所示,全部操作應在通風櫥中進行。
圖制備硫化氫的裝置
A 為置于水浴中的燒瓶;B,C,D,E,F 為250mL玻璃瓶,分別裝有水、飽和Ba(OH)2
(外面用冰鹽冷浴)、氯化鈣、五氧化二磷、玻璃棉(外面以干冰冷卻);
G為50mL試管,杜瓦瓶中為干冰乙醚冷凍劑;H為汞封;I 為出口
在發生瓶A中裝入500mL飽和氯化鎂溶液,并加入10g固體氯化鎂和50g優質硫化鈣。當混合物加熱到60℃時,即可平穩和連續地產生硫化氫氣體。C瓶中的氫氧化鋇吸收最初產生的硫化氫,轉變為硫氫化鋇后,硫化氫即可通過,而其他揮發性酸性雜質則被吸收。系統中空氣未排盡前可使氣體不通過汞封H,以加快排空氣的過程。反應一段時間后在試管G中即有液態硫化氫凝聚。
3.硫化鋁水解法:在燒瓶中放入適量硫化鋁固體,從滴液漏斗中慢慢滴入水,即可順利地產生十分純的硫化氫氣體。
用途
1.用于合成熒光粉,電放光、光導體、光電曝光計等的制造。有機合成還原劑。用于金屬精制、農藥、醫藥、催化劑再生。通用試劑。制取各種硫化物。
2.用于制造無機硫化物,還用于化學分析如鑒定金屬離子。[25]
安全信息
危險運輸編碼:UN 1053 2.3
危險品標志: 易燃
易燃  極毒
極毒  危害環境
危害環境
文獻
[1~25]參考書:危險化學品安全技術全書.第一卷/張海峰主編.—2版.北京;化學工業出版社,2007.6 ISBN 978-7-122-00165-8
備注
暫無
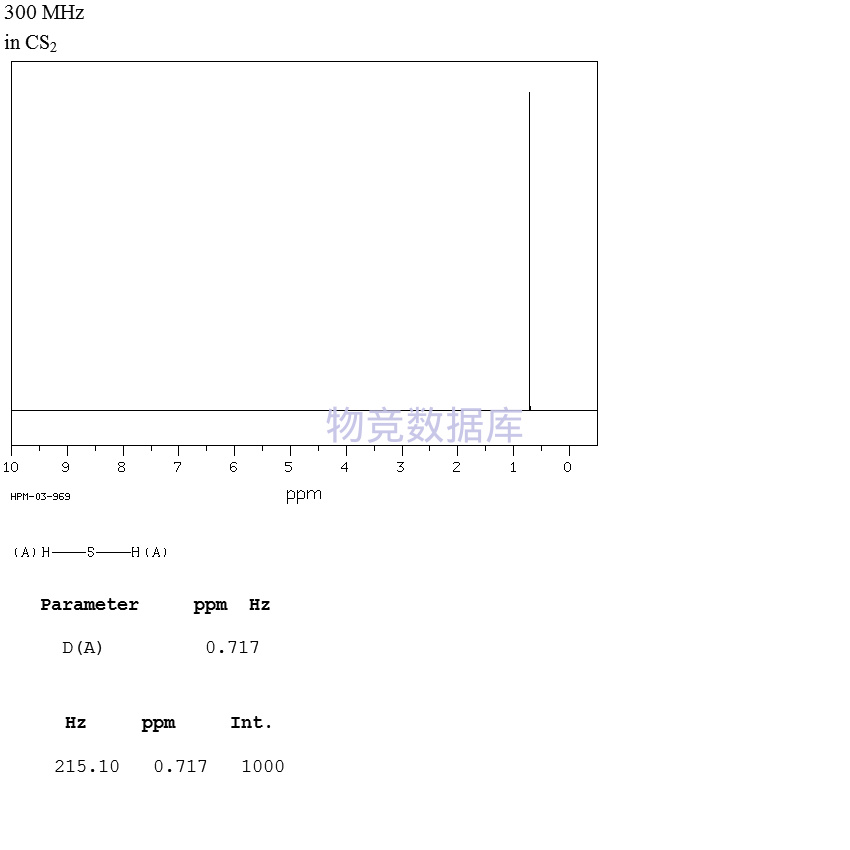
表征圖譜
統計數據
共收錄化學品數據
147579 條



 滬公網安備 31010602001115號
滬公網安備 31010602001115號