砷化氫 Arsine
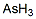
結構式
| 物競編號 | 0KHL |
|---|---|
| 分子式 | AsH3 |
| 分子量 | 77.95 |
| 標簽 | 砷烷, 電子用特種氣體 |
編號系統
CAS號:7784-42-1
MDL號:暫無
EINECS號:232-066-3
RTECS號:暫無
BRN號:暫無
PubChem號:暫無
物性數據
1.性狀:無色氣體,有大蒜臭味。[1]
2.熔點(℃):-116[2]
3.沸點(℃):-62[3]
4.相對密度(水=1):1.689(84.9℃,液體);2.69[4]
5.相對蒸氣密度(空氣=1):2.66[5]
6.飽和蒸氣壓(kPa):1463(20℃)[6]
7.臨界溫度(℃):99.95[7]
8.臨界壓力(MPa):6.55[8]
9.辛醇/水分配系數:0.68[9]
10.閃點(℃):-110[10]
11.爆炸上限(%):100[11]
12.爆炸下限(%):4.5[12]
13.溶解性:溶于水,微溶于乙醇、堿液,溶于苯、氯仿。[13]
毒理學數據
1.急性毒性[14] LC50:390mg/m3(大鼠吸入,10min);250mg/m3(小鼠吸入,10min)
2.刺激性 暫無資料
3.亞急性與慢性毒性[15] 各種動物在反復吸入12~36mg/m3本品時,可見血紅蛋白和紅細胞減少,其體征有溶血、貧血和黃疸。
4.致癌性[16] IARC致癌性評論:IARC將砷及其無機化合物列為G1,確認人類致癌物。
5.其他[17] LCLo:25ppm(人吸入30min);300ppm(人吸入5min)。TCLo:0.325mg/m3(人吸入)
生態學數據
1.生態毒性 暫無資料
2.生物降解性 暫無資料
3.非生物降解性 暫無資料
4.其他有害作用[18] 該物質對環境有危害,應特別注意對水體的污染。
分子結構數據
暫無
計算化學數據
暫無
性質與穩定性
在室溫下穩定,加熱至300oC開始分解。強還原劑。與空氣混合能形成爆炸性混合物,遇明火高熱能引起燃燒爆炸。部分分解放出不愉快的大蒜臭味。對空氣的相對密度為2.7。100mL 20℃的水可溶解20mL胂,也稍溶于乙醇。與氯、溴等鹵族單質反應分別生成AsCl3、AsBr3等。具有還原性,可將硝酸銀水溶液還原而析出銀。極毒。所有AsH3的實驗均應在通風櫥中進行。
貯存方法
儲存注意事項[19] 儲存于陰涼、通風的有毒氣體專用庫房。實行“雙人收發、雙人保管”制度。遠離火種、熱源。庫溫不宜超過30℃。應與氧化劑、食用化學品分開存放,切忌混儲。采用防爆型照明、通風設施。禁止使用易產生火花的機械設備和工具。儲區應備有泄漏應急處理設備。
合成方法
金屬砷與鋅反應生成鋅化砷,砷化鋅再與硫酸反應得精砷烷,經多級吸附純化可制得高純砷烷產品。
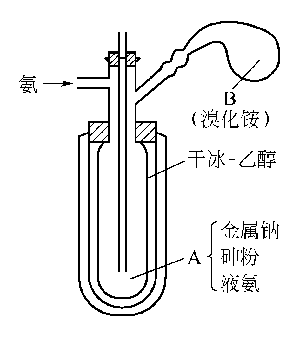
圖XV-4 AsH3的制備裝置
1.在如圖所示裝置的A中加10g金屬鈉,通入用氫氧化鉀、氧化鋇等充分干燥后的氨氣,圖的制備裝置容器A放入裝有干冰-乙醇冷凍劑的杜瓦瓶中,氨被液化。然后加入12g(比等摩爾稍過量)砷粉,搖動使之反應。將裝在B處的42g溴化銨NH4Br徐徐加入,所產生的氣體經水洗后,用P2O5干燥,用液氮在捕集器中使之液化。因為用這種方法不產生氫氣,所以可以生成高純度的胂。液化的胂可以進行蒸餾提純。
2.把50g鋅放進瓷皿中,將瓷皿送入石英管中。把45g砷放進另一瓷皿,將這個瓷皿放在石英管端,通入干燥氮氣,置換其中的空氣。首先加熱裝鋅的瓷皿,達到700℃以后,再加熱裝砷的瓷皿,使其達到300~500℃,使砷蒸氣送到鋅處與之反應,則合成Zn3As2。冷卻后,將此Zn3As2粉碎并裝入三口燒瓶中,在燒瓶上裝有滴液漏斗,用惰性氣體或氫氣置換系統中的空氣以后,從滴液漏斗滴加稀硫酸,就可以產生胂。因為所產生的氣體中含有氫,所以通過P2O5干燥以后,在液氮冷卻的捕集器中液化,再進行蒸餾提純。
3.為簡便制取胂,可將三氧化二砷溶于鹽酸(先令其溶解于氫氧化鈉水溶液,再用濃鹽酸調節pH值在1以下),加入鋅粒,在所產生的氣體中,胂不到四分之一,經干燥后,用液氮冷卻并進行蒸餾提純。
4.一般由As與Zn合成As2Zn3,然后再與H2SO4反應生成ZnSO4和AsH3,再經幾步純化、液化而得。
用途
1.砷烷用于半導體工業中,如外延硅的N型摻雜、硅中N型擴散、離子注入、生長砷化鎵(GaAs)、磷砷化鎵(GaAsP)以及與某些元素形成化合物半導體。
2.該產品在半導體工業中用于外延、n型摻雜、擴散和離子注入工藝,以及磷化鎵薄膜的生產。
3.用于有機合成、軍用毒氣,及應用于科研或某些特殊實驗中。[20]
安全信息
危險運輸編碼:UN 2188
危險品標志: 很易燃
很易燃  極毒
極毒  危害環境
危害環境
安全標識:S9 S16 S28 S33 S45 S60 S61 S36/S37
文獻
[1~20]參考書:危險化學品安全技術全書.第一卷/張海峰主編.—2版.北京;化學工業出版社,2007.6 ISBN 978-7-122-00165-8
備注
暫無
表征圖譜
統計數據
共收錄化學品數據
147579 條




 滬公網安備 31010602001115號
滬公網安備 31010602001115號