四水氯化鉻 Chromium(Ⅱ)chloride tetrahydrate

結構式
| 物競編號 | 1CDD |
|---|---|
| 分子式 | CrCl2?4H2O |
| 分子量 | 194.96 |
| 標簽 | 鉻族元素 |
編號系統
CAS號:13931-94-7
MDL號:暫無
EINECS號:暫無
RTECS號:暫無
BRN號:暫無
PubChem號:暫無
物性數據
暫無
毒理學數據
暫無
生態學數據
暫無
分子結構數據
暫無
計算化學數據
暫無
性質與穩定性
暫無
貯存方法
暫無
合成方法
制備氯化亞鉻最好的方法是氯化鉻溶液的電解還原,或將醋酸亞鉻轉化為氯化亞鉻。用氯化氫氣體作用于加熱的金屬鉻,或用氫氣還原無水氯化鉻,則可以制得無水鹽,電解還原法進行得很慢,并僅能生成氯化亞鉻溶液。用干法制備需要高溫。在亞鉻鹽中,醋酸鹽是最容易制備與提純的,而且它易與酸反應,因此常用它作為制備其他亞鉻化合物的原料。
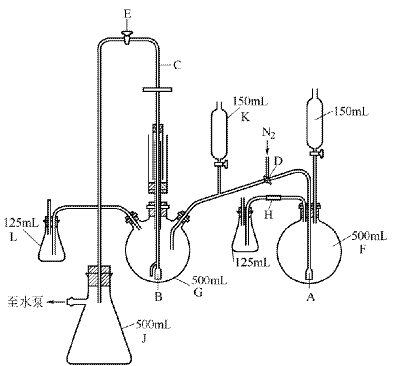
制法1儀器裝置如圖所示,制備氯化亞鉻的儀器
過濾器A的直徑約為1cm,其中疏松地填充了玻璃纖維。攪拌器過濾器組合B是用厚壁玻璃管構成的。在這個組合的末端熔接一小段1cm長的玻璃管,其中填充了玻璃纖維作為過濾之用,此外還熔接著一段玻璃棒的支管。當過濾時在C點處用一段橡皮管把過濾瓶J連接起來。進行攪拌時,這段橡皮管則令它和攪拌器相連,并用一小段玻璃棒把橡皮管塞閉起來。
在全部制備過程中反應瓶G中經常充填著氮氣(氮氣從D處進入瓶中而從L處逸出)。氮氣事先通過填充著焦性沒食子酸與氯化亞銅的氨溶液的兩個吸收塔以除去其中的氧氣,為了完全地除去反應瓶中的空氣,最容易的方法是先在其中充以新煮沸過的水,然后用氮氣將水從J瓶中排出。
將84g醋酸亞鉻溶解在100mL水中,并將溶液過濾。將這個溶液從漏斗K中加入到反應瓶中,并將此混合物攪拌少許時間。將液體濾出,用新煮沸過的蒸餾水洗滌沉淀物。如果需要將醋酸亞鉻從反應瓶中取出,在與空氣相接觸之前需將醋酸亞鉻充分地加以干燥,因為它在潮濕時比干燥時更容易被氧化。用乙醇和乙醚洗滌此沉淀物來進行干燥,最后少量的乙醚則用氮氣流把它除盡。
Cr(C2H3O2)2+2HCl+4H2O→CrCl2·4H2O+2HC2H3O2
制備氯化亞鉻和制備醋酸亞鉻的儀器唯一改變是在氮氣進口的管子上增加一支三通活塞(見圖)。這樣就有可能在反應瓶中通入氮氣,或通入氯化氫氣,或同時通入此兩種氣體。在開始制備之前,必須小心地除盡由氯化氫發生器和連接處而來的任何痕跡量的空氣。
將裝有醋酸亞鉻的反應瓶浸入冰鹽混合物中冷卻到0℃。將氯化氫和氮氣一起通入燒瓶中約1h。如果氣流不夠穩定的話,安全瓶中的水將會被吸入到反應瓶中來。將過量的液體濾出,并用20mL冷濃鹽酸洗滌沉淀。可以用丙酮洗滌CrCl2·4H2O進行干燥,不過完全干燥是困難的,因為丙酮蒸發得很慢。當曝置于空氣中時,CrCl2·4H2O很快被氧化,但保存在反應燒瓶中能穩定若干時間。
制法2 取活化的純電解鉻8g,加20%的鹽酸40~50mL在氮氣流中進行反應。反應初始激烈地進行,稍加冷卻,以防反應物噴溢出來。反應結束后,在水浴上加熱,使殘余的鉻完全溶解。接著將溶液置于冰箱內冷卻一夜,析出美麗的藍色結晶。趁冷在密封過濾器中吸濾。用除過氧的冷丙酮洗滌,減壓干燥后儲存于氮氣中。
性質減壓下進行徹底干燥,可失去部分結晶水。將吡啶加至鹵化物水溶液中,則析出綠色的沉淀,這是由吡啶取代結晶水而成的產物。CrCl2·2Py,這種結晶比水合物對氧穩定,置于空氣中數小時也不發生變化。可用乙醇或乙醇和吡啶的混合溶劑進行再結晶。
將在50℃時得到的暗綠色的四水合物加熱、經由藍色的三水合物、綠色的二水合物,最后在113℃以上變為白色的無水物。
在低溫下制備的四水合氯化亞鉻是亮藍色的晶狀物,能溶于水但幾乎不溶于冷濃鹽酸。高于38℃時,它變為異構的綠色變體。氯化亞鉻甚至在干態下也能從空氣中吸收氧,生成一種綠色的氯氧化物。當在溶液中放置時,它被水氧化而放出氫氣。酸、堿以及有鉑與鈀存在時,這個變化都能被催化。
用途
暫無
安全信息
危險運輸編碼:暫無
危險品標志:暫無
安全標識:暫無
危險標識:暫無
文獻
None
備注
None
表征圖譜
統計數據
共收錄化學品數據
147579 條




 滬公網安備 31010602001115號
滬公網安備 31010602001115號