氫化鋁 Aluminium hydride
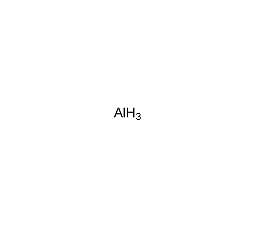
結構式
| 物競編號 | 1CJL |
|---|---|
| 分子式 | AlH3 |
| 分子量 | 30.01 |
| 標簽 | 鋁烷,, Alane |
編號系統
CAS號:7784-21-6
MDL號:暫無
EINECS號:232-053-2
RTECS號:暫無
BRN號:暫無
PubChem號:暫無
物性數據
1.性狀:無色固體
2.熔點(oC):110
3.溶解性:溶于THF和乙醚溶劑。
毒理學數據
暫無
生態學數據
暫無
分子結構數據
暫無
計算化學數據
1.疏水參數計算參考值(XlogP):無
2.氫鍵供體數量:0
3.氫鍵受體數量:0
4.可旋轉化學鍵數量:0
5.互變異構體數量:無
6.拓撲分子極性表面積0
7.重原子數量:1
8.表面電荷:0
9.復雜度:0
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:1
性質與穩定性
1.氫化鋁為無色的固體。對熱不穩定,加熱到150~200℃時即分解。準確的分解溫度因AlH3的生成條件而異。氫化鋁為強還原劑。遇水或濕氣會發生爆炸反應而生成氫氣。光照后即分解。在-10℃的封閉管中能夠保存一年。極易溶于四氫呋喃中。在乙醚中的溶解度為0.2mol/L。在乙醚中合成的產物是由AlH3和乙醚按摩爾比0.29~0.33構成的加成物。不含乙醚的產物是把AlH3的乙醚溶液加入到特別過量的戊烷或己烷中所得到的白色沉淀。一旦從乙醚中沉淀出來就不會再溶于乙醚中。如果有強的路易斯堿L存在,則生成LAlH3或者L2AlH3而溶解。
2.氫化鋁溶液不會自燃,但與水、酸類、潮濕空氣接觸有引起燃燒危險,遇氧化劑反應劇烈。氫化鋁溶液必須原位制備使用,大約3天后就會降解,因此不可能長時間保存。使用是必須小心謹慎。
貯存方法
在氮氣中貯存。
合成方法
1. 原料的提純:以下的所有操作必須在充滿氮氣或氬氣的干燥箱中進行。不得含有水蒸氣,含氧量不超過3~4mL/m3。而且,必須在系統中除去能與反應物和生成物進行反應的物質。當存在少量雜質時就可能把生成的氫化鋁分解掉。所有的試劑必須全用無水的。市售的乙醚、氫化鋁鋰、三氯化鋁等都必須進一步提純。使用的玻璃器具要用濃硝酸或者氫氟酸洗過之后,再用蒸餾水沖洗幾次,在110~120℃下進行干燥。將氫化鋁鋰加到乙醚內,在氮氣中或真空中蒸餾,并通過裝有分子篩的柱(40cm)進行干燥、提純。因為乙醚非常容易揮發,這些操作應在通風櫥內進行。將氫化鋁鋰溶于乙醚,過濾后經減壓蒸餾蒸出溶劑濃縮,進行重結晶。三氯化鋁可在高真空下使其升華(110~120℃)得以提純,在此溫度下要使50g三氯化鋁升華需要24h,其蒸氣再通過1~2cm長的裝有活性炭(50~200目)吸附柱處理,可更加純凈。
主反應3LiAlH4+AlCl3→4AlH3+3LiCl
在干燥箱中,把32.3g三氯化鋁(0.242mol)和電磁攪拌棒裝入500mL圓底燒瓶中,加塞后將燒瓶從干燥箱中取出,在低氮氣壓下(25~50mmHg,1mmHg=133.322Pa)迅速安裝盛有乙醚的滴液漏斗,將上述500mL燒瓶放在干冰二氯甲烷浴中一邊攪拌物料一邊進行冷卻,從滴液漏斗把經過蒸餾提純的300mL乙醚慢慢地加入燒瓶中。乙醚冷卻后從干冰浴中取出燒瓶。如果三氯化鋁發生放熱的溶劑化反應而使乙醚沸騰時,應把燒瓶再次冷卻。三氯化鋁溶解后,將溶液加熱到室溫,嚴密加塞放入干燥箱。另取28.2g純氫化鋁鋰(0.743mol)裝入容積為1.5L的燒瓶中,并用750mL蒸餾過的乙醚加以溶解。然后往LiAlH4和AlCl3的乙醚溶液表面分別吹入干燥氮氣,使其冷卻到-5℃。為了保持一定的溶劑體積必須經常加入乙醚。將AlCl3溶液在攪拌下加到冷的LiAlH4溶液中。加完后,對反應混合液施以19.7~34.2kPa壓力的氮氣,經玻璃過濾器,濾到1.5L燒瓶中。該燒瓶預先裝入10g NaBH4(該NaBH4應在真空中于60℃干燥8h,并粉碎至1μm以下,可得最好的結果)和電磁攪拌棒。攪拌濾液,利用NaBH4將未反應的AlCl3從AlH3的乙醚溶液中除去。LiBlH4留在溶液中,氯化鈉則沉淀出來。邊往濾液中吹入干燥氮氣邊攪拌3~4min之后,再往另一個1.5L燒瓶中過濾。這樣就可把過剩的NaBH4和已沉淀的氯化鈉除去。往濾液中邊吹入干燥氮氣,邊濃縮至600mL之后,加熱到室溫。經6~8h后,氫化鋁的乙醚加成物就沉淀出來。將生成物過濾后,用100mL無水乙醚洗滌兩次,在高真空下干燥10~12h;產量約30g(58%)。
用途
1.還原劑,似氫化鋁銼。但對鹵素、硝基的還原活性比后者小得多,因而選擇性更好。還原毅基成輕基。也用于烯胺的氫解,鹵代物的脫內、磺酸內酯的脫硫,以及酮厲、院膠和睛還原成胺等。
2.氫化鋁是一種對多種官能團有效的還原試劑[1],能夠將醛、縮醛、酮、醌、縮酸、酸酐、酰氯、酯和內酯還原為相應的醇,將酰胺、腈、肟和異氰酸酯還原為相應的胺。氫化鋁對硝基化合物、硫化物、砜以及甲基苯磺酸鹽無還原活性,但是對二硫化物和亞砜有效。
對于酮的還原,氫化鋁較其它還原試劑能夠表現出不同的立體選擇性,這點在具有生物活性的甾族化合物的還原中尤為重要 (式1)[2]。對于α,β-不飽和酮還原為烯丙醇的反應,氫化鋁也能表現出特異的立體選擇性 (式2)[3]。

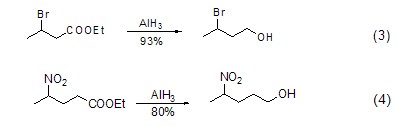
對于羧酸和酯的還原反應,氫化鋁較氫化鋁鋰的反應更快。但是對于鹵代烷烴的還原,氫化鋁則表現出較惰性的還原活性。因此使用氫化鋁可以有效地實現帶鹵素的羧酸和酯的還原反應 (式3)。此外,氫化鋁鋰能夠還原硝基化合物,而氫化鋁則對其不具有還原效果,因此使用氫化鋁還能實現帶硝基的羧酸和酯的還原反應 (式4)。
對于酰胺化合物還原為胺的反應,通常存在C-O鍵斷裂和C-N鍵斷裂的競爭反應。但使用氫化鋁則可以選擇性地實現C-O鍵的斷裂,從而實現α,β-不飽和酰胺向烯丙基胺化合物的轉化 (式5)[4]。
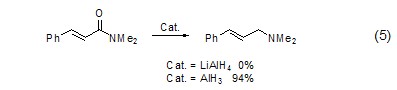
由于氫化鋁的堿性相對氫化鋁鋰較弱,因此對于含酸性氫原子的底物同樣適用。如對含有酸性α-H的烯丙基腈化合物的還原 (式6,式7)。
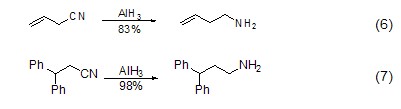
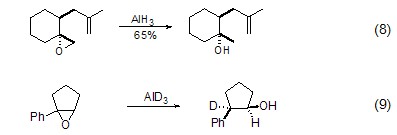
氫化鋁的另一類重要反應是誘導環氧化合物的開環反應。對于大多數環氧化合物,負氫進攻都是發生在立體位阻較小的一端 (式8)[5],但由于氫化鋁中負氫自身的性質,它也可以進攻立體位阻較大的碳原子 (式9)[6]。
此外,氫化鋁還能實現丙炔醇系統上的氫鋁化反應,即對炔烴發生加成反應,進而用碘淬滅實現sp2-碘代烯丙醇化合物的制備。并且氫化鋁較氫化鋁鋰表現出了不同的區域選擇性,負氫會優先進攻3-位炔碳原子 (式10)[7]。

安全信息
危險運輸編碼:暫無
危險品標志:暫無
安全標識:暫無
危險標識:暫無
文獻
1. (a) Saito, S. Science of Synthesis, 2004, 7, 15. (b) Finholt, A. E.; Bond, A. C.; Schlesinger, H. I. J. Am. Chem. Soc., 1947, 69, 1199. 2. Martinez, E.; Muchowski, J. M.; Velarde, E. J. Org. Chem., 1977, 42, 1087. 3. (a) Brown, H. C.; Hess, H. M. J. Org. Chem., 1969, 34, 2206. (b) Dilling, W. L.; Plepys, R. A. J. Org. Chem., 1970, 35, 2971. 4. Ashby, E. C.; Sanders, J. R.; Claudy, P.; Schwarts, P. J. Am. Chem. Soc., 1973, 95, 6485. 5. Maruoka, K.; Saito, S.; Ooi, T.; Yamamoto, H. Synlett, 1991, 255. 6. Lansbury, P. T.; Scharf, D. J.; Pattison, V. A. J. Org. Chem., 1967, 32, 1748. 7. Elsenbaumer, R. L.; Mosher, H. S.; Morrison, J. D.; Tomaszewskil, J. E. J. Org. Chem., 1981, 46, 4034. 8.參考書:現代有機合成試劑<性質、制備和反應>;胡躍飛 付華 編著;化學工業出版社;ISBN 7-5025-8542-7
備注
暫無
表征圖譜
統計數據
共收錄化學品數據
147579 條




 滬公網安備 31010602001115號
滬公網安備 31010602001115號