苯基次甲基-[1,3-二(2,4,6-三甲基苯基)-2-咪唑啉基]-二氯(三環己基膦基)釕 Benzylidene[1,3-bis(2,4,6-trimethylphenyl)-2-imidazolidinylidene]dichloro(tricyclohexylphosphine)ruthenium
![苯基次甲基-[1,3-二(2,4,6-三甲基苯基)-2-咪唑啉基]-二氯(三環己基膦基)釕結構式](http://staticv5.basechem.org/img/tupu/old/c8112b7565144aeba8f46d21c7ca2827.gif)
結構式
| 物競編號 | 1D5H |
|---|---|
| 分子式 | C46H65Cl3N2PRu |
| 分子量 | 848.98 |
| 標簽 | 第II代Grubbs 催化劑, Grubbs Catalyst 2nd Generation, 催化劑 |
編號系統
CAS號:246047-72-3
MDL號:MFCD03453237
EINECS號:暫無
RTECS號:暫無
BRN號:暫無
PubChem號:暫無
物性數據
1.性狀:紫紅色粉末狀固體
2..熔點(℃):143.5~148.5
3.溶解性:易溶于有機溶劑,通常在CH2Cl2、苯或者甲苯的溶液中使用。
毒理學數據
暫無
生態學數據
暫無
分子結構數據
暫無
計算化學數據
1.疏水參數計算參考值(XlogP):無
2.氫鍵供體數量:0
3.氫鍵受體數量:2
4.可旋轉化學鍵數量:6
5.互變異構體數量:無
6.拓撲分子極性表面積6.5
7.重原子數量:52
8.表面電荷:0
9.復雜度:927
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:2
性質與穩定性
該試劑對空氣和濕氣較穩定,即使放置在空氣中也不會分解,其催化活性也不受到溶劑中的空氣、水蒸氣以及痕量雜質的影響。
貯存方法
暫無
合成方法
實驗室可以參考文獻的標準實驗步驟來制備[1~3]。
用途
Grubbs 第II代催化劑是將第I代催化劑中的三環己基膦配體置換為二取代二氫咪唑配體。由于配體中氮原子取代基的空間位阻效應和電子效應,催化劑在反應過程中比較穩定,自身不容易發生分解[4~6]。與第I代催化劑相比,它具有更強的穩定性,更高的反應活性。反應條件更加溫和,用量也相對更小,大多情況下催化劑的用量在5 mol% 即可。而且反應時間也相應縮短,具有更加廣闊的應用前景。
與第I代催化劑不同的是,該試劑在催化多取代烯烴的RCM反應時,能夠克服位阻的影響,高產率地得到三取代和四取代的環烯產物 (式1)[7]。

在催化分子內RCM反應生成大環類化合物時,第I代催化劑很容易發生分子間復分解反應,而使用第II代催化劑可以有效地提高分子內RCM反應的產率 (式2)[8]。

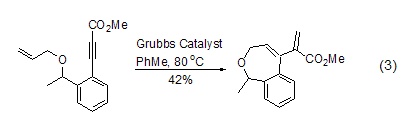
在缺電子烯烴或者炔烴發生RCM反應時,如果使用第I代催化劑必須添加路易斯酸試劑來提高反應的活性。然而,由于第II代催化劑自身較高的反應活性,即使不使用路易斯酸試劑,產物也能達到較好的收率 (式3)[3,9]。
在含氮類底物的RCM反應中,第II代催化劑對于游離胺仍然無能為力。但是,在Ti(O-iPr)4的幫助下,無需將胺轉化為酰胺或者季銨鹽便可以得到很好的收率 (式4,式5)[10]。

安全信息
危險運輸編碼:暫無
危險品標志:暫無
安全標識:S26 S36/S37/S39
危險標識:R36/37/38
文獻
1. Huang, J.; Stevens, E. D.; Nolan, S. P.; Petersen, J. L. J. Am. Chem. Soc., 1999, 121, 2674. 2. Scholl, M.; Trnka, T. M.; Morgan, J. P.; Grubbs, R. H. Tetrahedron Lett., 1999, 40, 2247. 3. Furstner, A.; Ackermann, L.; Gabor, B.; Goddard, R.; Lehmann, C. W.; Mynott, R.; Frank Stelzer, F.; Oliver R. Thiel, O. R. Chem. Eur. J., 2001, 7, 3236. 4. Herrmann, W. A.; Kocher, C. Angew. Chem. Int. Ed., 1997, 36, 2162. 5. Bourissou, D.; Guerret, O.; Gabbai, F. P.; Bertrand, G. Chem. Rev., 2000, 100, 39. 6. Arduengo, A. J. Acc. Chem. Res., 1999, 32, 913. 7. Furstner, A.; Thiel, O. R.; Ackermann, L.; Schanz, H. J.; Nolan, S. P. J. Org. Chem., 2000, 65, 2204. 8. Bielawski, C. W.; Grubbs, R. H. Angew. Chem. Int. Ed., 2000, 39, 2903. 9. Chatterjee, A. K.; Morgan, J. P.; Scholl, M.; Grubbs, R. H. J. Am. Chem. Soc., 2000, 122, 3783. 10. Yang, Q.; Xiao, W.-J.; Yu, Z. Org. Lett., 2005, 7, 871. 11.參考書:現代有機合成試劑<性質、制備和反應>;胡躍飛 付華 編著;化學工業出版社;ISBN 7-5025-8542-7
備注
暫無
表征圖譜
統計數據
共收錄化學品數據
147579 條




 滬公網安備 31010602001115號
滬公網安備 31010602001115號