碘酰苯 Iodoxybenzene
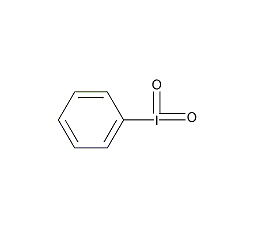
結構式
| 物競編號 | 1D5R |
|---|---|
| 分子式 | C6H5IO2 |
| 分子量 | 236.01 |
| 標簽 | 暫無 |
編號系統
CAS號:696-33-3
MDL號:暫無
EINECS號:暫無
RTECS號:暫無
BRN號:暫無
PubChem號:暫無
物性數據
1.熔點(℃):230
2.溶解性:溶于水和大多數有機溶劑。經常在芳烴溶劑中使用,例如苯和氯苯。
毒理學數據
暫無
生態學數據
暫無
分子結構數據
暫無
計算化學數據
1.疏水參數計算參考值(XlogP):1.5
2.氫鍵供體數量:0
3.氫鍵受體數量:2
4.可旋轉化學鍵數量:0
5.互變異構體數量:無
6.拓撲分子極性表面積34.1
7.重原子數量:9
8.表面電荷:0
9.復雜度:132
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:1
性質與穩定性
該試劑對空氣和濕氣不穩定,最好是制備后馬上使用。由于該試劑在250 oC左右會發生分解爆炸,因此盡量避免無溶劑情況下加熱。建議在通風櫥中操作和使用。
貯存方法
暫無
合成方法
在實驗室可以通過多種方法來制備。最傳統的方法是使用過氧乙酸將碘苯氧化成碘酰苯[1]。最方便的方法是使用溴酸酸鉀在硫酸的存在下將碘苯氧化成碘酰苯[2]。
用途
碘酰苯在有機合成中被用作選擇性氧化劑,它的應用范圍較窄,但非常特殊。與金屬氧化劑比較,它在有機溶劑中具有更好的溶解度和對環境幾乎不產生污染。
碘酰苯發生的主要反應之一是烯丙基位的氧化反應。在二芳基聯硒的存在下,碘酰苯可以選擇性地在烯鍵的烯丙基位上發生氧化反應,生成α,β-不飽和酮[3,4]。在復雜產物的合成中使用更能夠顯示出該試劑的優越性 (式1)[5,6]。雖然烯丙基位上的氧化反應也可以使用Cr(VI) 氧化劑來完成,但會引起雙鍵的移動而造成選擇性較差。最近有人報道使用碘酰苯在DMSO溶液中氧化烯丙基醇發生氧化重排反應,生成α,β-不飽和酮 (式2)[7]。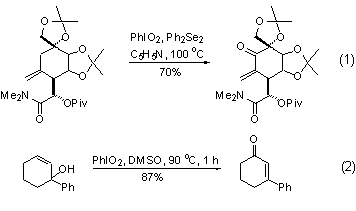
碘酰苯發生的另一個主要反應是氧化環酮化合物成為α,β-不飽和酮 (式3)[8,9]。如果底物結構合適的話,可在酮官能團的兩端產生兩個雙鍵 (式4)[10,11]。該反應在環狀和非環狀化合物之間具有很高的區域選擇性,在甾體化學中具有非常高的應用價值。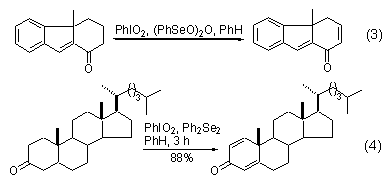
此外,碘酰苯在手性配體的存在下將硫醚氧化成手性亞砜的反應 (式5)[12]和在Pd催化劑存在下與CO發生的芳基羧酸化反應也值得關注 (式6)[13]。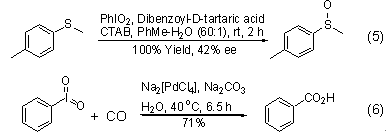
安全信息
危險運輸編碼:暫無
危險品標志:暫無
安全標識:暫無
危險標識:暫無
文獻
1. Sharefkin, J. G.; Saltzman, H. Org. Synth., 1963, 43, 65. 2. Banerjee, A.; Banerjee, G. C.; Bhattacharya, S.; Banerjee, S.; Samaddar, H. J. Indian Chem. Soc., 1981, 58, 605. 3. Barton, D. H. R.; Crich, D. Tetrahedron, 1985, 41, 4359. 4. Gleiter, Rolf.; Mueller, G. J. Org. Chem., 1988, 53, 3912. 5. Hinman, A.; Du Bois, J. J. Am. Chem. Soc., 2003, 125, 11510. 6. Kuramochi, A.; Usuda, H.; Yamatsugu, K.; Kanai, M.; Shibasaki, M. J. Am. Chem. Soc., 2005; 127, 14200. 7. Shibuya, M.; Ito, S.; Takahashi, M.; Iwabuchi, Y. Org. Lett., 2004, 6, 4303. 8. Neuhaus, D.; Rees, C. W. Chem. Comm., 1983, 318. 9. Iida, T.; Nishida, S.; Chang, F. C.; Niwa, T.; Goto, J.; Nambara, T. Chem. Pharm. Bull., 1993, 41, 763. 10. Barton, D. H. R.; Godfrey, C. R. A.; Morzycki, J. W.; Motherwell, W. B.; Ley, S. V. J. Chem. Soc., Perkin Trans. 1, 1982, 1947. 11. Kuenzer, H.; Sauer, G.; Wiechert, R. Tetrahedron, 1989, 45, 6409. 12. Tohma, H.; Takizawa, S.; Watanabe, H.; Fukuoka, Y.; Maegawa, T.; Kita, Y. J. Org. Chem., 1999, 64, 3519. 13. Grushin, V. V.; Alper, H. J. Org. Chem., 1993, 58, 4794。 14.參考書:現代有機合成試劑<性質、制備和反應>;胡躍飛 付華 編著;化學工業出版社;ISBN 7-5025-8542-7
備注
暫無
表征圖譜
統計數據
共收錄化學品數據
147579 條




 滬公網安備 31010602001115號
滬公網安備 31010602001115號