亞甲基三苯基膦烷 Methylenetriphenylphosphorane
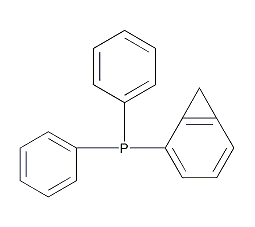
結構式
| 物競編號 | 1D6J |
|---|---|
| 分子式 | C19H17P |
| 分子量 | 276.31 |
| 標簽 | 暫無 |
編號系統
CAS號:3487-44-3
MDL號:暫無
EINECS號:暫無
RTECS號:暫無
BRN號:暫無
PubChem號:暫無
物性數據
1.性狀:白色晶體
2.熔點(℃):96
3.溶解性:溶于醚、THF、DME、苯、甲苯、DMSO。水或者質子溶劑會將該試劑徹底破壞。
毒理學數據
暫無
生態學數據
暫無
分子結構數據
暫無
計算化學數據
1.疏水參數計算參考值(XlogP):無
2.氫鍵供體數量:0
3.氫鍵受體數量:0
4.可旋轉化學鍵數量:3
5.互變異構體數量:無
6.拓撲分子極性表面積0
7.重原子數量:20
8.表面電荷:0
9.復雜度:275
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:1
性質與穩定性
該試劑應一直在氮氣或氬氣氛下使用或處理。
貯存方法
合成方法
制備方法通常是:向懸浮在適當溶劑中的甲基三苯基溴化加入強堿,如丁基鋰、叔丁基鉀或氨基鈉等。通常甲基三苯基溴化懸浮在干燥的乙醚或THF中,在0 oC、氮氣氛下加入正丁基鋰,在室溫下反應1小時,顏色由黃色變為橙色說明該葉立德試劑已經形成。
用途
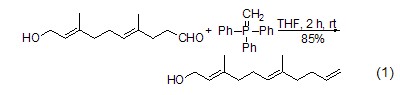
醛、酮的亞甲基化 該試劑最廣泛的應用是與醛、酮發生Wittig[1]亞甲基化反應 (式1,式2)[2,3],分子中的烯鍵與羥基不受影響。
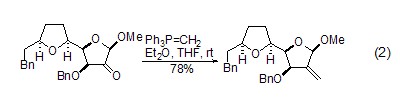
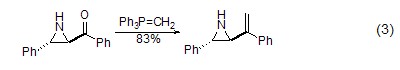
類似吖丙啶烯的化合物,也可以通過與亞甲基三苯基膦作用進行亞甲基化 (式3)[4]。
取代的1,3-二烯可以通過該磷葉立德與相應的烯醛或烯酮反應制備 (式4)[5],與羰基共軛的雙鍵也不受影響。制得的二烯化合物通常會繼續用來進行Diels-Alder反應。

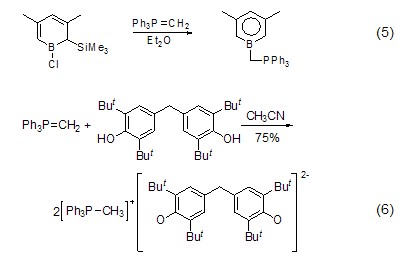
硼的亞甲基化 亞甲基三苯基膦烷可以與鹵代硼反應,生成含有B-C鍵的化合物 (式5)[6],與酚羥基也可以形成鹽 (式6)[7]。
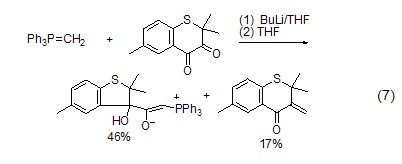
葉立德重排 亞甲基三苯基膦中的亞甲基可以用丁基鋰使其鋰鹽化,這樣就可以與有一定位阻的酮反應,使其亞甲基化。α,β-二酮化合物與過量的亞甲基三苯基膦烷反應,可以發生α-酮醇重排,得到一種穩定的葉立德(式7)[8]。X射線衍射結果表明,這種葉立德分子中磷原子和氧原子處在雙鍵的同側。
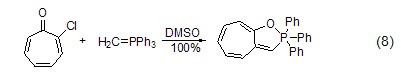
形成甘菊環 亞甲基三苯基膦與2-氯環庚三烯酮反應,可以得到甘菊環系統 (式8)[9]。反應過程中亞甲基首先進攻7-H,然后再脫掉氯原子,形成二環系統。
與內酯的反應 過量的亞甲基三苯基膦烷與內酯反應,可以得到羥基端烯開環產物 (式9)[10]。

安全信息
危險運輸編碼:暫無
危險品標志:暫無
安全標識:暫無
危險標識:暫無
文獻
1. Wittig, G. Liebigs Ann. Chem., 1953, 580, 44. 2. Koh J. H.; Gagne M. R. Angew. Chem., Int. Ed., 2004, 43, 3459. 3. Gurjar, M. K.; Mohapatra, S.; Phalgune, U. D.; Puranik, V. G.; Mohapatra, D. K. Tetrahedron Lett., 2004, 45, 7899. 4. Rowlands, G. J.; Barnes, W. K. Tetrahedron Lett., 2004, 45, 5347. 5. Bartelt, R. J.; Weisleder, D.; Momany, F. A. Synthesis, 2003, 117. 6. Zheng X.; Wang B. Herberich G. E. Organometallics, 2002, 21, 1949. 7. Broder C. K., Davidson M. G., Forsyth V. T., Howard J. A. K., Lamb S., Mason S. A. Cryst. Growth Design, 2002, 2, 163. 8. Gabbutt C. D.; Hepworth J. D.; Heron B. M.; Jones A. M.; Raper E. S.; Clegg W. Phosphorus Sulfur Silicon Relat. Elem., 1998, 143, 221. 9. Takayasu T.; Nitta M. J. Chem. Soc. Perkin Trans. 1, 1997, 681. 10. Brunel Y.; Rousseau G. Tetrahedron Lett., 1996, 37, 3853. 11.參考書:現代有機合成試劑<性質、制備和反應>;胡躍飛 付華 編著;化學工業出版社;ISBN 7-5025-8542-7
備注
暫無
表征圖譜
統計數據
共收錄化學品數據
147579 條




 滬公網安備 31010602001115號
滬公網安備 31010602001115號