碳酸鋰 Lithium carbonate
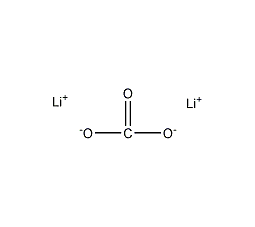
結構式
| 物競編號 | 05Q4 |
|---|---|
| 分子式 | Li2CO3 |
| 分子量 | 73.89 |
| 標簽 | 高純碳酸鋰, 酸鋰, Carbolith, Carbolithium, Lithonate, Candamide, Camcolit, 催化劑, 制藥, 鋰鹽制備, 磁性材料原料及中間體 |
編號系統
CAS號:554-13-2
MDL號:MFCD00011084
EINECS號:209-062-5
RTECS號:OJ5800000
BRN號:3999191
PubChem號:24882220
物性數據
1. 性狀:白色粉末狀物質。
2. 密度(g/mL,25/4℃):2.11
3. 相對蒸汽密度(g/mL,空氣=1):2.51
4. 熔點(oC):720
5. 沸點:1310
6. 溶解性:不溶于醇和丙酮,溶于酸。微溶于水。
毒理學數據
1.具有明顯的刺激作用,首先對胃腸道、腎臟和中樞神經系統有損害。
2.空氣中最高允許濃度: 冷凝: 0.05mg/m3; 碎裂氣溶膠:0.5mg/m3
生態學數據
其它有害作用:該物質對環境可能有危害,對水體應給予特別注意。
分子結構數據
暫無
計算化學數據
1.疏水參數計算參考值(XlogP):無
2.氫鍵供體數量:0
3.氫鍵受體數量:3
4.可旋轉化學鍵數量:0
5.互變異構體數量:無
6.拓撲分子極性表面積63.2
7.重原子數量:6
8.表面電荷:0
9.復雜度:18.8
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:3
性質與穩定性
1.不溶于醇,溶于酸。600 ℃以下對熱穩定,618 ℃開始部分分解成氧化鋰和二氧化碳。
貯存方法
1.貯存于通風干燥處,注意防雨淋水浸。
2.三合一復合袋內襯塑料袋包裝,25kg/袋;或者纖維板桶包裝,25kg/桶。密閉貯藏于陰涼、干燥、通風處。
3.不可與酸類物品接觸.
合成方法
1.鹵水綜合利用法鹵水經提取氯化鋇后的含鋰料液加入純堿以除去料液內鈣、鎂離子,加入鹽酸酸化,蒸發去除氯化鈉,再經除鐵,然后加入過量純堿使碳酸鋰沉淀,經水洗、離心分離、干燥,制得碳酸鋰成品。其反應式如下:
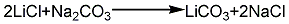
2.石灰燒結法鋰輝石精礦(一般含氧化鋰6%)和石灰石按1∶(2.5~3)重量比配料。混合磨細,在1150~1250 ℃下燒結生成鋁酸鋰和硅酸鈣,經濕磨粉碎,用洗液浸出氫氧化鋰,經沉降過濾,濾渣返回或洗滌除渣,浸出液經蒸發濃縮,然后加入碳酸鈉生成碳酸鋰,再經離心分離、干燥,制得碳酸鋰成品。其反應式如下:
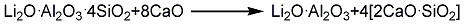
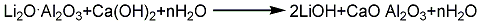
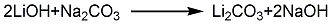
3.用氫氧化鋰和二氧化碳為原料反應便可制得高純度的碳酸鋰,也可以用硫酸鋰和碳酸鈉為反應物,但碳酸鋰易溶于其他鹽溶液中,故產率不太高,一般為75%左右,而且產物中還會含有少量的硫酸鋰。
精制法[13]稱取25g碳酸鋰,在室溫下攪拌溶于2L水中,過濾除去不溶物質,激烈攪拌防止碳酸鋰粘在燒杯壁上,慢慢加熱至接近沸點,至完全沉淀,趁熱過濾,再用沸水洗滌碳酸鋰2~3次,在110℃下干燥,將濾液冷卻,加入碳酸鋰直至飽和,重復以上操作,可制得與第一次純度基本相同的產物。
4.硫酸法 將熔融的鋰輝石與硫酸反應,經凈化后再與碳酸鈉反應制得。石灰法 將焙燒的鋰輝石與石灰乳反應,經凈化后再與碳酸鈉反應制得。副產法 由井鹽鹵制氯化鋇后含鋰的母液中提取。
5.以工業氫氧化鋰為原料,加熱水將其溶解后,濾去不溶物,趁熱向濾液中通入干凈二氧化碳氣體至不再生成沉淀為止:
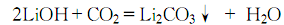
趁熱過濾,甩干,用熱蒸餾水洗滌至合格,于110℃烘干即可。將工業碳酸鋰溶于冷水中,過濾后,濾液煮沸,停止加熱,趁熱過濾,熱水洗滌、甩干、干燥,也能制得試劑碳酸鋰。
用途
1.用于治療狂燥性精神病,制作鎮靜劑等。是制取鋰化合物和金屬鋰的原料。可作鋁冶煉的電解浴添加劑。在玻璃、陶瓷、醫藥和食品等工業中應用廣泛,亦可用于合成橡膠、染料、半導體及軍事國防工業等方面。
2.用作抗躁狂藥。用作搪瓷玻璃的添加劑,可增加搪瓷的光滑度,降低熔化點,并增強瓷器的耐酸、耐冷激、熱激性能。在顯像管制造中,它可提高顯像管的穩定性并增加強度、清晰度,并降低表面粗糙度。還用于制造其他鋰化合物、熒光粉及電解鋁工業等。
3.用作光譜分析試劑,催化劑。用于鋰鹽制備,制藥及陶瓷、玻璃工業。
4.用作鋁冶煉的電解添加劑和用于電鍍處理中。
安全信息
危險運輸編碼:UN 3264 8/PG 3
危險品標志: 有害
有害
安全標識:S8 S26 S43 S45 S24/25 S36/S37 S37/S39
危險標識:R22 R36 R41 R36/37/38 R36/38
文獻
暫無
備注
暫無
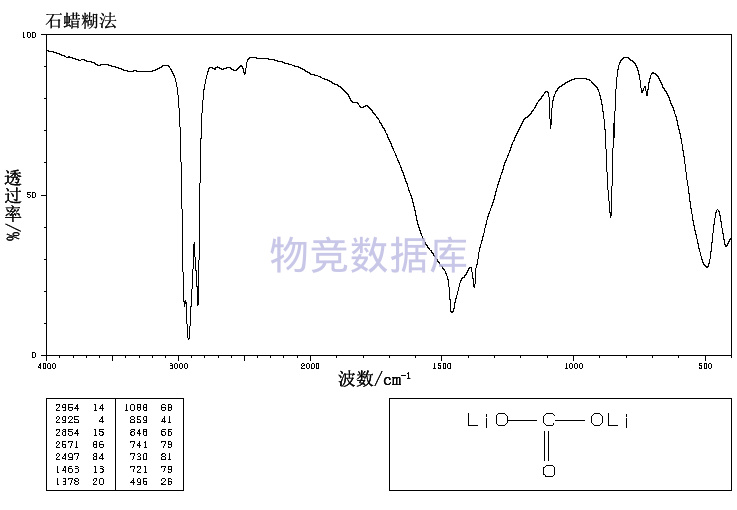
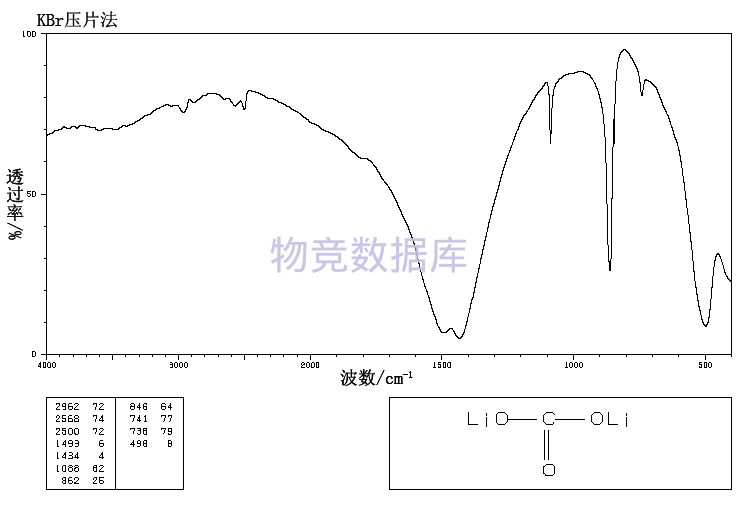
表征圖譜
統計數據
共收錄化學品數據
147579 條



 滬公網安備 31010602001115號
滬公網安備 31010602001115號