叔丁基鋰 tert-Butyllithium

結構式
| 物競編號 | 063X |
|---|---|
| 分子式 | C4H9LI |
| 分子量 | 64.05 |
| 標簽 | Lithium-2-methyl-2-propanide, t-BuLi, 合成試劑 |
編號系統
CAS號:594-19-4
MDL號:MFCD00008795
EINECS號:209-831-5
RTECS號:暫無
BRN號:3587204
PubChem號:24889995
物性數據
1. 性狀:為使商品性質穩定,通常為正戊烷溶液。
2. 密度(g/mL,25/4℃): 0.652
3. 相對蒸汽密度(g/mL,空氣=1):未確定
4. 熔點(oC): 未確定
5. 沸點(oC,常壓):未確定
6. 沸點(oC,5.2kPa):70
7. 折射率:未確定
8. 閃點(oC):-6
9. 比旋光度(o):未確定
10. 自燃點或引燃溫度(oC):未確定
11. 蒸氣壓(kPa,25oC):未確定
12. 飽和蒸氣壓(kPa,60oC):未確定
13. 燃燒熱(KJ/mol):未確定
14. 臨界溫度(oC):未確定
15. 臨界壓力(KPa):未確定
16. 油水(辛醇/水)分配系數的對數值:未確定
17. 爆炸上限(%,V/V):未確定
18. 爆炸下限(%,V/V):未確定
19. 溶解性: 溶于正戊烷等。溶于烴類和醚類溶劑。
毒理學數據
暫無
生態學數據
暫無
分子結構數據
暫無
計算化學數據
1.疏水參數計算參考值(XlogP):無
2.氫鍵供體數量:0
3.氫鍵受體數量:1
4.可旋轉化學鍵數量:0
5.互變異構體數量:無
6.拓撲分子極性表面積0
7.重原子數量:5
8.表面電荷:0
9.復雜度:8.4
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:2
性質與穩定性
叔丁基鋰溶液暴露于空氣或濕氣時易起火。對叔丁基鋰的操作應在無水無氧條件下進行,并穿戴好護目鏡、防腐手套等安全裝備。一旦著火,應用干粉滅火器撲滅,千萬不可使用含水或氯代烷烴的滅火器。叔丁基鋰參與的反應必須在隔絕空氣和濕氣的氮氣或氬氣保護下進行。由于反應會放熱,因此應控制反應在低溫下進行。
貯存方法
通常以1.7mol/L戊烷溶液形式貯存、銷售及使用。
合成方法
1. 將鋰與少量鈉一起熔融于干燥的礦物油中,同時加兒滴油酸以防止銼沙粘結。激烈振蕩幾秒鐘后冷卻,在薄薄一層玻璃毛上過濾,用乙醚洗滌,然后將鏗砂轉移到1升的三頸中。此法制得的鈕砂直徑約1毫米,呈淺銀灰色。
在三頸燒瓶上裝置封閉式攪拌器、頂端有氣體導入管的恒壓滴液漏斗和與一個礦物油計泡計連接的氣體導出管(計泡計用來指示氮氣及其它氣體的流通情況)。瓶上的玻璃接頭都應涂上潤沿脂。用袒絲做成的Hershberg攪拌器能更有效地攪動混合物,以避免鏗砂被形成的鹽所復蓋或沉降于瓶底而不再繼續反應。溫度計經氣體導管插入瓶中將三頸燒瓶置于干冰一丙酮浴中冷卻,加300一400毫升乙醚。在一30℃一40℃和2一3小時內,滴加在室溫下與乙醚等體積的叔丁基氯。控制溫度不超過一30℃,以使反應順利進行〔若超過一30℃,會產生更多的不飽和烴而急速逸出氣體;但若過分冷卻,如在一70℃,反應則很慢產率75%。也可用戊烷作溶劑0.2%的金屬鈉和青酮粉未作銼的活化劑來制備此試劑。
2. 通過叔丁基氯與1%~2%的鈉-鋰合金在干燥正戊烷溶劑中反應而來。
用途
1. 羰基化合物的烷基化。脫溴劑。有機合成。
2. 用于重要的鋰試劑。通過鹵素一金屬交換反應而可用于制備其它有機鏗化合物,如芳基鏗、三烷基氫化硼銼、乙烯基銼、a一鏗烷基苯硫醚、β一鏗代烯胺等。在溫和條件下還原撥基成怒基也是聚合反應的引發劑。
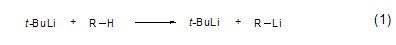
3.叔丁基鋰相比正丁基鋰和異丁基鋰而言,具有更強的堿性和金屬化活性以及更弱的親核性,因此能夠用于質子酸性更弱的烴類底物的脫質子鋰化反應 (式1)[1]。通常,簡單烷烴對于叔丁基鋰仍然能保持惰性,但是對于含雜原子的溶劑如THF則會與叔丁基鋰發生反應。
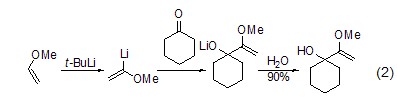
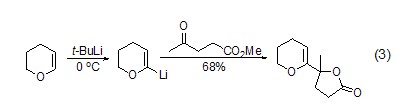
當底物是含雜原子如氧、氮、硫的化合物時,使用叔丁基鋰作脫質子試劑能夠獲得很高的區域選擇性。如乙烯基醚或環醚與叔丁基鋰反應是一種簡單制備α-鋰化乙烯基醚的方法 (式2,式3)[2,3]。
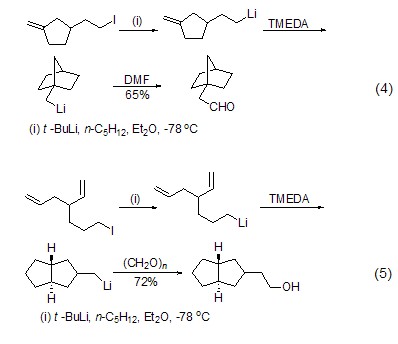
與其它烷基鋰試劑類似,叔丁基鋰對含雜原子取代基的芳烴化合物的鋰化反應同樣具有鄰位鋰化效應。在鋰鹵交換反應中,叔丁基鋰由于其較弱的親核性,因而相比正丁基鋰和異丁基鋰具有更大的優勢。其中,鋰-碘交換反應進行得最為完全、有效,如先在低溫下與6-碘-1-己烯作用發生鋰-碘交換,然后升溫發生高立體選擇性和區域選擇性的5-外環化反應,進而被親電試劑進攻得到官能化產物 (式4)[4]。類似的異構反應也可以用來制備多環化合物 (式5)[5]。
兩當量的舒丁基鋰與α,ω-二碘化合物在–23 oC反應能夠經過α-鋰-ω-碘代烷烴中間體,定量生成五元碳環化合物 (式6)[6]。
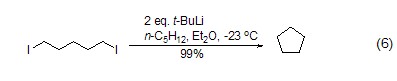
在乙醚或氨的存在下,叔丁基鋰能夠快速加成到烯烴上定量得到新己基鋰 (式7)[7]。值得強調的是叔丁基鋰對碳-碳雙鍵的加成只有在以下幾種情況下才能發生:(1) π-烯烴是共軛的;(2) 環狀烯烴存在較大張力 (式8)[8];(3) 產生的陰離子能夠被底物官能團穩定或支持;(4) 在烯丙基位存在好的離去基團。
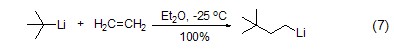
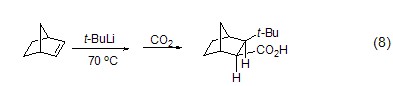
安全信息
危險運輸編碼:UN 3394 4.2/PG 1
危險品標志: 易燃
易燃  腐蝕
腐蝕  危害環境
危害環境
安全標識:S26 S43 S45 S36/S37/S39
危險標識:R11 R15 R17 R34 R38 R65 R67 R50/53
文獻
1. (a) Wakefield, B. J. The Chemistry of Organolithium Compounds, Pergamon: Oxford, 1974. (b) Wakefield, B. J. Organolithium Methods, Academic: San Diego, 1990. (c) Wardell, L. J. In Comperhensive Organometallic Chemistry, Wilkinson, G., Ed.; Pergamon: Oxford, 1982, Chapetr 2. 2. Baldwin, J. E.; Hofle, G. A.; Lever, O. W. J. Am. Chem. Soc., 1974, 96, 7125. 3. Boeckman, R. K.; Bruza, K. J. Tetrahedron Lett., 1977, 4187. 4. Bailey, W. F.; Patricia, J. J.; Del Gobbo, V. C.; Jarret, R. M.; Okarma, P. J. J. Org. Chem., 1985, 50, 1999. 5. (a) Bailey, W. F.; Khanolkar, A. D.; Gavaskar, K. V. J. Am. Chem. Soc., 1992, 114, 8053. (b) Bailey, W. F.; Rossi, K. J. Am. Chem. Soc., 1993, 115, 3080. 6. (a) Bailey, W. F.; Gagnier, R. P.; Patricia, J. J. J. Org. Chem., 1984, 49, 2098. (b) Bailey, W. F.; Gagnier, R. P. Tetrahedron Lett. 1982, 23, 5123. 7. (a) Bartlett, P. D.; Friedman, S.; Stiles, M. J. Am. Chem. Soc., 1953, 75, 1771. (b) Bartlett, P.D.; Stiles, M. J. Am. Chem. Soc., 1955, 77, 2806. (c) Bartlett, P.D.; Tauber, S. J.; Weber, W. P. J. Am. Chem. Soc., 1969, 91, 6362. (d) Bartlett, P.D.; Goebel, C. V.; Weber, W. P. J. Am. Chem. Soc., 1969, 91, 7425. 8. Mulvaney, J. E.; Gardlund, Z. G. J. Org. Chem., 1965, 30, 917. 9.參考書:現代有機合成試劑<性質、制備和反應>;胡躍飛 付華 編著;化學工業出版社;ISBN 7-5025-8542-7
備注
暫無
表征圖譜
統計數據
共收錄化學品數據
147579 條




 滬公網安備 31010602001115號
滬公網安備 31010602001115號