過氧化鋇 Barium Peroxide
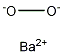
結構式
| 物競編號 | 093G |
|---|---|
| 分子式 | BaO2 |
| 分子量 | 169.33 |
| 標簽 | 二氧化鋇, Barium bioxide, Barium dioxide , Barium superoxide, 氧化劑, 媒染劑, 漂白劑, 引火劑, 催化劑 |
編號系統
CAS號:1304-29-6
MDL號:MFCD00003454
EINECS號:215-128-4
RTECS號:CR0175000
BRN號:暫無
PubChem號:24847364
物性數據
1.性狀:白色或灰白色粉末[1]
2.熔點(℃):450[2]
3.沸點(分解,℃):800[3]
4.相對密度(水=1):4.96[4]
5.溶解性:微溶于水,不溶于乙醇、乙醚、丙酮。[5]
毒理學數據
1.急性毒性[6] LD50:50mg/kg(小鼠皮下)
2.刺激性 暫無資料
生態學數據
1.對是水稍微有危害的不要讓未稀釋或大量的產品接觸地下水、水道或者污水系統,若無政府許可,勿將材料排入周圍環境。
2.生態毒性 暫無資料
3.生物降解性 暫無資料
4.非生物降解性 暫無資料
分子結構數據
1、摩爾折射率:無可用的
2、摩爾體積(cm3/mol):無可用的
3、等張比容(90.2K):無可用的
4、表面張力(dyne/cm):無可用的
5、介電常數:無可用的
6、極化率:無可用的
7、單一同位素質量:169.895071 Da
8、標稱質量:170 Da
9、平均質量:169.3258 Da
計算化學數據
1.疏水參數計算參考值(XlogP):無
2.氫鍵供體數量:0
3.氫鍵受體數量:2
4.可旋轉化學鍵數量:0
5.互變異構體數量:無
6.拓撲分子極性表面積46.1
7.重原子數量:3
8.表面電荷:0
9.復雜度:2.8
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:2
性質與穩定性
1.在酸的作用下可生成相應鋇鹽和過氧化氫。為強氧化劑。有順磁性,與碳共熱時能起去極劑的作用。有毒!吸入有害。
2.在堿土金屬的過氧化物中過氧化鋇最穩定,在水中溶解度最大。室溫下與水形成八水合物,遇酸分解生成H2O2。只要密封就可長期保存。
3.穩定性[7] 穩定
4.禁配物[8] 強還原劑、水、酸類、易燃或可燃物、醇類、二氧化碳、活性金屬粉末
5.避免接觸的條件[9] 撞擊、摩擦、潮濕空氣
6.聚合危害[10] 不聚合
7.分解產物[11] 氧化鋇
貯存方法
儲存注意事項[12] 儲存于陰涼、干燥、通風良好的庫房。庫溫不超過30℃,相對濕度不超過80%。遠離火種、熱源。包裝密封。注意防潮和雨淋。應與還原劑、酸類、醇類、活性金屬粉末、食用化學品分開存放,切忌混儲。儲區應備有合適的材料收容泄漏物。
合成方法
1.過氧化氫-氫氧化鋇合成法 氫氧化鋇與水加熱溶解配成50%的溶液,保溫沉淀4 h,清液注入反應器中,再加水稀釋,攪拌下加入30%過氧化氫于45℃下進行反應,生成的八水過氧化鋇經加熱蒸發、過濾、真空干燥或于110℃干燥2~3 h,即得過氧化鋇成品。其反應方程式如下: 
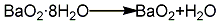
2.過氧化氫-鋇鹽合成法 氯化鋇溶于水中,加入30%過氧化氫。在攪拌下再加^氨水進行反應后,經洗滌、吸濾、于110℃下燥、粉碎,得到過氧化鋇成品。其反應方程式如下:
3.空氣氧化法 硝酸鋇或碳酸鋇在1000~1050℃下煅燒制得氧化鋇多孔性物質,再通入瑣熱至500~600℃不含二氧化碳的干燥熱空氣進行氧化,即得過氧化鋇。其反應方程式如下: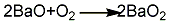
4.氧氣氧化法 將不含二氧化碳及水分的氧氣不斷通入氧化鎖中,在2.02×105~3 03×105Pa壓力下進行氧化,物料冷卻至350~380℃后切斷氧氣,生成產物經粉碎、篩分,即得過氧化鋇成品。
5.疏松的氧化鋇在仔細干燥且不含CO2的O2氣流中,于500℃加熱則得到無水過氧化鋇。將BaO2在O2氣氛中在室溫下干燥一個月可得100%的BaO2。或者用八水合物在真空干燥器中脫水,然后在置有五氧化二磷的真空干燥器中加熱至100℃繼續脫水而制得。八水合物的制法:在飽和的Ba(OH)2的水溶液里,加入3%H2O2即得八水過氧化鋇。
用途
1.用作氧化劑、漂白劑、媒染劑及鋁焊引火劑,碳氫化合物熱裂催化劑。
2.用于制備少量過氧化氫、氧氣或其他過氧化物。
3.用于鋇鹽或過氧化氫的制備,用作氧化劑、漂白劑、媒染劑、消毒劑等。[13]
安全信息
危險運輸編碼:UN 1449 5.1/PG 2
危險品標志: 氧化劑
氧化劑  有害
有害
文獻
[1~13]參考書:危險化學品安全技術全書.第一卷/張海峰主編.—2版.北京;化學工業出版社,2007.6 ISBN 978-7-122-00165-8
備注
暫無
表征圖譜
統計數據
共收錄化學品數據
147579 條




 滬公網安備 31010602001115號
滬公網安備 31010602001115號