二氧化錳 Manganese(IV) oxide
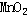
結(jié)構(gòu)式
| 物競(jìng)編號(hào) | 094V |
|---|---|
| 分子式 | MnO2 |
| 分子量 | 86.93 |
| 標(biāo)簽 | 黑色氧化錳, Manganese binoxide, Manganese dioxide, Manganese peroxide, Manganese superoxide, Black manganese oxide, 氧化劑, 催化劑, 干燥劑 |
編號(hào)系統(tǒng)
CAS號(hào):1313-13-9
MDL號(hào):MFCD00003463
EINECS號(hào):215-202-6
RTECS號(hào):OP0350000
BRN號(hào):暫無(wú)
PubChem號(hào):24877699
物性數(shù)據(jù)
1.性狀:深棕色粉末
2.熔點(diǎn)(分解,oC):mp 535
3.密度:5.03 g/cm3
4.溶解性:不溶于水和有機(jī)溶劑。
毒理學(xué)數(shù)據(jù)
1、急性毒性:大鼠口經(jīng)LD50:>3478mg/kg,小鼠植入皮下LC50:422mg/kg。氧化錳粉塵可引起人的錳塵肺。高價(jià)錳氧化物,不論侵入機(jī)體的途徑,其毒性作用對(duì)大腦有損傷。
生態(tài)學(xué)數(shù)據(jù)
對(duì)是水稍微有危害的不要讓未稀釋或大量的產(chǎn)品接觸地下水、水道或者污水系統(tǒng),若無(wú)政府許可,勿將材料排入周?chē)h(huán)境。
分子結(jié)構(gòu)數(shù)據(jù)
1、摩爾折射率:無(wú)可用的
2、摩爾體積(cm3/mol):無(wú)可用的
3、等張比容(90.2K):無(wú)可用的
4、表面張力(dyne/cm):無(wú)可用的
5、介電常數(shù):無(wú)可用的
6、極化率(10-24cm3):無(wú)可用的
7、單一同位素質(zhì)量:86.927878 Da
8、標(biāo)稱質(zhì)量:87 Da
9、平均質(zhì)量:86.9368 Da
計(jì)算化學(xué)數(shù)據(jù)
1.疏水參數(shù)計(jì)算參考值(XlogP):無(wú)
2.氫鍵供體數(shù)量:0
3.氫鍵受體數(shù)量:2
4.可旋轉(zhuǎn)化學(xué)鍵數(shù)量:0
5.互變異構(gòu)體數(shù)量:無(wú)
6.拓?fù)浞肿訕O性表面積34.1
7.重原子數(shù)量:3
8.表面電荷:0
9.復(fù)雜度:18.3
10.同位素原子數(shù)量:0
11.確定原子立構(gòu)中心數(shù)量:0
12.不確定原子立構(gòu)中心數(shù)量:0
13.確定化學(xué)鍵立構(gòu)中心數(shù)量:0
14.不確定化學(xué)鍵立構(gòu)中心數(shù)量:0
15.共價(jià)鍵單元數(shù)量:1
性質(zhì)與穩(wěn)定性
1.如果遵照規(guī)格使用和儲(chǔ)存則不會(huì)分解,未有已知危險(xiǎn)反應(yīng),避免還原劑、易氧化材料、酸、鋁和鋁合金、鹵間化合物.有強(qiáng)氧化性。
2.與冷鹽酸反應(yīng)生成高價(jià)氯化錳的棕色溶液,經(jīng)受熱放出氯氣并形成氯化錳。在氫氣中加熱至200 ℃左右,生成三氧化二錳及四氧化三錳。在熱濃硫酸中放出氧而成硫酸錳。與苛性鈉和氧化劑共熔生成錳酸鹽。與硫黃加熱時(shí),形成二氧化硫及硫化錳。在高溫下遇碳還原成金屬錳。420℃時(shí)遇一氧化碳還原為一氧化錳。遇雙氧水或氯酸鉀發(fā)生催化分解。加熱到535 ℃分解脫氧,生成低價(jià)錳的氧化物。
貯存方法
保持貯藏器密封、儲(chǔ)存在陰涼、干燥的地方,確保工作間有良好的通風(fēng)或排氣裝置。
合成方法
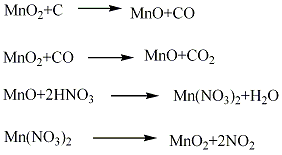
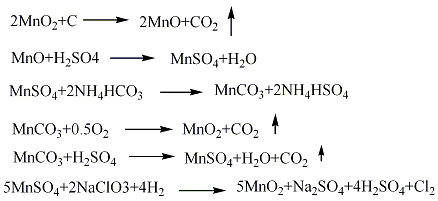
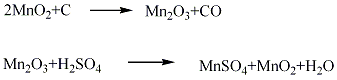
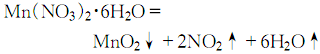
用途
1.主要用在干電池中作去極化劑。是玻璃工業(yè)中的良好脫色劑,可將低價(jià)鐵鹽氧化成高鐵鹽,使玻璃的藍(lán)綠色轉(zhuǎn)為弱黃色。
2.電子工業(yè)中用以制錳鋅鐵氧體磁性材料。煉鋼工業(yè)中用作鐵錳合金的原料,澆鑄工業(yè)的增熱劑。防毒面具中用作一氧化碳的吸收劑。
3.化學(xué)工業(yè)中用作氧化劑(如紫紅素合成)、有機(jī)合成的催化劑、油漆和油墨的干燥劑。也用作火柴工業(yè)的助燃劑,陶瓷、搪瓷的釉藥和錳鹽的原料。還用于煙火,水的凈化除鐵、醫(yī)藥、肥料及織物印染等方面。
4.在有機(jī)合成中,MnO2被用作氧化劑,其反應(yīng)活性與其結(jié)構(gòu)、制備方法以及溶劑極性有關(guān)[1]。
不飽和脂肪醇的氧化 用MnO2能將烯丙基醇轉(zhuǎn)化為α,β-乙烯基醛,當(dāng)醇或胺存在時(shí),酰基氰化物會(huì)醇解或氨解得到相應(yīng)的α,β-乙烯基酯和氨。炔丙基醇可以被MnO2氧化成烷基醛和酮,而不穩(wěn)定的炔丙基醛能進(jìn)一步得到Michael產(chǎn)物 (式1)[2]。
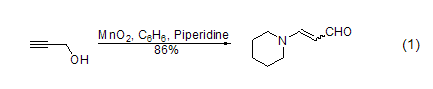
苯基醇和雜環(huán)醇的氧化 共軛芳醛或酮可以由MnO2氧化芳基醇得到,而同時(shí)很多其它的官能團(tuán)卻不會(huì)參與反應(yīng) (式2)[3]。
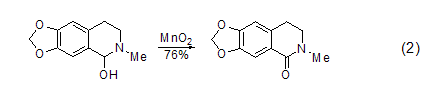
飽和醇的氧化 飽和的脂肪醇和脂肪環(huán)醇與MnO2反應(yīng)可以高產(chǎn)率得到飽和的醛或酮 (式3)[4]。1,2-二醇很容易被MnO2氧化為醛或酮,而1,2-環(huán)二醇則反應(yīng)生成二醛或者是二酮,這在很大程度上決定于反應(yīng)物的結(jié)構(gòu)。
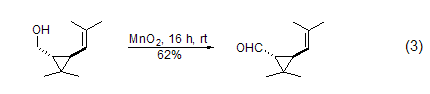
胺與炔的合成 在硼氫化鈉存在下,α,β-不飽和烯醇氧化后可以與胺進(jìn)一步反應(yīng) (式4)[5]。一級(jí)醇在MnO2氧化后用Bestmann-Ohira試劑處理可以得到端炔 (式5)[6]。
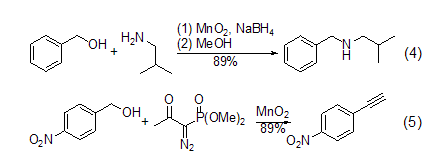
氰基轉(zhuǎn)化為酰胺 在硅膠的參與下,MnO2能把氰基轉(zhuǎn)化為酰胺 (式6)[7]。
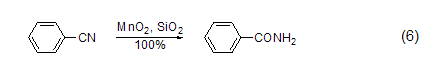
胺類化合物的氧化 用MnO2氧化胺可以得到甲酰胺、重氮化合物等。二烷基羥胺用MnO2氧化會(huì)得到相應(yīng)的硝酮 (式7)[8]。

其它反應(yīng) MnO2也可以用來(lái)發(fā)生其它反應(yīng),如α-羥基酸的裂解、二芳基甲烷的氧化、二芳基酮的轉(zhuǎn)化、醛到羧酸的轉(zhuǎn)化、由硫制備二硫化物、由磷制備磷化物或是由胺制備酮。此外,近兩年興起的在二氧化錳中添加高錳酸鉀的綠色循環(huán)方法也有了廣泛應(yīng)用 (式8,式9)[9]。
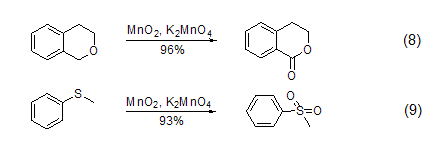
安全信息
危險(xiǎn)運(yùn)輸編碼:UN 3137
危險(xiǎn)品標(biāo)志: 有害
有害
安全標(biāo)識(shí):S25
危險(xiǎn)標(biāo)識(shí):R20/22
文獻(xiàn)
1. Hudlicky, M. Oxidations in Organic Chemistry, American Chemical Society: Washington, 1990. 2. Makin, S. M.; Ismail, A. A.; Yastrebov, V. V.; Petrv, K. I. Zh. Org. Khim., 1971, 7, 21210 (CA 1972, 76, 13712). 3. Hansel, R.; Su, T. L.; Schulz, J. Chem. Ber., 1977, 110, 3664. 4. Crombie, L.; Crossley, J. J. Chem. Soc., 1963, 4983. 5. Kanno, H.; Taylor, R. J. K. Tetrahedron Lett., 2002, 43, 7337. 6. Quesada, E.; Taylor, R. J. K. Tetrahedron Lett., 2005, 46, 6473. 7. Liu, K. T.; Shin, M. H.; Huang, H. W.; Hu, C. J. Synthesis, 1988, 715. 8. Cicchi, S.; Marradi, M.; Goti, A.; Brandi, A. Tetrahedron Lett., 2001, 42, 6503. 9. Shaabani, A.; Mirzaei, P.; Naderia, S.; Lee, D. G. Tetrahedron, 2004, 60, 11415. 10.參考書(shū):現(xiàn)代有機(jī)合成試劑<性質(zhì)、制備和反應(yīng)>;胡躍飛 付華 編著;化學(xué)工業(yè)出版社;ISBN 7-5025-8542-7
備注
暫無(wú)
表征圖譜
統(tǒng)計(jì)數(shù)據(jù)
共收錄化學(xué)品數(shù)據(jù)
147579 條




 滬公網(wǎng)安備 31010602001115號(hào)
滬公網(wǎng)安備 31010602001115號(hào)