五氧化二磷 Phosphorus(V) oxide
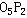
結構式
| 物競編號 | 095Q |
|---|---|
| 分子式 | P2O5 |
| 分子量 | 141.94 |
| 標簽 | 無水磷酸, 磷酸酐, 五氧化磷, Phosphorus pentoxide, Phosphorous oxide (P2O5), Phosphoric anhydride, Diphosphorus pentoxide, 脫水干燥劑, 有機合成縮合劑, 表面活性劑 |
編號系統
CAS號:1314-56-3
MDL號:MFCD00011440
EINECS號:215-236-1
RTECS號:TH3945000
BRN號:暫無
PubChem號:24867015
物性數據
1.性狀:白色粉末,不純品為黃色粉末,易吸潮。[11]
2.熔點(℃):340~360[12]
3.沸點(℃):360(升華)[13]
4.相對密度(水=1):2.39[14]
5.相對蒸氣密度(空氣=1):4.9[15]
6.飽和蒸氣壓(kPa):0.13(384℃)[16]
7.溶解性:不溶于丙酮、氨水,溶于硫酸。[17]
毒理學數據
1.急性毒性[18] LC50:1217mg/m3(大鼠吸入,1h)
2.刺激性 暫無資料
生態學數據
1.生態毒性 暫無資料
2.生物降解性 暫無資料
3.非生物降解性 暫無資料
4.其他有害作用[19] 該物質對環境有危害,應特別注意對水體的污染。
分子結構數據
1、摩爾折射率:無可用的
2、摩爾體積(cm3/mol):無可用的
3、等張比容(90.2K):無可用的
4、表面張力(dyne/cm):無可用的
5、介電常數:無可用的
6、極化率(10-24cm3):無可用的
7、單一同位素質量:141.922095 Da
8、標稱質量:142 Da
9、平均質量:141.9445 Da
計算化學數據
1、 疏水參數計算參考值(XlogP):-2.4
2、 氫鍵供體數量:0
3、 氫鍵受體數量:10
4、 可旋轉化學鍵數量:0
5、 互變異構體數量:
6、 拓撲分子極性表面積(TPSA):124
7、 重原子數量:14
8、 表面電荷:0
9、 復雜度:327
10、 同位素原子數量:0
11、 確定原子立構中心數量:0
12、 不確定原子立構中心數量:0
13、 確定化學鍵立構中心數量:0
14、 不確定化學鍵立構中心數量:0
15、 共價鍵單元數量:1
性質與穩定性
1.溶于水生成磷酸。固體物氧化磷有三種晶形。H型:屬于亞穩定性,熔點為420℃,沸點為340℃,升華溫度為360℃。O型:斜方晶形,H型在封閉管中400℃加熱2h則變為O型,熔點為562℃,沸點為605℃。O′(T)型:正方晶系,H型在封閉管中于450℃加熱24h則生成O’(T)型,熔點為580℃,沸點為605℃。
2.穩定性[20] 穩定
3.禁配物[21] 鉀、鈉、水、醇類、堿類、過氧化物
4.避免接觸的條件[22] 潮濕空氣
5.聚合危害[23] 不聚合
6.分解產物[24] 氧化磷
貯存方法
儲存注意事項[25] 儲存于陰涼、干燥、通風良好的庫房。遠離火種、熱源。庫溫不超過25℃,相對濕度不超過75%。包裝必須密封,切勿受潮。應與活性金屬粉末、堿類、過氧化物、醇類等分開存放,切忌混儲。儲區應備有合適的材料收容泄漏物。
合成方法
1.氧化法 將黃磷加熱熔融后,送入氧化燃燒爐,用干燥空氣(經濃硫酸脫水)進行氧化燃燒反應,生成五氧化二磷因受熱而升華,在爐頂遇冷而落入氧化燃燒爐底部的沉降室內,制得五氧化二磷成品。由氧化燃燒爐逸出的尾氣經旋風分離器以回收五氧化二磷粉塵。回收成品與沉降室中的產品一起作為成品包裝。其4P+5O2→2P2O5以試劑級五氧化二磷為原料,在充分干燥的氧氣氣流中灼燒升華提純,經冷凝器捕集升華物,制得高純五氧化二磷成品。
2.在廣口瓶上安裝一個用馬口鐵制成的寬口漏斗,漏斗上倒罩著一個比漏斗口小的襯錫的馬口鐵圓筒(直徑350mm,高500mm)。圓筒底部裝入通氣彎管,中上部開有一口,是用來安裝燃燒勺用的。加熱燃燒勺,向勺中放入干燥的白磷,迅速插入圓筒中,并借燃燒勺柄上的塞子固定在圓筒上。當磷燒盡后再重復此操作。通氣強度和燃燒速度可由調節圓筒與漏斗間的縫隙大小控制。燃燒生成的氧化磷在圓筒內壁上冷卻。輕輕敲動圓筒就落入廣口瓶中。提純市場上或上述所制得的氧化磷常含有磷的低價氧化物,有時還含有黃磷,一般實驗可直接使用,欲需要較純的可進一步在干燥的氧氣流中灼燒升華制取。將一干燥清潔的T型管倒置,管口上安裝放有起始原料的P2O5玻管。從T型管的一端通入經CaCl2干燥的氧氣,另一端接玻璃冷卻管。將待灼燒升華的P2O5放入T型管中加熱。200g市售樣品在2h后可得到大約70g純品。以試劑級五氧化二磷為原料,在充分干燥的氧氣氣流中灼燒升華提純,經冷凝器捕集升華物,制得高純五氧化二磷成品。
3.在預先經濃硫酸、固體氫氧化鉀和工業品五氧化二磷干燥過的純氧氣流作用下,將工業品五氧化二磷升華提純,可得不含低級氧化物的五氧化二磷。
用途
1.用作生產高純度磷酸、磷酸鹽類和磷酸酯的原料,也用于五氧化二磷溶膠和以H型為主的氣溶膠的制造。
2.可用作氣體和液體的干燥劑、有機合的脫水劑。合成纖維的抗靜電劑及糖的精制劑。還用于制造光學玻璃、透紫外線玻璃、隔熱玻璃、微晶玻璃和乳濁玻璃等,以提高玻璃的色散系數和透過紫外線的能力。
3.五氧化二磷主要用于干燥劑、有機合成的脫水劑和關環反應的催化試劑。
酰胺脫水成腈 酰胺用五氧化二磷脫水可以制備腈。未取代的酰胺與過量的五氧化二磷共蒸餾可以高產率制備腈 (式1)[1]。很多反應是在無溶劑條件下進行的,有時可以用高沸點的溶劑。

催化重排反應 10%濃度的五氧化二磷甲磺酸溶液 (Eaton試劑) 是有效的酸性環合試劑,可以有效的代替多磷酸 (PPA),例如用于Beckman重排 (式2,式3)[2,3]。

Eaton試劑還能促進共軛不飽和炔類化合物關環 (式4)[4]。
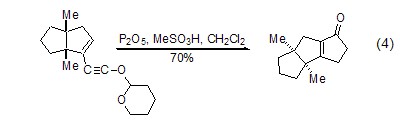
脫水環合反應 P2O5在高溫下能使反應物脫水而環化 (式5)[5],這是制備異喹啉的一個重要方法。
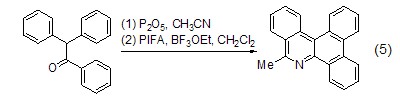
合成脂環化合物時,P2O5也是非常有效的關環的催化劑 (式6)[6]。
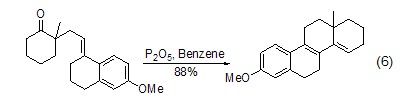
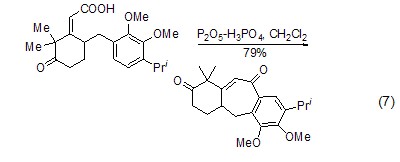
有時要加入磷酸促進關環的進行 (式7)[7]。
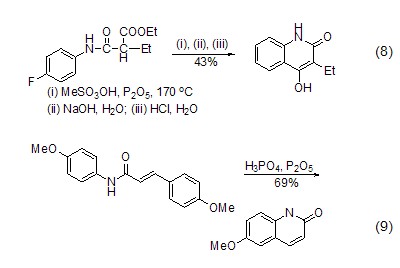
合成含氮雜環 通過加熱五氧化二磷和含氮酮或醇是一種合成含氮雜環化合物的通用方法 (式8,式9)[8,9]。
合成碘代物 在磷酸/五氧化二磷的催化下,一級醇與KI反應得到1-碘代物 (式10)[10]。
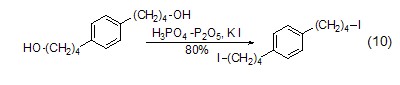
4.用作干燥劑、脫水劑,用于制造高純度磷酸、磷酸鹽及農藥等。[26]
安全信息
危險運輸編碼:UN 1807 8/PG 2
危險品標志: 腐蝕
腐蝕
危險標識:R35
文獻
1. Camps, P.; Munoz-Torrero, D.; Simon, M. Synth. Commun., 2001, 31, 3507. 2. Hilmey, G. D.; Paquette, L. A. Org. Lett., 2005, 7, 2067. 3. Eshghi, H.; Gordi, Z. Synth. Commun., 2003, 33, 2971. 4. Srikrishna, A.; Dethe, D. H. Org. Lett., 2003, 5, 2295. 5. Churruca, F.; SanMartin, R.; Carril, M.; Urtiaga, M. K.; Solans, X.; Tellitu, I.; Dominguez, E. J. Org. Chem., 2005, 70, 3178. 6. Saraber, F. C. E.; Groot, A. Tetrahedron Lett., 2004, 45, 9431. 7. Ning, C.; Wang, X.; Pan, X. Synth. Commun., 1999, 29, 2115. 8. Freeman, G. A.; Andrews, C. W. III; Hopkins, A. L.; Lowell, G. S.; Schaller, L.T.; Cowan, J. R.; Gonzales, S. S.; Koszalka, G. W.; Hazen, R. J.; Boone, L. R.; Ferris, R. G.; Creech, K. L.; Roberts, G. B.; Short, S. A.; Weaver, K.; Reynolds, D. J.; Milton, J.; Ren, J.; Stuart, D. I.; Stammers, D. K.; Chan, J. H. J. Med. Chem., 2004, 47, 5923. 9. Inglis, S. R.; Stojkoski, C.; Branson, K. M.; Cawthray, J. F.; Fritz, D.; Wiadrowski, E.; Pyke, S. M.; Booker, G. W. J. Med. Chem., 2004, 47, 5405. 10. Hamze, A.; Rubi, E.; Arnal, P.; Boisbrun, M.; Carcel, C.; Salom-Roig, X.; Maynadier, M.; Wein, S.; Vial, H.; Calas, M. J. Med. Chem., 2005, 48, 3639. [1~10]參考書:現代有機合成試劑<性質、制備和反應>;胡躍飛 付華 編著;化學工業出版社;ISBN 7-5025-8542-7 [11~26]參考書:危險化學品安全技術全書.第一卷/張海峰主編.—2版.北京;化學工業出版社,2007.6 ISBN 978-7-122-00165-8
備注
暫無
表征圖譜
統計數據
共收錄化學品數據
147579 條




 滬公網安備 31010602001115號
滬公網安備 31010602001115號