基于 NMR的代謝組學研究
- 2012-12-07
- 專題
代謝物是生命過程中發生的生物化學反應的產物,能夠從某種程度上反映生命過程的本質。雖然人們對代謝物和代謝水平的認識和研究已經有上百年的歷史,但是,將生物體作為一個整體進行研究的代謝組學(metabonomics/metabolomics),成為分子病理、基因功能分析和系統生物學研究的強有力的技術平臺只有7年的歷史。1998年Tweeddale等[1]在研究大腸桿菌的代謝時提出了代謝組(Metabolome)這個概念用來表示代謝物整體(total metabolite pool),并且指出,代謝組分析能夠提供有關細胞代謝和調控的信息。Nicholson等[2]在1999 年提出代謝組學的概念(metabonomics)時將其定義為:對病理/生理刺激或基因改變時生物體系的動態代謝響應的多參數定量分析(the quantitative measurement of the dynamic multiparametric metabolic responses of living systems to pathophysiological stimuli or genetic modification)。Metabonomics一詞來自希臘文的詞根“meta”和“nomos”。“meta”意思是“變化(change)”,“nomos”意思是“規律”或“原則”(就象 economics)。從這個定義本身不難看出,代謝組學分析的對象是生物體本身,而且是一個動態的整體。Nicholson研究組的工作包括動物體生理[3~5]、藥物毒理[6~9]、分子表型學[10,11]、疾病診斷[12~14]和以系統生物學為基礎的功能基因組學[15~17]。Fiehn等[18]在2000年,Raamsdonk 等[19]在2001 年又提出了metabolomics這個單詞,用以強調把代謝組學這個技術平臺用于研究細胞系統基因的功能。目前,metabolomics有多個定義,但其本質是:給定細胞在給定時間和環境下的所有小分子代謝物的定量分析(the quantitative measurement of all low molecular weight metabolites in an organism's cells at a specified time under specific environmental conditions)。所以從定義來看,metabolomics指的是靜態生物體系代謝組分析,因此可以認為是 metabonomics 的一部分。事實上,近年來也有動態代謝組學(dynamic metabolomics)[20]提法出現,說明metabolomics的含義正在朝著metabonomics靠近。在中文的表述中,沒有必要將兩個名詞分開,一律用“代謝組學”以避免不必要的名詞混淆。2002年以來,Nicholson等[21]和Fiehn等[22]分別撰寫綜述文章從不同的角度闡明代謝組學是研究藥物毒性和基因功能的平臺技術,以及聯結基因型和性狀表型的有力工具。這一系列論述奠定了代謝組學的基礎。代謝組學的出現,主要得益于分析技術的發展使得對大量樣品和大量代謝物的快速定量測定成為可能,而最為常用的方法是核磁共振(NMR) 和質譜(MS)(圖1) 。
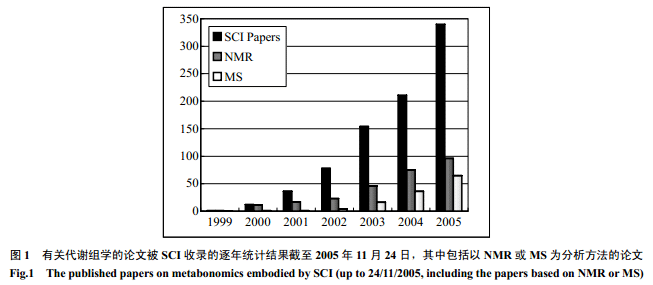
1 代謝組學的發展趨勢
代謝組學是一個全新的研究熱點。這主要表現在:第一、代謝組學的研究論文數正在以指數方式增長(圖1);第二、高影響因子(>8.0) 學術刊物上發表的論文數量較多(>60 篇)[17~19,21,23~81];第三、核心論文引用率高,其中引用100 次以上的有6篇,單篇最高引用接近240 次;第四、研究范圍廣泛并不斷增加,涉及到功能基因組學、營養學、病理學、藥理學、毒理學、植物學、微生物學以及系統生物學等眾多領域;第五、儀器和分析技術的快速發展為代謝組學的進步提供了更加廣闊的空間,也就帶來了更多的挑戰和機會。不斷提高的磁場強度使得核磁共振譜儀的分辨率有了更進一步的提升,超低溫探頭的出現也讓 NMR的檢測靈敏度有了一定程度的提高。自動進樣技術極大的縮短了大批量樣品的檢測時間。而計算機技術的飛速發展為數據分析的速度和可靠性提供了更有力的支撐。
2 代謝組學與基因組學、蛋白質組學的關系
代謝組學研究的是在病理生理刺激或基因改變條件下生物體系代謝水平的應答,此前提出的基因組學和蛋白質組學則分別從基因水平和細胞蛋白表達水平研究生物體系對藥物刺激的響應。每個物種的基因組所含的基因序列與基因數目相對固定,但這些基因的表達水平會隨著發育階段不同或外部條件的變化而變化。從藥物研究和毒理學的角度來看,基因組學研究的是生物體受外源性藥物刺激后基因表達的改變,然而基因表達的改變或者調節與細胞系統整體功能之間的關系尚不清楚。因此蛋白質組學方法主要針對給藥或其它病理生理過程引起的細胞蛋白質組成的變化進行半定量測量[82~84]。盡管與基因組學相比,蛋白質組學研究不那么昂貴,但是由于蛋白質數量眾多,現有蛋白組學手段通量有限,因此勞動強度較大,進展緩慢。同時必須指出,基因組、轉錄組和蛋白質組研究更強調生命過程的調控機制和物質基礎,而代謝組是以體內生物化學反應的產物的整體變化為出發點來研究生命過程的本質。事實上,多數哺乳動物(如人)是動物體本身(宿主)和消化系統微生物菌群共同進化、協同工作的“協同生物體”(symbiotic species)[85],對宿主本身的基因,蛋白質的認識只是該體系的一小部分[86]。因此,基因組、轉錄組、蛋白質組和代謝組是從不同層面和水平上研究生命過程的途徑。
基因和蛋白質數量眾多,它們的功能除了與一級和二級結構有關外,在更多情況下與它們的三級結構、動力學過程和相互作用有關。這也是功能基因組學和功能蛋白質組學研究的重點。與此形成對比的是,代謝物分型要少得多。目前已知的代謝物只有幾千種。由于代謝物是生命過程的終端產物,不僅分子量小而且在所有的生物體中都是相同的,因此,一般不存在三維結構和動力學的問題,也不要求完整的基因序列或者龐大的 EST(Expression Sequence Tag)數據庫。基因和蛋白表達具有重復性,由此導致的代謝物或代謝水平的變化則具有累加性。這種含量上的放大效應,使得代謝物的識別比基因或蛋白質的識別要容易得多。有限的代謝物分型必然導致一種代謝物同時涉及多個代謝過程或代謝循環。每個代謝循環會產生多個代謝物,不同代謝循環之間相互聯系、互相影響。代謝組學正是從代謝物整體變化的角度來研究生物體對各種刺激的動態響應。
3 代謝組學研究方法
體液中的代謝物質與細胞以及組織中的代謝物質處在一個動態的平衡當中,所以當機體由于毒性或代謝障礙導致組織細胞出現異常的時候,生物體液的組成就會產生變化。代謝組學研究方法就是檢測代謝物水平的整體和動態變化,提取潛在的有診斷或常規程序化價值的生化信息,以此來反映生物體在外源刺激作用下真實的體內的生物學過程,建立“組學”參數的輸入與響應輸出之間的聯系。
代謝物整體水平的檢測所依賴的方法是分析化學中的各種譜學技術,如核磁共振波譜、質譜、高效液相色譜、紅外光譜、紫外可見光譜以及各種原子光譜等。對海量譜學數據進行統計和歸類分析,從中提取代謝特征或代謝時空的整體變化規律,是分析化學中的化學計量學或化學信息學的研究范疇。值得指出的是,代謝組學所強調的代謝特征或代謝時空的整體變化,不是傳統意義上的某種代謝物或少數幾種代謝物含量和存在方式的變化。建立代謝特征或代謝時空的變化與生物體特性的變化之間的有機聯系,是代謝組學研究的最終目標。因此,分析化學在代謝組學研究中發揮著非常重要的作用,甚至是不可取代的作用。
3.1 代謝組學的研究過程
代謝組學研究一般包括四個步驟:第一步,給予生物體一定的刺激。這種刺激可以是基因的變異、剔除或引入,體內生物過程的催化或抑制,致病或致病物質(無機、有機、病毒、細菌、寄生蟲等等)的引入,以及各種環境因素的改變等等。除了刺激因素之外,引入刺激的時間和強度等也需要精心設計。適合于代謝組學研究的樣品種類非常廣泛,可以說是無所不包,例如尿液、血液、組織或組織提取物、器官甚至整個生物體等等。樣品收集時間、部位、種類等應給予充分考慮。第二步,代謝組數據的采集。用核磁共振、質譜、色譜等分析手段測定其中代謝物的種類、含量和狀態以及其變化。第三步,建立表征代謝特征的時空模型[87]。在代謝組學中最常用的建模方法是主成分分析(Principle Components Analysis, PCA)。PCA 是對多變量數據進行統計處理的一種數據線性投影方法,它在保留原有信息的基礎上將高維空間中的樣本投影到較低維的主成分空間中。其基本思路是以一種最優化方法濃縮數據,尋找幾個由原始變量線性組合而成的主成分,以揭示原始數據的特征,提取基本信息,實現對數據的可視化和樣本的分類聚集。用PCA 方法建立的以代謝物的種類、含量和狀態隨時間的變化為基礎的代謝物時空模型應能夠清楚地反映出外源性刺激的種類、程度和動態變化以及引起樣本在時空模型中的不同分布的標志性代謝物。第四步,建立代謝物時空變化與生物體特性的關系,達到從不同層次和水平上闡述生物體對相應刺激的響應的目的。
3.2 基于 NMR的代謝組學的特點
作為眾多化學分析方法中的一種,NMR在代謝物組學的研究中起著非常重要的作用。這主要取決于NMR所具有的優勢:首先,用NMR分析生物體液等復雜混合物時樣品的前處理簡單,測試手段豐富,包括液體高分辨NMR、高分辨魔角旋轉(HR-MAS)NMR 和活體核磁共振波譜(MRS),因此,能夠在最接近生理狀態的條件下對不同類型的樣品進行檢測。其中需要特別提到HR-MAS方法,該方法是將樣品在與靜磁場成魔角(54.7°) 的方向旋轉,消除了磁場不均勻性、化學位移各向異性和偶極-偶極相互作用帶來的譜線增寬影響,從而可以獲得與液體高分辨 NMR相媲美的分辨率。更重要是,這種方法對代謝物在組織中的定位有獨特的優點,目前已經有不少將此方法用于肝臟[88~90],腦組織[91~93],前列腺[94~96]等組織的研究報道。其次,NMR是一種無損的多參數和動態分析技術,NMR同時具有定性分析和定量分析功能,并且通過單次檢測可以得到所有含量在NMR檢測限以上的物質(含有 NMR可觀測核的物質)的特征NMR譜,以及這些物質在整個刺激周期中的動態變化,而且NMR譜攜帶有豐富的分子結構和動力學信息;再次,NMR檢測可以在很短的時間內完成(一般5~10 min),這對于實現高通量樣品檢測和保證樣品在檢測期內維持原有性質來說是至關重要的。此外,流動探頭、自動進樣技術和自動 NMR譜處理技術的出現和不斷完善,也使得測定速度和準確性不斷提高。而且,核磁共振手段靈活多變,通過操控脈沖序列我們可以獲得多種多樣的信息。例如代謝組學中常用到的譜編輯手段[88,97~99]:使用單脈沖、CPMG(Carr-Purcell-Meiboom-Gill)和擴散加權序列,可以分別獲得樣品中不同官能團、不同分子量或不同存在狀態的分子的1H NMR譜。
當然NMR方法也有其局限性,例如它的檢測靈敏度較低,而且檢測動態范圍有限,很難同時檢測同一樣品中含量相差很大的物質。色譜(LC)以其卓越的分離能力,質譜(MS)技術以其普適性、高靈敏度和專一性,也成為代謝組學中重要的分析手段,但是它們也存在各自的缺陷,如色譜和質譜的選擇性檢測能力較差、大量譜峰的識別以及方法的重現性問題、質譜中不同離子化程度對代謝物定量的影響等。
4 代謝組學研究的廣泛應用
代謝組學經過幾年的發展,方法正日趨成熟,其應用已經滲入生命科學研究的方方面面,并日益彰顯出其強有力的科學潛能。
4.1 藥物開發、安全性評價
快速發展的醫藥工業對分析手段的效率以及可靠性提出了更高的要求。藥物直接或者通過某些代謝途徑產生的代謝物使基因表達產生改變,基因表達的改變又會影響蛋白質的合成,基因與蛋白質的變化都可以造成毒理終點的產生;另外藥物通過代謝進入血液,進而分布到一些組織器官產生作用,也能形成毒理終點。而毒理終點造成的生化改變是 NMR所能檢測到的。對 NMR數據采用適當的化學計量學和多變量分析方法,就能提取出豐富的藥物代謝信息。因此代謝組學在制藥工業中發揮著巨大的作用:在藥物開發階段,代謝組學不僅可以進行早期活體毒理測試,而且能為藥物分子的篩選提供依據;在藥物臨床應用前,它能幫助確定藥物的安全性生物標記物和代謝表型,并能評價將動物模型實驗應用于人類疾病的可行性。
Nicholson研究組多年的實驗發現:基于NMR的代謝組學方法不僅能區分組織器官的正常與非正常的狀態,而且能給出毒性作用的靶器官以及作用機制,識別出毒性的生物標記物。他們的工作主要集中在藥物對腎臟、肝臟毒性的研究上,通過長期的實驗經驗積累,他們將體液的磁共振波譜分解成一系列的“生物標記物窗口”,這些“窗口”分別與特定的器官毒性相對應,從而可以從簡單的1D1H NMR譜獲取豐富的毒理信息[21]。在藥物毒理代謝組學的研究領域,最為矚目的工作是國際COMET(Consortium for Metabonomic Toxicology)計劃[100,101],該計劃由五家著名的制藥公司與英國帝國理工學院聯合完成,旨在用嚙齒動物的尿液、血液的1H NMR譜建立代謝組數據庫,并為目標器官及其位點的毒性建立預測性專家系統。在完成約147種毒性模型的實驗研究后,他們已經建立起了第一個基于機器學習的實驗室嚙齒動物肝臟和腎臟毒性預測的專家系統。
4.2 病理學研究
由于病理狀態造成的代謝紊亂同樣也是核磁共振技術所能檢測的,同時,機體任何部分出現異常狀態,在體液的組成上都會有反映。
相對于傳統的醫療診斷方法,代謝組學方法具有無創性及樣品制備簡單等優點,因此其應用范圍涵蓋了先天性代謝缺陷、腎臟和肝臟移植、Alzheimer疾病、癌癥等廣泛的領域[102~104]。其中典型的例子是冠心病的研究。冠心病以前主要通過血管造影術來診斷,該方法不僅昂貴,而且伴隨有不良反應,甚至可能導致死亡。而 Brindle 等[25]用代謝組學方法用于冠心病診斷,結果顯示經過正交信號校正(OSC) 的模式識別方法能很好的區分重癥冠心病(三支血管疾病,TVD)和冠狀動脈正常人的血清。另外,對于傳統的測量血壓、總膽固醇、總甘油三脂、纖維蛋白素原、白細胞數量等冠心病危險度因子(risk factor)無法區分的不同嚴重程度的冠心病,代謝組學方法也能很好的區分,并且通過回歸分析,發現VLDL、LDL、HDL和膽堿等是導致兩者區分的主要因素。他們也用代謝組學方法對不同程度的高血壓病人作了研究[12],發現導致不同收縮壓(Systolic Blood Pressure, SBP)的因素是血清中脂蛋白顆粒的組成,如脂肪酸側鏈的不飽和度、脂蛋白分子之間相互作用的強度,而不是脂類的絕對含量。多種癌癥[96,105](乳腺癌、卵巢癌、肝癌、前列腺癌、腦腫瘤)、先天性障礙[102~104]等疾病在代謝組學方法的指引下也有了許多新的發現。最近,wang等[44]用代謝組學方法研究了血吸蟲病對嚙齒動物尿液代謝的影響,發現血吸蟲的侵染嚴重擾亂了體內三羧酸循環等代謝過程,并對腸道菌群的代謝產生了影響。可以預見,代謝組學在分子病理和疾病診斷等領域將有廣闊的應用前景。
4.2 營養代謝組學
代謝組學的方法可以幫助識別和常量營養物的最終攝入效應密切相關的代謝物,并且有助于定義各種常量營養物的正常攝入范圍。從長遠來看,代謝組學的研究可以幫助理解當單一的養分(如氨基酸等)攝入過多或者過少時整個機體的新陳代謝會發生怎樣的改變。除此之外,這也是一個在考慮到代謝的復雜性的基礎上合乎科學地建立常量營養物的合理攝入范圍的評估策略。
Solanky 等[106]對進食含有(結合態或非結合態)大豆異黃酮的食物的女性的尿液進行了檢測。結果發現,由于大豆異黃酮的攝入,導致了尿液中的氧化三甲胺明顯升高,對氧化三甲胺的升高有兩種可能的解釋:(1)動物實驗表明大豆蛋白對損傷的腎臟有明顯的保護作用,而氧化三甲胺含量的升高以及伴隨發生的甜菜堿、膽堿、肌酸和肌酐含量的變化,標志著腎功能的增強;(2)氧化三甲胺、甜菜堿、膽堿等都是微生物代謝的中間產物,因此進食含有豐富大豆異黃酮的食物,可能擾動了腸道微生物菌群。谷氨酸和谷氨酰胺的上升表明三羧酸(TCA) 循環受到了影響,因為它們可以很容易轉化成 TCA 循環的中間產物。另外檸檬酸的下降和糖含量的改變標志著糖酵解速率的下降,從而影響到糖類的代謝。而甲胺通路的中間產物以及膽堿、甜菜堿、甘氨酸和乙酸鹽的含量變化表明脂類和膽固醇的代謝、轉移發生了改變。以上結果顯示出基于 NMR的代謝組學能夠給出復雜生物體系對飲食改變的精細生化響應。
幾個世紀以來,菊花茶作為一種功能性飲料一直為人類所飲用,起到抗炎、抗氧化和抗菌等保健作用。Wan g等[107]對持續飲用歐洲黃菊的志愿者的尿液進行了分析,通過正交信號校正的模式識別方法排除了性別、飲食的影響,提取出了僅僅和此花攝入有關的代謝信息。研究結果表明:由于菊花的抗氧化作用導致了尿液中的肌酸酐的下降,而馬尿酸和苯乙酰基谷酰胺含量的上升則表明了由于菊花的抗菌作用對人體腸道菌群產生了一定的影響,而這種影響最終造成了什么效果等問題還有待進一步回答。
4.3 功能基因組的研究
代學組學應用于功能基因組學是基于這樣一種觀點:基因產生變異的生物體在生長速率等表型上可能沒有顯著的改變,這是因為細胞內的代謝物濃度的改變補償了變異產生的影響。但是這也同時意味著生物體在代謝表型上可能會有顯著的變化[108]。譬如,無論從遺傳還是代謝的角度看,傳統認為,Han Wistar (HW)和Sprague Dawley (SD) 兩個大鼠系十分接近,而且兩個系均廣泛地被用于藥物的研制。可是代謝組學研究發現,它們的尿液代謝組有本質的區別。Bundy等[11,109]用代謝組學方法研究蚯蚓的表型時發現,幾種形態上并無區別的蚯蚓,其體腔液(coelomic fluids)和組織代謝組有明顯的區別。這些例子都表現出代謝組學方法的高靈敏性。
剔除或過表達蛋白編碼基因很可能導致多種代謝物的濃度發生變化,因此理論上定量研究變異產生的代謝物濃度的相對變化有可能可以識別基因產物的作用位點。另外,由于具有相似變化的基因具有相似的功能,所以可以將剔除一個未知功能的基因所產生的細胞代謝上的變化,與剔除已知功能基因所產生的代謝變化進行比較,從而確定未知基因的功能,這就為我們研究基因的生物學功能提供了理論依據和新的途徑。了解基因變異帶來的功能上的改變對于建立和驗證新的人類疾病模型有著非常重要的意義。而且用代謝組學的方法評價基因修飾在植物改良中的安全性也有著巨大的潛力。
Raamsdonk等[19]利用FANCY(Functional ANalysis by Co-responses in Yeast)方法對野生型 FY23及其6種突變株進行了研究。這6種突變株分別是選擇性剔除了 PFK26、PFK27、PET27、PET191、COX5a和ρ。在培養的指數生長中期分別對其代謝物進行提取,并獲取1H NMR譜。實驗數據的 PCA方法分析結果表明,代謝組學方法能對具有相關生物活性的基因進行分類,能正確地區分性質上相似、程度上不同的表型突變。甚至基因表型緘默的幾種突變體也能夠被明顯區分為呼吸缺陷突變體、部分呼吸缺陷突變體和控制組三類。
代謝組學還參與到了 BAIR(Biological Atlas of Insulin Resistance) 計劃當中。BAIR計劃是由英國倫敦大學帝國理工學院、女王瑪麗與威斯特菲爾德學院,劍橋大學和牛津大學合作,由英國 Wellcome Trust功能基因組發展倡議基金資助的一個項目(http://www.bair.org.uk/) ,其目標是用包括代謝組學在內的各種組學、生物信息學、嚙齒動物基因打靶、人類遺傳學以及結構生物學等手段,研究胰島素作用和導致胰島素抵抗的分子機制,并對處于正常或紊亂狀態的胰島素行為作出系統的分子描述,以對人類的遲發糖尿病、肥胖癥、高血壓和冠心病等疾病作出相應的解釋,從而使人類能更合理、有效的處理和防止這類疾病的發生。
5 機遇和挑戰
整體來講,代謝組學研究仍然處于早期發展階段,面臨著方法學和廣泛應用兩方面的挑戰。儀器和分析技術的發展,特別是基于計算機的模式識別和專家系統的發展將對基于 NMR的代謝研究的進步產生巨大的推進作用。但是,仍有大量方法學上的問題需要解決:生物體系的復雜性決定了生物體液以及生物組織組成的復雜性,從而造成了 NMR譜峰的重疊,對物質的歸屬和精確定量造成一定的影響;NMR方法的低靈敏度也是一直困擾 NMR工作者的一個問題;現有的代謝組學數據分析方法對高含量物質濃度的變化有很好的識別能力,但是對低含量代謝物分析的準確性和可靠性都較低,然而在某些情況下這些低含量的物質往往攜帶了重要的信息。雖然科研工作者已經得到了大量與重要生理病理變化或基因變異等有關的標志性代謝物,但是離建立完整的診斷專家系統,實現診斷常規化還有很長的距離。
盡管代謝組學的應用領域已經涉及到功能基因組學、營養學、病理學、藥理學、毒理學、植物學、微生物學、昆蟲/動物、系統生物學等諸多領域,但是在這些領域里的代謝組學還有許多具體應用的潛在價值可以發掘。相信隨著代謝組學應用的廣度和深度的不斷增加,我們將會更充分認識到其優越性,這也將為人類更高效、準確的評價藥物的安全性、更全面的認知疾病過程,甚至于指導人類的營養健康、監測環境等提供一種有力的手段。
參考文獻
[1] H Tweeddale, L Notley-McRobb, T Ferenci. J. Bacteriol., 1998, 180: 5109~5116.
[2] J K Nicholson, J C Lindon, E Holmes. Xenobiotica, 1999, 29: 1181~1189.
[3] M E Bollard, E G Stanley, J C Lindon et al. NMR Biomed., 2005, 18: 143~162.
[4] E G Stanley, N J C Bailey, M E Bollard et al. Anal. Biochem., 2005, 343: 195~202.
[5] T M D Ebbels, E Holmes, J C Lindon et al. J. Pharm. Biomed. Anal., 2004, 36: 823~833.
[6] A W Nicholls, J K Nicholson, J N Haselden et al. Biomarkers, 2000, 5: 410~423.
[7] M Coen, E M Lenz, J K Nicholson et al. Chem. Res. Toxicol., 2003, 16: 295~303.
[8] M Coen, S U Ruepp, J C Lindon et al. J. Pharm. Biomed. Anal., 2004, 35: 93~105.
[9] N J Waters, E Holmes, C J Waterfield et al. Biochem. Pharmacol., 2002, 64: 67~77.
[10] J L Griffin, L A Walker, S Garrod et al. Comp. Biochem. Physiol. B Biochem. Mol. Biol., 2000, 127: 357~367.
[11] J G Bundy, D J Spurgeon, C Svendsen et al. FEBS Lett., 2002, 521: 115~120.
[12] J T Brindle, J K Nicholson, P M Schofield et al. Analyst, 2003, 128: 32~36.
[13] J L Griffin, S A Bonney, C Mann et al. Physiol. Genomics, 2004, 17: 140~149.
[14] J T Brindle, H Antti, E Holmes et al. Nat. Med., 2002, 8: 1439~1444.
[15] C L Gavaghan, E Holmes, E Lenz et al. FEBS Lett., 2000, 484: 169~174.
[16] C L Gavaghan, I D Wilson, J K Nicholson. FEBS Lett., 2002, 530: 191~196.
[17] R J Bino, R D Hall, O Fiehn et al. Trends Plant Sci., 2004, 9: 418~425.
[18] Fiehn, J Kopka, P Dormann et al. Nat. Biotechnol., 2000, 18: 1157~1161.
[19] L M Raamsdonk, B Teusink, D Broadhurst et al. Nat. Biotechnol., 2001, 19: 45~50.
[20] M Varnau, A Singhania. Genet. Eng. News, 2002, 22: 15.
[21] J K Nicholson, J Connelly, J C Lindon et al. Nat. Rev. Drug Discov., 2002, 1: 153~161.
[22] Fiehn. Plant Mol.Biol., 2002, 48: 155~171.
[23] J L Griffin, J P Shockcor. Nat. Rev. Cancer, 2004, 4: 551~561.
[24] A R Fernie, R N Trethewey, A J Krotzky et al. Nat. Rev. Mol. Cell Biol., 2004, 5: 763~769.
[25] J T Brindle, H Antti, E Holmes et al. Nat. Med., 2002, 8: 1439~1444.
[26] J Allen, H M Davey, D Broadhurst et al. Nat. Biotechnol., 2003, 21: 692~696.
[27] H Jenkins, N Hardy, M Beckmann et al. Nat. Biotechnol., 2004, 22: 1601~1606.
[28] J K Nicholson, E Holmes, J C Lindon et al. Nat. Biotechnol., 2004, 22: 1268~1274.
[29] A Macchiarulo, I Nobeli, J M Thornton. Nat. Biotechnol., 2004, 22: 1039~1045.
[30] M Brazil. Nat. Rev. Drug Discov., 2003, 2: 169~169.
[31] J K Nicholson, I D Wilson. Nat. Rev. Drug Discov., 2003, 2: 668~676.
[32] R B Stoughton, S H Friend. Nat. Rev. Drug Discov., 2005, 4: 345~350.
[33] W Weckwerth. Annu. Rev. Plant Biol., 2003, 54: 669~689.
[34] D A Fell. Trends Genet., 2001, 17: 680~682.
[35] L L Smith. Trends Pharmacol. Sci., 2001, 22: 281~285.
[36] S Ekins, Y Nikolsky, T Nikolskaya. Trends Pharmacol. Sci., 2005, 26: 202~209.
[37] N T Wood. Trends Plant Sci., 2001, 6: 191~191.
[38] J Memelink. Trends Plant Sci., 2005, 10: 305~307.
[39] S K Herbert. Proc. Natl. Acad. Sci. U. S. A., 2002, 99: 12518~12519.
[40] J D Mougous, M D Leavell, R H Senaratne et al. Proc. Natl. Acad. Sci. U. S. A., 2002, 99: 17037~17042.
[41] A Zewail, M W Xie, Y Xing et al. Proc. Natl. Acad. Sci. U. S. A., 2003, 100: 3345~3350.
[42] J Browse, B M Lange. Proc. Natl. Acad. Sci. U. S. A., 2004, 101: 14996~14997.
[43] D R Janero, N S Bryan, F Saijo et al. Proc. Natl. Acad. Sci. U. S. A., 2004, 101: 16958~16963.
[44] Y L Wang, E Holmes, J K Nicholson et al. Proc. Natl. Acad. Sci. U. S. A., 2004, 101: 12676~12681.
[45] D Cook, S Fowler, O Fiehn et al. Proc. Natl. Acad. Sci. U. S. A., 2004, 101: 15243~15248.
[46] W Weckwerth, M E Loureiro, K Wenzel et al. Proc. Natl. Acad. Sci. U. S. A., 2004, 101: 7809~7814.
[47] M Y Hirai, M Yano, D B Goodenowe et al. Proc. Natl. Acad. Sci. U. S. A., 2004, 101: 10205~10210.
[48] J E Ippolito, J Xu, S J Jain et al. Proc. Natl. Acad. Sci. U. S. A., 2005, 102: 9901~9906.
[49] G S Catchpole, M Beckmann, D P Enot et al. Proc. Natl. Acad. Sci. U. S. A., 2005, 102: 14458~14462.
[50] C Kristensen, M Morant, C E Olsen et al. Proc. Natl. Acad. Sci. U. S. A., 2005, 102: 1779~1784.
[51] H Bono, I Nikaido, T Kasukawa et al. Genome Res., 2003, 13: 1345~1349.
[52] O C Yoder, B G Turgeon. Curr. Opin. Plant Biol., 2001, 4: 315~321.
[53] M Fehr, D W Ehrhardt, S Lalonde et al. Curr. Opin. Plant Biol., 2004, 7: 345~351.
[54] E Fridman, E Pichersky. Curr. Opin. Plant Biol., 2005, 8: 242~248.
[55] J L Griffin. Curr. Opin. Chem. Biol., 2003, 7: 648~654.
[56] J van der Greef, P Stroobant, R van der Heijden. Curr. Opin. Chem. Biol., 2004, 8: 559~565.
[57] H O Villar, J L Yan, M R Hansen. Curr. Opin. Chem. Biol., 2004, 8: 387~391.
[58] J Minshull, J E Ness, C Gustafsson et al. Curr. Opin. Chem. Biol., 2005, 9: 202~209.
[59] A Saghatelian, B F Cravatt. Curr. Opin. Chem. Biol., 2005, 9: 62~68.
[60] D Seo, G S Ginsburg. Curr. Opin. Chem. Biol., 2005, 9: 381~386.
[61] M Morris, S M Watkins. Curr. Opin. Chem. Biol., 2005, 9: 407~412.
[62] D B Kell, R D King. Trends Biotechnol., 2000, 18: 93~98.
[63] T M Kutchan. Trends Biotechnol., 2005, 23: 381~383.
[64] S G Villas-Boas, S Rasmussen,G A Lane. Trends Biotechnol., 2005, 23: 385~386.
[65] M J van der Werf. Trends Biotechnol., 2005, 23: 11~16.
[66] C Birkemeyer, A Luedemann, C Wagner, et al. Trends Biotechnol., 2005, 23: 28~33.
[67] D Edwards, J Batley. Trends Biotechnol., 2004, 22: 232~237.
[68] R Goodacre, S Vaidyanathan, W B Dunn et al. Trends Biotechnol., 2004, 22: 245~252.
[69] A M Burja, S Dhamwichukorn, P C Wright. Trends Biotechnol., 2003, 21: 504~511.
[70] P Brazhnik, A de la Fuente, P Mendes. Trends Biotechnol., 2002, 20: 467~472.
[71] G H Thomas. Trends Biotechnol., 2001, 19: 126~127.
[72] M Tomita. Trends Biotechnol., 2001, 19: 205~210.
[73] T J Phelps, A V Palumbo, A S Beliaev. Curr. Opin. Biotechnol., 2002, 13: 20~24.
[74] B van Ommen,R Stierum. Curr. Opin. Biotechnol., 2002, 13: 517~521.
[75] M Arita, M Robert, M Tomita. Curr. Opin. Biotechnol., 2005, 16: 344~349.
[76] K M Oksman-Caldentey, K Saito. Curr. Opin. Biotechnol., 2005, 16: 174~179.
[77] M Stitt, A R Fernie. Curr. Opin. Biotechnol., 2003, 14: 136~144.
[78] G Hofmann, M McIntyre, J Nielsen. Curr. Opin. Biotechnol., 2003, 14: 226~231.
[79] S M Watkins, J B German. Curr. Opin. Biotechnol., 2002, 13: 512~516.
[80] W Weckwerth, O Fiehn. Curr. Opin. Biotechnol., 2002, 13: 156~160.
[81] D Delneri, F L Brancia, S G Oliver. Curr. Opin. Biotechnol., 2001, 12: 87~91.
[82] L Aicher, D Wahl, A Arce et al. Electrophoresis, 1998, 19: 1998~2003.
[83] M J Geisow. Nat. Biotechnol., 1998, 16: 206~206.
[84] N L Anderson, J Taylor, J P Hofmann et al. Toxicol. Pathol., 1996, 24: 72~76.
[85] J K Nicholson, E Holmes, I D Wilson. Nat. Rev. Microbiol., 2005, 3: 431~438.
[86] J Xu, J I Gordon. Proc. Natl. Acad. Sci. USA, 2003, 100: 10452~10459.
[87] J C Lindon, E Holmes, J K Nicholson. Prog. Nucl. Magn. Reson. Spectrosc., 2001, 39: 1~40.
[88] Y L Wang, M E Bollard, H Keun et al. Anal. Biochem., 2003, 323: 26~32.
[89] M Rooney, J Troke, J K Nicholson et al. Magn. Reson. Med., 2003, 50: 925~930.
[90] H Vilca-Melendez, I F Duarte, R Girlanda et al. Hepatology, 2005, 42: 338A~338A.
[91] P K Valonen, J L Griffin, K K Lehtimaki et al. NMR Biomed., 2005, 18: 252~259.
[92] T M Tsang, J L Griffin, J Haselden et al. Magn. Reson. Med., 2005, 53: 1018~1024.
[93] E M Ratai, S Pilkenton, M R Lentz et al. NMR Biomed., 2005, 18: 242~251.
[94] J L Taylor, C L Wu, D Cory et al. Magn. Reson. Med., 2003, 50: 627~632.
[95] C L Wu, J L Taylor, W L He et al. Magn. Reson. Med., 2003, 50: 1307~1311.
[96] M A Burns, W L He, C L Wu et al. Technol. Cancer Res. Treat., 2004, 3: 591~598.
[97] B M Beckwith-Hall, N A Thompson, J K Nicholson et al. Analyst, 2003, 128: 814~818.
[98] H R Tang, Y L Wang, J K Nicholson et al. Anal. Biochem., 2004, 325: 260~272.
[99] L H Lucas, C K Larive, P S Wilkinson et al. J. Pharm. Biomed. Anal., 2005, 39: 156~163.
[100] J C Lindon, J K Nicholson, E Holmes et al. Toxicol. Appl. Pharmacol., 2003, 187: 137~146.
[101] J C Lindon, H C Keun, T M D Ebbels et al. Pharmacogenomics, 2005, 6: 691~699.
[102] M A Constantinou, E Papakonstantinou, M Spraul et al. Anal. Chim. Acta, 2005, 542: 169~177.
[103] M A Constantinou, E Papakonstantinou, D Benaki et al. Anal. Chim. Acta, 2004, 511: 303~312.
[104] S H Moolenaar, U F H Engelke, R A Wevers. Ann. Clin. Biochem., 2003, 40: 16~24.
[105] K Odunsi, R Wollman, C Ambrosone et al. J. Soc. Gynecol. Invest., 2004, 11: 70A~70A.
[106] K S Solanky, N J Bailey, B M Beckwith-Hall et al. J. Nutr. Biochem., 2005, 16: 236~244.
[107] Y L Wang, H R Tang, J K Nicholson et al. J. Agric. Food Chem., 2005, 53: 191~196.
[108] B Teusink, F Baganz, H V Westerhoff et al. Method Microbiol., 1998, 26: 297~336.
[109] J G Bundy, E M Lenz, N J Bailey et al. Environ. Toxicol. Chem., 2002, 21: 1966~1972.
注:本文為提供者整理翻譯的,由于知識所限,錯誤在所難免,敬請原諒。如有問題可以查找原文。
統計數據
共收錄化學品數據
147579 條



 滬公網安備 31010602001115號
滬公網安備 31010602001115號