“消相反應(yīng)”在合成中的應(yīng)用
- 2012-07-09
- 專題
對于比較劇烈的放熱反應(yīng),一般通過低溫下緩慢滴加反應(yīng)物來進行調(diào)控。這種反應(yīng)條件一方面使操作變得復(fù)雜,另一方面需要額外消耗能量來維持低溫,這對于大規(guī)模工業(yè)化生產(chǎn)是非常不利的。近年來,隨著氟化學(xué)的發(fā)展而誕生的“消相反應(yīng)”(Phase-Vanishing Reactions)[1]很好地解決了這一問題。利用“消相反應(yīng)”,可使反應(yīng)物和底物在反應(yīng)初期被氟相間隔而不混合,并通過氟相相互進行微量傳遞,進而使得放熱反應(yīng)在室溫下可控進行。這不僅大大簡化了反應(yīng)操作,而且無需額外消耗能量。從這點來看,“消相反應(yīng)”在工業(yè)上具有潛在的應(yīng)用價值。
這一領(lǐng)域的發(fā)展始于20世紀(jì)90年代初,Vogt 等[2]首先報道了氟溶劑和有機溶劑的相溶性具有溫度依賴性。接著Horvath等[3]發(fā)明了氟兩相催化(Fluorous Biphasic Catalysis, FBC) 體系來回收催化劑。這一新概念的提出,立即引起了化學(xué)界的廣泛關(guān)注。在1996 年后,氟化學(xué)在有機合成領(lǐng)域的應(yīng)用得到了飛速發(fā)展,一些重要的進展包括氟相分離(Fluorous Separations) 技術(shù)[4~10]、氟相組合化學(xué)(Fluorous Combination Chemistry)[11]、氟三相反應(yīng)(Fluorous Triphasic Reactions)[12]、“消相反應(yīng)”(Phase-Vanishing Reactions)[1]等。本文主要介紹“消相反應(yīng)”的研究進展,并簡要介紹筆者在高分子合成方面的初步研究工作,其它方面的研究進展可參見近期的綜述[13~22]。
1 “消相反應(yīng)”的原理
1.1 基本原理
“消相反應(yīng)”是氟三相反應(yīng)的一種變體,其機理有兩種[23]。一是擴散機理,第一相的有機或無機底物擴散到氟相(第二相),然后在第三相與底物反應(yīng)。在反應(yīng)過程中,反應(yīng)物相消失,由此而命名為“消相反應(yīng)”。另一是萃取機理,先通過溶劑擴散,頂部相密度逐漸增大,底部相密度逐漸減少;當(dāng)頂部相密度接于中間氟相密度時,就以小液滴的形式穿過氟相到達底物相;小液滴中溶有部分反應(yīng)物,這樣就使得反應(yīng)物和底物相接觸并發(fā)生反應(yīng)。擴散機理限于能溶于氟相的底物或反應(yīng)物,而萃取機理適用于不溶于氟相的反應(yīng)物。
1.2 基本過程
在“消相反應(yīng)”中,多使用氟溶劑作為間隔介質(zhì),使有機底物和反應(yīng)物在反應(yīng)初期不相互混合。這主要是利用氟溶劑特殊的物理性能,即氟溶劑和大多數(shù)有機試劑不相溶,而且比大多數(shù)有機試劑重[12]。如果反應(yīng)物(如鹵化物)密度比氟溶劑大,則反應(yīng)可在試管中進行(圖1)。反應(yīng)結(jié)束后,產(chǎn)物留在上層有機相而底部則出現(xiàn)相消失。如果底物和反應(yīng)物都比氟溶劑輕,則相消失反應(yīng)可在U 形管中進行(圖1)。當(dāng)反應(yīng)結(jié)束時,底物和反應(yīng)物相中必有一相消失[22]。
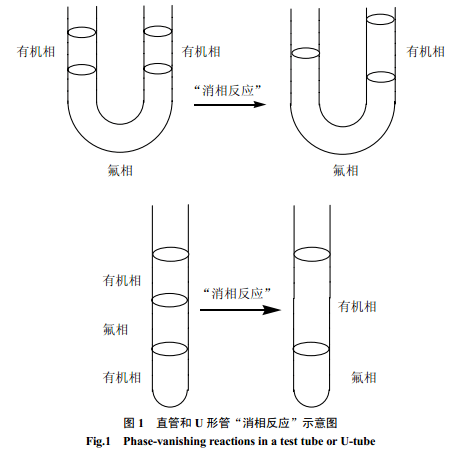
2 “消相反應(yīng)”的應(yīng)用
2.1 溴化反應(yīng)
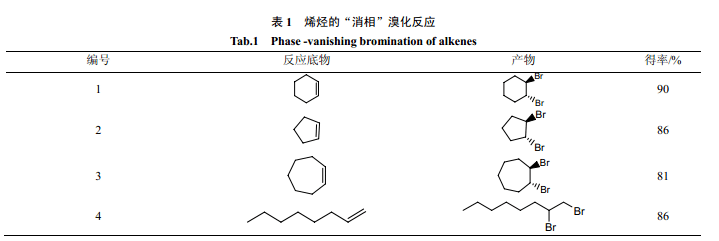
2002 年,Curran 等[12]最先報道了“消相反應(yīng)”。他們在室溫下,以全氟己烷為屏蔽相,用液溴對不同的烯烴進行溴化反應(yīng)(表1)。當(dāng)反應(yīng)進行完全時,液溴層消失,氟相恢復(fù)透明。研究表明,在保持三相體系條件下,對液溴層進行緩慢的攪拌能大大提高反應(yīng)速度。
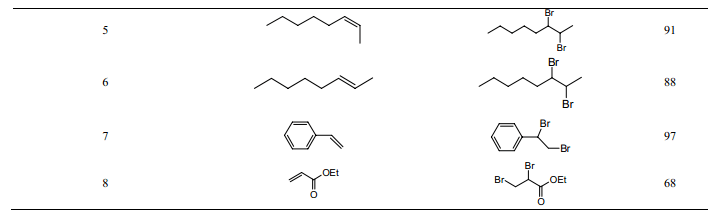
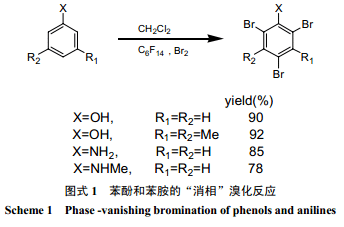
Verkade等[24]利用“消相反應(yīng)”,用液溴對酚類和苯胺類有機物進行了溴化,得率較高(圖式 1) 。
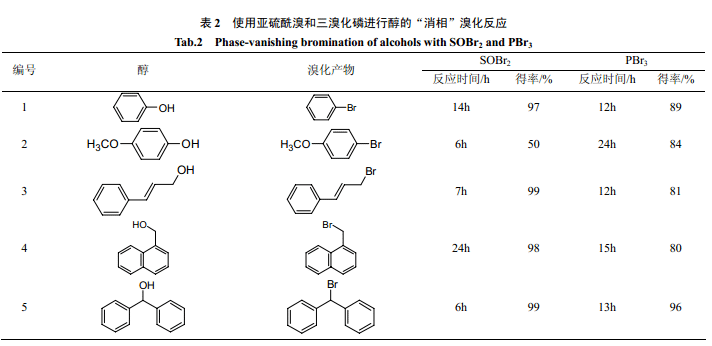
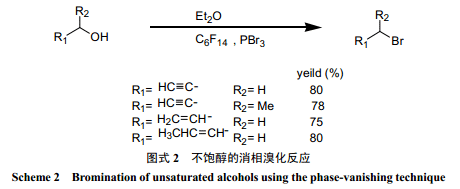
Ryu 等[25]分別用亞硫酰溴和三溴化磷進行了醇的消相溴化反應(yīng)。在消相反應(yīng)中,亞硫酰溴的溴化效果明顯好于三溴化磷。另外從反應(yīng)的得率來看,也比較高。由于消相反應(yīng)存在傳質(zhì)過程,所以反應(yīng)時間要比單一液相反應(yīng)長。Verkade等[24]用三溴化磷對帶炔丙基和烯丙基的不飽和醇進行了消相溴化反應(yīng)(圖式 2)。
2.2 氯化反應(yīng)
Jernej 等[26]在氟三相體系下,用氯氣對烯烴進行氯化反應(yīng)。這個反應(yīng)利用了氟溶劑易溶解氯氣的特性。當(dāng)烯烴被完全消耗后,底物相由于溶解了氯氣而變黃,所以通過有機相顏色的變化可以判斷底物是否反應(yīng)完全。和許多用氯氣直接氯化的反應(yīng)相比,在U 形管中通過氟相傳遞的氯化反應(yīng)有許多優(yōu)點:第一,反應(yīng)相和本體反應(yīng)物是分離的,這點對于像氯氣這樣非常活潑、危險和強腐蝕性的物質(zhì)來說尤其重要;第二,通過氟相傳遞氯氣的過程是比較緩慢的,這種緩慢加入反應(yīng)物的過程對于活潑的反應(yīng)物和放熱反應(yīng)非常有利;第三,氟溶劑的回收利用率高。

Ryu 等[25]在U 形管裝置中,分別用亞硫酰氯和三氯化磷進行了醇的氯化反應(yīng)。他們還用亞硫酰氯進行了平行氯化反應(yīng),驗證了三相U 型反應(yīng)體系也適用于平行反應(yīng)。
2.3 氧化反應(yīng)
Verkade等[24]用間氯過氧苯甲酸(m-CPBA )進行了胺、硫化物和烯烴的“消相”氧化反應(yīng),得率接近文獻報道的最大值。在三相體系中,m-CPBA 溶于密度大于全氟己烷的1,2-二溴乙烷,形成下層有機相;底物溶于一般的有機溶劑,形成上層有機相;氟相作為中間間隔介質(zhì)。完全反應(yīng)時,上層或下層有機相消失。后來Curran 指出Verkade進行的“消相”氧化反應(yīng)機理屬于萃取機理。上層或下層有機相消失取決于最終有機相的密度。Vrkade使用1,2-二溴乙烷來溶解比氟溶劑輕且難溶于氟相的有機物,這一方法大大拓寬了“消相反應(yīng)”的應(yīng)用范圍。

2.4 烷基化反應(yīng)和脫烷基化反應(yīng)
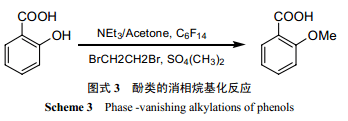
利用硫酸二甲酯進行酚類的烷基化反應(yīng)一般要在回流條件下進行。但 Verkade等[24]發(fā)現(xiàn),利用“消相反應(yīng)”,在室溫下就可用硫酸二甲酯進行水楊酸的烷基化反應(yīng),得率高于以往文獻報道的最大值(圖式 3) 。
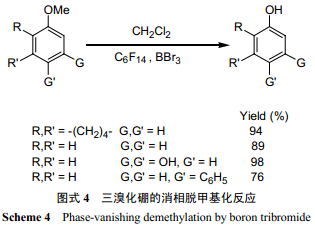
三溴化硼是高效的醚類脫烷基化試劑,而且其密度比全氟己烷大。三溴化硼的脫烷基化反應(yīng)是個高度放熱反應(yīng),一般需要在低溫下進行。但 Curran 等[1]利用“消相反應(yīng)”,在室溫下用三溴化硼對苯甲醚進行了脫甲基化反應(yīng)(圖式 4)。
2.5 付氏酰基化反應(yīng)
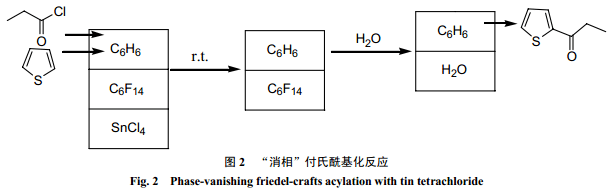
Ryu 等[27]利用消相反應(yīng),成功地用四氯化錫對噻吩進行了付氏酰基化反應(yīng)。在三相體系中,噻吩和丙酰氯溶于苯形成上層有機相,四氯化錫形成底相,全氟己烷作為中間間隔介質(zhì)。反應(yīng)結(jié)束時,底相消失,產(chǎn)物從上層有機相得到(圖2) 。
3 氟三相體系下甲基丙烯酸甲酯的氧化還原自由基聚合
氟三相體系以及消相反應(yīng)的應(yīng)用目前主要集中在有機物合成以及產(chǎn)物分離方面,在高分子合成研究領(lǐng)域的應(yīng)用尚鮮見報道。筆者在氟三相體系下進行了聚合反應(yīng)嘗試,并成功地實現(xiàn)了甲基丙烯酸甲酯氧化還原自由基聚合,在引發(fā)劑側(cè)得到了分子量分布較窄的聚甲基丙烯酸甲酯,多分散系數(shù)為1.38 ,反應(yīng)示意圖如圖 3 所示[28]。

實驗結(jié)果表明,氟試劑的屏蔽作用使得引發(fā)劑和單體相分離,導(dǎo)致兩側(cè)自由基濃度產(chǎn)生巨大差異,并最終使得兩側(cè)所得聚合物的分子量和多分散系數(shù)明顯不同。引發(fā)劑側(cè)之所以能得到分子量分布較窄的聚合物,很可能是由于該側(cè)自由基濃度大而單體濃度低所致。目前,該聚合體系的動力學(xué)正在進一步研究之中,有望產(chǎn)生一種新的高分子合成方法。
4 結(jié)語
雖然消相反應(yīng)體系的研究仍處于初始階段,但是許多研究成果表明消相反應(yīng)在合成上有著巨大的應(yīng)用潛力。利用消相反應(yīng),在室溫下可使放熱反應(yīng)緩慢和可控地進行,無需外加設(shè)備。消相反應(yīng)的節(jié)能優(yōu)點,使它具備了大規(guī)模工業(yè)化生產(chǎn)的潛力。但氟試劑價錢高、環(huán)境污染和對人體有害等是該技術(shù)的不利因素。反應(yīng)時間長是該技術(shù)的另一個明顯不足。因此,目前該技術(shù)的一個重要研究方向是通過調(diào)節(jié)氟三相體系的溶劑組成、用量和相界面的截面積來提高有機物在氟相的擴散速度,縮短反應(yīng)時間[23]。相信隨著氟相技術(shù)的不斷發(fā)展,其工業(yè)化進程必將大大加快。
參考文獻
[1] I Ryu, H Matsubara, D P Curran et al. J. Am. Chem. Soc., 2002, 124: 12946~12947.
[2] D W Zhu. Synthesis, 1993: 953~954.
[3] I THorvath, T Rabai. Science, 1994, 266: 72~75.
[4] D P Curran. Synlett, 2001: 1488~1496.
[5] D P Curran, Z Luo. J. Am. Chem. Soc., 1999, 121: 9069~9072.
[6] D P Curran, Y Oderaotoshi. Tetrahedron, 2001, 57: 5243~5253.
[7] W Zhang, Z Luo, D P Curran. J. Am. Chem. Soc., 2002, 124: 10443~10450.
[8] Y Nakamura, S Takeuchi, K Okumura. Tetrahedron Lett., 2003, 44: 6221~6225.
[9] H Matsuzawa, K Mikami. Tetrahed Lett., 2003, 44: 6227~6230.
[10] H Matsuzawa, K Mikami. Synlett., 2002: 1607~1613.
[11] Z Luo, Q Zhang, D PCurran. Science, 2001, 291: 1766~1769.
[12] N Hiroyuki, L Bruno, D P Curran et al. J. Am. Chem. Soc., 2001, 123: 10119~10120.
[13] I T Horvath. Acc. Chem. Res., 1998, 31: 641~650.
[14] E Wolf , G Koten, B Deelman. J. Chem. Soc. Rev., 1999, 28: 37~41.
[15] M Cavazzinni, F Montannari, G Pozzi et al. J. Fluorine Chem., 1999, 94: 183~193.
[16] D P Curran. Med. Res. Rev., 1999, 19: 432~438.
[17] D P Curran. Pure Appl. Chem., 2000, 72:1649~1653.
[18] J A Gladysz, D P Curran. Tetrahedron, 2002, 58: 3823~3825.
[19] C C Tzschucke, C Markert, W Bannwarth et al. Angew. Chem. Int. Ed., 2002, 41: 3964~4000.
[20] A P Dobbs, M R Kimberley. J. Fluorine Chem., 2002, 118: 3~7.
[21] J I Yoshida, K Itami. Chem. Rev. 2002, 102: 3693~3716.
[22] W Zhang. Chem. Rev., 2004, 104: 2531~2556.
[23] D P Curran. Org. Lett., 2004, 6: 1021~1204.
[24] N K Jana, J G Verkade. Org. Lett., 2003, 5: 3787~3790.
[25] H Nakamura, T Usui, I Ryu et al. Org. Lett., 2003 , 5 :1167~1169.
[26] I Jernej, S Stojan, Z Marko. Chem. Commun., 2003, 2496~2497.
[27] H Matsubasa, S Yasuda, I Ryu. Synlett, 2003: 247~249.
[28] S Z Chen, Y P Bai, Z L Li. Chinese Chemical Letters, 2006, 17:258~260.
注:本文為提供者整理翻譯的,由于知識所限,錯誤在所難免,敬請原諒。如有問題可以查找原文。
統(tǒng)計數(shù)據(jù)
共收錄化學(xué)品數(shù)據(jù)
147579 條



 滬公網(wǎng)安備 31010602001115號
滬公網(wǎng)安備 31010602001115號